
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гниение аминокислот, обезвреживание продуктов гниения ⇐ ПредыдущаяСтр 10 из 10
ГНИЕНИЕ АМИНОКИСЛОТ Аминокислоты, которые не подверглись всасыванию, поступают в толстую кишку, где подвергаются гниению. ГНИЕНИЕ АМИНОКИСЛОТ - это процесс распада аминокислот под действием ферментов, вырабатывающихся микрофлорой толстого отдела кишечника. Аминокислоты при гниении подвергаются следующим превращениям:
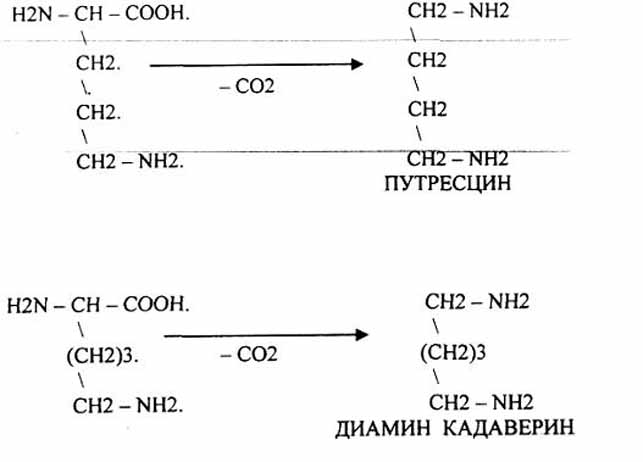
РЕАКЦИИ ДЕКАРБОКСИЛИРОВАНИЯ: Подвергаются орнитин и лизин. ОРНИТИН в состав белков не входит, но обязательно содержится в организме. Проукты декарбоксилирования - ПУТРЕСЦИН и КАДАВЕРИН - являются токсическими веществами. Они входят в состав трупных ядов.
Десульфированию подвергаются серосодержащие аминокислоты (метионин, цистеин). В результате образуются сероводород, метилмеркаптан. РАСПАД ЦИКЛИЧЕСКИХ АМИНОКИСЛОТ При распаде тирозина, фенилаланина, триптофана образуются метан, углекислый газ, аммиак, фенол, крезол, индол. Все эти вещества токсические. Они поступают в печень, где и происходит их обезвреживание. В печени имеется две системы, участвующие в обезвреживании этих веществ: 1.УДФГК - УРИДИНДИФОСФОГЛЮКУРОНОВАЯ К-ТА. 2.ФАФС-ФОСФОАДЕНОЗИНФОСФОСУЛЬФАТ. Процесс обезвреживания - это процесс конъюгации токсических веществ с компонентами одной из этих систем, и образования конъюгатов, которые являются уже нетоксичными веществами.
ИНДОКСИЛСУЛЬФАТ нейтрализуется и превращается в натриевую или калиевую соль. Все эти вещества выводятся из организма с мочой. В норме реакция на индол должна быть отрицательна. При положительной реакции на индол - нарушена обезвреживающая функция печени. Положительная реакция на ИНДИКАН наблюдается при очень активном гниении белков в толстом кишечнике. Метаболизм аминокислот Метаболизм аминокислот Источниками аминокислот в клетке являются: 1.белки пищи после их гидролиза в органах пищеварения; 2.синтез заменимых аминокислот; 3.распад тканевых белков. Тканевые белки подвергаются гидролитическому расщеплению при участии тканевых ПРОТЕАЗ - КАТЕПСИНОВ, которые в основном находятся в ЛИЗОСОМАХ. Выделяют разные КАТЕПСИНЫ, которые отличаются оптимумом рН и специфичностью действия. Распад тканевых белков необходим для обновления белков, а также для устранения дефектных молекул белка.
Несмотря на то, что почти для каждой аминокислоты выяснены индивидуальные пути обмена, известен ряд превращений, общих для многих аминокислот: ТРАНСАМИНИРОВАНИЕ; ДЕКАРБОКСИЛИРОВАНИЕ; ДЕЗАМИНИРОВАНИЕ. ТРАНСАМИНИРОВАНИЕ – реакции межмолекулярного переноса аминогруппы от аминокислоты на кетокислоту без промежуточного образования аммиака. Особенности реакций трансаминирования: протекают при участии ферментов - аминотрансфераз; для реакций необходим кофермент – пиридоксальфосфат (ПФ); реакции обратимы; могут подвергаться все аминокислоты кроме лиз, тре; в результате реакции образуются новая аминокислота и новая кетокислота.
1.Синтез заменимых аминокислот. При этом происходит перераспределение азота в органах и тканях; 2.Являются начальным этапом катаболизма аминокислот. Реакции ДЕКАРБОКСИЛИРОВАНИЯ – отщепление альфа – карбоксильной группы аминокислот в виде углекислого газа. При этом аминокислоты в тканях образуют биогенные амины, которые являются биологически активными веществами (БАВ). Среди них могут быть соединения, которые выполняют функции: 1.НЕЙРОМЕДИАТОРОВ (СЕРОТОНИН, ДОФАМИН, ГАМК), 2. Гормоны (АДРЕНАЛИН, НОРАДРЕНАЛИН), 3. Регуляторы местного действия (ГИСТАМИН).
ДОФАМИН является НЕЙРОМЕДИАТОРОМ возбуждающего действия. Он является основой для синтеза АДРЕНАЛИНА и НОРАДРЕНАЛИНА.
Этому виду дезаминирования подвергаются остальные аминокислоты, но через стадию трансаминирования с альфа-кетоглутаровой кислотой. Затем глутаминовая кислота (продукт этой реакции) подвергается окислительному дезаминированию.
Пути обезвреживания аммиака Аммиак образуется из аминокислот при распаде других азотсодержащих соединений (биогенных аминов, НУКЛЕОТИДОВ). Значительная часть аммиака образуется в толстой кишке при гниении. Он всасывается в кровь системы воротной вены, здесь концентрация аммиака больше, чем в общем кровотоке.Аммиак образуется в различных тканях. Концентрация его в крови незначительна, т.к. он является токсичным веществом (0,4 - 0,7мг/л). Особенно выраженное токсическое действие он оказывает на нервные клетки, поэтому значительное его повышение приводит к серьёзным нарушениям обменных процессов в нервной ткани.
ПУТИ ОБЕЗВРЕЖИВАНИЯ АММИАКА. 1. образование АМИДОВ
2. Восстановительное АМИНИРОВАНИЕ альфа – кетоглутаровой кислоты
4. Синтез мочевины - основной путь обезвреживания аммиака - ОРНИТИНОВЫЙ ЦИКЛ.
АРГИНАЗА обладает абсолютной специфичностью и содержится только в печени. В составе мочевины содержится два атома азота: один поступает из аммиака, а другой выводится из АСП. Образование мочевины идёт только в печени. Две первые реакции цикла (образование ЦИТРУЛЛИНА и АРГИНИНОСУКЦИНАТА) идут в МИТОХОНДРИЯХ, остальные в цитоплазме. В организме в сутки образуется 25г мочевины. Этот показатель характеризует мочевинообразовательную функцию печени. Мочевина из печени поступает в почки, где и выводится из организма, как конечный продукт азотистого обмена. Глюконеогенез ГЛЮКОНЕОГЕНЕЗ Основными источниками глюкозы для организма человека являются: 1. углеводы пищи; 2. гликоген тканей; 3. глюконеогенез. ГЛЮКОНЕОГЕНЕЗ - это биосинтез глюкозы из неуглеводных предшественников, главными из которых являются ПИРУВАТ, ЛАКТАТ, ГЛИЦЕРИН, МЕТАБОЛИТЫ ЦТК КРЕБСА, АМИНОКИСЛОТЫ. ГЛЮКОНЕОГЕНЕЗ возможен не во всех тканях. Главным местом синтеза глюкозы является печень, в меньшей степени процесс идёт в почках и слизистой кишечника. Биологическая роль глюконеогенеза заключается не только в синтезе глюкозы, но и в возвращении лактата, образованного в реакциях анаэробного ГЛИКОЛИЗА, в клеточный фонд углеводов. За счет этого процесса поддерживается уровень глюкозы в тканях в кризисных ситуациях (при углеводном голодании, сахарном диабете, тканевой гипоксии). Большинство реакций ГЛЮКОНЕОГЕНЕЗА представляют собой обратные реакции ГЛИКОЛИЗА, за исключением трёх термодинамически необратимых: ПИРУВАТКИНАЗНОЙ, ФОСФОФРУКТОКИНАЗНОЙ, ГЕКСОКИНАЗНОЙ. Эти реакции при ГЛЮКОНЕОГЕНЕЗЕ имеют обходные пути и связаны с образованием 2-фосфоенолпирувата, фруктозо-6-фосфата и глюкозы. Обходные реакции Образовавшаяся в реакциях глюконеогенеза, глюкоза может вновь участвовать в клеточном метаболизме как пластический, энергетический материал, откладываться про запас в виде гликогена.
|
||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 1052; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.136.97.64 (0.011 с.) |
 ВОССТАНОВИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ: (на примере аланина)
ВОССТАНОВИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ: (на примере аланина) ДЕСУЛЬФИРОВАНИЕ
ДЕСУЛЬФИРОВАНИЕ Роль реакций ТРАНСАМИНИРОВАНИЯ:
Роль реакций ТРАНСАМИНИРОВАНИЯ: ГАМК является НЕЙРОМЕДИАТОРОМ тормозного действия, поэтому препараты на основе ГАМК используются в клинике для лечения некоторых заболеваний ЦНС. Эта реакция используется в педиатрической практике: детям при сильном возбуждении используют раствор витамина В6, который стимулирует процесс образования ГАМК.
ГАМК является НЕЙРОМЕДИАТОРОМ тормозного действия, поэтому препараты на основе ГАМК используются в клинике для лечения некоторых заболеваний ЦНС. Эта реакция используется в педиатрической практике: детям при сильном возбуждении используют раствор витамина В6, который стимулирует процесс образования ГАМК. Реакции ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы в виде аммиака. ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ. Непосредственно, ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ подвергается только ГЛУ.
Реакции ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы в виде аммиака. ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ. Непосредственно, ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ подвергается только ГЛУ.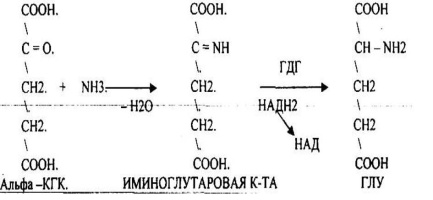 НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ
НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ ГЛУТАМИН и АСПАРАГИН - нетоксические вещества. Их называют транспортной формой аммиака в организме. Они не проникают через мембраны и в почках распадаются до аминокислот и аммиака.
ГЛУТАМИН и АСПАРАГИН - нетоксические вещества. Их называют транспортной формой аммиака в организме. Они не проникают через мембраны и в почках распадаются до аминокислот и аммиака. 3. Образование солей АММОНИЯ
3. Образование солей АММОНИЯ



