
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Энергетический метаболизм миокардаСодержание книги Поиск на нашем сайте
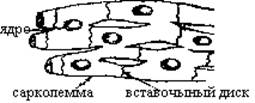
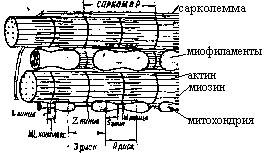
Ультраструктура миокарда Мышечные волокна сердца состоят из отдельных миоцитов, пересеченных через определенные промежутки вставочными дисками. Плазматическая мембрана миоцитов вместе с базальной мембраной формирует сарколемму (Сл). Через вставочные диски осуществляется электротоническая связь между миоцитами. В нормальных условиях ионная проницаемость вставочных дисков достаточно высока, чтобы обеспечить проведение возбуждения. При гибели одного из соседних миоцитов ионная проницаемость вставочного диска сразу же резко снижается.
А Б Рис. 1. Схематизированная структура миокарда в условиях световой (А) и электронной (Б) микроскопии
На границе саркомеров (участков миофибрилл, ограниченных двумя Z-дисками) Сл. образует впячивания Т-системы. В саркоплазме вблизи Т-систем располагаются митохондрии и цистерны саркоплазматическогок ретикулума (СР). Ультраструктурная организация миофибрилл представлена на рис. 1.
Механизм систолы Согласно теории Г. Хаксли, систола осуществляется благодаря скольжению актиновых протофибрилл вдоль миозиновых. При этом длина протофибрилл заметно не меняется. Активные протофибриллы (АП) втягиваются в анизотропный диск и сближаются в центре Н-зоны, которая исчезает. Миозиновые протофибриллы (МП) доходят до Z-мембраны, что приводит к исчезновению «И» диска (рис. 2). Мышечное сокращение - сложный физико-химический процесс, предусматривающий уменьшение длины саркомеров при сохранении их объема.
Рис. 2. Схема, представляющая
Взаимодействие актина и миозина определяется состоянием регуляторных белков - тропонина и тропомиозина, расположенных между протофибриллами. Регуляторные белки препятствуют образованию актомиозина в покое, снижая АТФ-азную активность миозина (рис. 3). Потенциал действия проводятся внутрь мышечного волокна Т-системой и вызывают приток кальция внутрь саркоплазмы (СП), а также выброс кальция из цистерн СР и митохондрий (рис. 4). Взаимодействие кальция и тропонина приводит к тому, что молекулы актина становятся доступными для образования связей МП и АП. При ассоциации АП и МП АТФ-азная активность миозина повышается) высвобожденная энергия затрачивается на конформационные изменения молекул миозина, обусловливающих скольжение нитей актина.
Активный перенос кальция через Сл и в цистерны СР приводит к восстановлению тропонинового блока и диастоличеекому расслаблению. Образовавшийся в процессе систолы аденозиндифосфат (АДФ) в момент расслабления вновь фосфорилируется в АТФ за счет креатиндифосфата. В связи с тем, что активный перенос кальция также требует затрат энергии, процесс расслабления не может эффективно осуществляться в отсутствие макроэргических фосфатов. При дефиците энергии сердце останавливается в систоле (на рис. 5-7 представлены последовательные этапы сокращения волокон миокарда и работы «калий-натриевого» насоса).
Эффективность работы сердца Здоровое сердце превращает около 40% энергии АТФ в механическую работу. При патологических состояниях КПД (ŋ) сердца резко снижается. Так, в условиях гипоксии внутриклеточное повышение концентрации лактата и свободных жирных кислот, разобщающих окисление и фосфорилирование, резко понижают эффективность работы сердца. КПД сердца определяется как соотношение Wвнешн./Wист., где Wвнешн. – внешняя ударная работа сердца (энергия, которую сердце сообщило перемещенной крови), а Wист. – полная величина работы, совершаемой сердцем. Внешняя работа сердца, измеряемая в кг/м, определяется формулой
где: Ра - среднее давление в аорте в кг/кв. м, Vуд. -ударный объем в м3, m - масса ударного объема в кг, v - скорость кровотока в аорте в м/с, g -9,81 м/с2 - ускорение свободного падения.
Истинная работа сердца всегда, даже в нормальных условиях, значительно больше внешней, так как внешняя работа сердца отражает результат его деятельности как насоса. При патологических состояниях превышение истинной работы над внешней становится еще значительнее. При недостаточности митрального клапана Wист. ≥ Wвнешн. за счет обратного тока крови через поврежденный клапан, при кардиосклерозе - из-за резкого увеличения внутреннего трения в миокарде. Таким образом, у ряда больных обеспечение нормального гемодинамического эффекта достигается ценой постоянной гиперфункции миокарда, которую практически невозможно учесть при определении внешней работы. Ранее предполагалось, что внешняя работа сердца изменяется пропорционально потреблению кислорода миокардом, однако Эванс и др., рассчитывая внешнюю работу сердца как произведение ударного объема на среднее систолическое давление, показали, что работа далеко не всегда изменяется пропорционально потреблению кислорода. Полученные результаты привели к заключению о том, что не работа, а напряжение миокарда является его главной функциональной характеристикой.
В целом, общая эффективность работы сердца зависит от следующих фактов: 1) эффективности преобразования энергии в миокарде, то есть преобразования энергии окисленных веществ в энергию концевой фосфатной связи АТФ (ŋф); 2) эффективности преобразования энергии концевой фосфатной связи АТФ в энергию напряжения миофибрилл (ŋсп.); 3) эффективности превращения энергии напряжения миофибрилл в общую работу сердца (ŋт) и, наконец, 4) эффективности превращения общей работы сердца в его внешнюю работу (ŋмех.). Общая эффективность пропорциональна произведению эффективности всех четырех этапов ŋобщ. = ŋфּŋиспּŋмех.
Подобный способ оценки эффективности работы сердца позволяет дифференцировать нарушения сократительной активности, обусловленные неполноценным обменом в миокарде, от процессов, связанных с преобразованием общей работы во внешнюю. При различных формах патологии может преобладать изменение обмена веществ или нарушение биомеханики. Данные прямых микрокалориметрических исследований сокращения миофибрилл ин витро свидетельствуют о том, что КПД гипертрофированного миокарда ниже, чем нормального. В настоящее время принято считать, что при каждой систоле в миокарде запасается часть энергии, которая в дальнейшем обеспечивает более эффективную диастолу. Расширение сердца во время диастолы обеспечивается энергией, запасающейся при систоле.
Существует, по крайней мере, два механизма, отвечающих за этот процесс (Томас Ф., Робинсон и др.). Один из них создается движением сердца как целого. Мы уже указывали, что при сокращении сердца кровь из чего выбрасывается вверх. В соответствии с законом Ньютона само сердце при этом смещается в противоположную сторону (вниз). Происходит растяжение крупных сосудов и соединительной ткани, удерживающих сердце. В момент расслабления сердце, благодаря упругости ткани, подтягивается кверху, что создает условия для повышения скорости движения крови относительно сердца и увеличению ее притока в полости. Второй механизм запасания энергии при сокращении сердца с целью дальнейшего использования в диастоле связан с деформацией самого миокарда. Предполагается, что во время систолы происходит сжатие упругих элементов сердечной мышцы, и после того, как систола завершена, полости сердца стремятся к расширению даже при отсутствии каких-либо внешних сил. Расширение объема замкнутой полости приводит к повышению степени разряжения в полостях, что также способствует более эффективному заполнению их кровью. Так, если в модели Отто Франка и Эрнеста Старлинга сердце рассматривается лишь как статически выкачивающий насос, то, согласно новой гипотезе, сердце отождествляется с динамической закачивающей системой. Закон Франка-Старлинга считался фундаментальным. Однако основные его положения были сформулированы на основании изучения деятельности изолированных сердец. В связи с этим, он справедлив лишь для сердец с угнетенной функцией, при которой сердечный выброс мал, а венозное давление значительно повышено.
Томас Ф. Робинсон и др. считают, что энергия, выделяющаяся при сокращении сердца, может запасаться и соединительной тканью, располагающейся между мышечными клетками сердца. Сетевидные соединительно-тканные структуры миокарда создают своеобразную «силу отдачи», которая способствует восстановлению исходной длины кардиомиоцитов после их сокращения. Кроме того, боковые поверхности кардиомиоцитов связаны друг с другом жгутообразными структурами - своеобразными распорками, состоящими из коллагена, скрученного в спираль подобно тросу. Данные образования обладают большим сопротивлением к растяжению. Их роль заключается в ограничении, сдерживании деформации сердца, что также способствует сохранению энергии деформации для создания присасывающего эффекта во время диастолы. При некоторых патологических состояниях отдача и присасывающий эффект сердца утрачиваются, вследствие чего могут изменяться характеристики его диастолического наполнения.
Сердечный цикл
Основные энерготраты приходятся на фазу изометрического сокращения в период напряжения. В связи с этим, нагрузка объемом (изотоническая гиперфункция), когда удлиняется период изгнания, энергетически более выгодна, чем нагрузка давлением (изометрическая гиперфункция), при которой удлиняется период напряжения. Рассматривая периоды сердечной деятельности, необходимо подчеркнуть, что их длительность различна для правого и левого отдела сердца, однако это не сказывается на ударном объеме. Имеется четкая координация в отношении ударных объемов, причем, малый круг кровообращения играет роль своеобразного демпфера, выравнивающего их разность. Основная функция системы кровообращения состоит, как известно, в транспорте кислорода и питательных веществ тканям и удалении продуктов обмена. Она может быть успешно выполнена только при условии обеспечения необходимой объемной скорости кровотока. Объемная скорость кровотока-количество крови, проходящее за одну минуту через поперечное сечение сосудов большого или малого круга кровообращения, известное физиологам и клиницистам как минутный объем крови (МОК).
МОК == СО ×ЧСС, где МОК - минутный объем крови в л; СО - систолический объем в л; ЧСС - частота сердечных сокращений. В эксперименте МОК и СО определяют при кровопускании, в клинике - по различным формулам с известными допущениями: С0== 100×0,5 ПД-0,6 ДД-0,6 В (формула Старра) ПД-пульсовое давление в мм рт. ст.; ДД-диастолическое давление в мм рт. ст.; В - возраст в годах. Следовательно, систолический объем находится в определенной зависимости от артериального давления во время систолы и диастолы. В свою очередь, систолическое, диастолическое и пульсовое давления определяются МОК и периферическим сопротивлением сосудистого русла. Благодаря наличию аортальной компрессионной камеры и эластическим свойствам сосудов пульсирующий кровоток преобразуется в артериолах и прекапиллярах в ламинарный. В связи с этим допустимо говорить о среднем динамическом давлении (СДД), которое представляет собой результирующую всех переменных давлений в артериях на протяжении сердечного цикла. При различных формах патологии сердца мы встретимся с изменениями всех перечисленных показателей, однако при явлениях сердечной недостаточности чаще всего наблюдается уменьшение СО или МОК. Организм поддерживает рабочий уровень СДД и МОК, регулируя частоту сердечных сокращений, общее периферическое сопротивление и венозный возврат. ПАТОФИЗИОЛОГИЯ ЭНДОКАРДА
Одной из наиболее частых причин нарушений гемодинамики является поражение внутренней оболочки сердца – эндокарда, сопровождающееся формированием пороков сердца. Пороки сердца - сборное понятие, объединяющее разнообразные формы патологии эндокарда. Обычно они подразделяются на две большие группы: врожденные и приобретенные. Врождённые пороки сердца Врожденные пороки сердца являются следствием внутриутробной патологии. Они могут быть сравнительно простыми - такими, как дефект межжелудочковой перегородки, или очень сложными - например, пентады Фалло. В зависимости от нарушений гемодинамики врожденные пороки можно разделить на 4 основные группы: 1.С неизмененным или мало измененным легочным кровотоком - аномалии дуги аорты или ее отсутствие, стеноз и коарктация аорты, стеноз левого атриовентрикулярного отверстия, недостаточность митрального клапана, пороки развития венечных артерий и др. 2. С гиперволемией малого круга кровообращения - дефект межжелудочковой перегородки, аортально-легочный свищ. 3. С гиповолемией малого круга кровообращения - триада, тетрада и пентада Фалло. 4. Комбинированные пороки - полная транспозиция аорты и легочной артерии, синдром Тауссинг-Бинга. Среди врожденных пороков сердца наиболее часто встречается дефект межжелудочковой и дефект межпредсердной перегородок. Размеры дефекта межжелудочковой перегородки могут достигать 3-4 см в диаметре. Артериовенозное шунтирование приводит к переполнению малого круга кровообращения и перегрузке обоих желудочков и левого предсердия.
Дефект межпредсердной перегородки диаметром менее 1 см практически не сопровождается какими-либо нарушениями гемодинамики. Длительное существование шунта может привести либо к развитию легочной гипертензии, либо к возникновению «относительного» стеноза легочной артерии. В силу большей емкости и растяжимости правого предсердия при одном и том же наполнении давление в его полости будет в 1,5-2 раза меньше, чем в левом. Кроме того, площадь правого атриовентрикулярного отверстия больше площади левого, что, в свою очередь, создает меньшее сопротивление диастолическому наполнению правого предсердия по сравнению с левым. Однако при развитии легочной гипертензии нагрузка на правый желудочек возрастает, работа его резко увеличивается. Принципы нарушений гемодинамики при других видах врожденных пороков в значительной степени напоминают изменения гемодинамики при приобретенных пороках и будут рассмотрены в соответствующих разделах.
Приобретённые пороки сердца Причинами приобретенных пороков могут быть ревматизм (в большинстве случаев), атеросклероз, сифилис, бактериальные и вирусные эндокардиты, травма. Стеноз левого атриовентрикулярного отверстия В нормальных условиях площадь левого атриовентрикулярного отверстия варьирует от 4 до 6 кв. см. Пока степень сужения невелика и площадь отверстия превышает 2 кв. см, компенсация происходит за счет некоторого растяжения и увеличения сократительной деятельности левого предсердия без заметного повышения давления в нем. Это усиление сократительной деятельности способствует до определенного предела прохождению оптимального количества крови через суженное отверстие. При большей степени стеноза отверстия нарушается давление в левом предсердии, которое на первых этапах носит компенсаторный характер. Более полному опорожнению предсердия способствует удлинение периода диастолического наполнения левого желудочка. В связи с высоким давлением в левом предсердии происходит более раннее открытие митрального клапана. Закрытие клапана происходит позже, во время изометрического сокращения желудочка, период которого удлиняется. При физической нагрузке, а затем и в покое, мышце левого желудочка приходится производить значительно большую работу, что неизбежно вызывает гипертрофию предсердия. Гипертрофия, однако, не бывает значительной, так как компенсаторные возможности предсердия ограничены. Как уже упоминалось, внешнюю работу можно рассчитать по формуле:
При митральном стенозе внешняя работа оказывается значительно уменьшенной по сравнению с общей работой миокарда, тогда как общая работа значительно больше, чем в норме. Это объясняется, в первую очередь, тем, что полость левого предсердия растягивается сильнее, в ней остается часть крови, которая должна была поступить в желудочек, предсердия сокращаются с большей силой, гипертрофируются. Если процесс стенозирования продолжается и, если к миокарду предъявляются повышенные требования, то увеличивающееся сопротивление оттоку крови вызывает еще большее растяжение полости левого предсердия, сокращения предсердия становятся малоэффективными. Возникает мерцание предсердий, которое приводит к еще большему застою крови. При сужении левого венозного отверстия до 1 кв. см сопротивление легочному кровотоку увеличивается в 15-20 раз. Это связано с функциональным спазмом легочных сосудов, к которому с течением времени присоединяется органическое поражение их стенок, в связи с чем препятствие для продвижения крови в легочных сосудах становится необратимым. Создается так называемый «второй барьер», возникновение которого на первых этапах носит компенсаторный характер - предохраняет организм от развития отека легких. Однако нагрузка на правый желудочек про должает возрастать. Очевидно, уместно снова вспомнить о модели А. Гайтона, согласно которой управление в ССС соответствует, в основном метаболическому принципу. Тогда возникновение «второго барьера» - повышение давления в системе малого круга кровообращения будет способствовать снижению систолического выброса правым желудочком и, таким образом, приведет к стабилизаци объемной скорости кровотока в сосудах легких. Как мы уже указывали, модель А. Гайтона не предусматривает введения «сверху» какого-либо установочного параметра. Управляющими величинами в данном случае будут являться скорость насыщения крови кислородом и константы водно-солевого гомеостаза в легких. Многие авторы (В. X. Василенко, В. Н. Маколкин и др.) считают, что повышение сопротивления в легочных артериолах, создающее «второй барьера», является более тяжелым для больного, чем сам стеноз. В свою очередь, повышение давления в системе легочной артерии приводит к расширению ее клапанного кольца. Возникает недостаточность клапанов легочной артерии, в результате чего часть крови начинает забрасываться обратно в правый желудочек, его полость дилятируется, он начинает сокращаться с большей силой, но увеличения работы при этом не происходит. Истинная работа правого желудочка иногда увеличивается в 8- 10 раз. В результате расширения фиброзного кольца трехстворчатого клапана развивается его функциональная недостаточность. Кровь возвращается в правое предсердие, что приводит к его расширению и падению работы сердца. Все это в конечном итоге приводит к повышению венозного давления, которое в полых венах вместо 90-110 мм водяного столба достигает 300 мм. Таким образом, даже при наличии компенсаторных реакций при стенозе левого атриовентрикулярного отверстия резко увеличивается внешняя работа сердца, что неизбежно сопровождается той или иной степенью недостаточности кровообращения. По мере уменьшения размеров митрального отверстия и количества крови, поступающей в сосудистое русло, развивается циркуляторная гипоксия. Длительное кислородное голодание вызывает дистрофические изменения тканей и нарушение функций органов, в первую очередь - головного мозга и миокарда. Недостаточность двустворчатого клапана В подавляющем большинстве случаев недостаточность митрального клапана является результатом ревматического эндокардита. Как правило, разрушается или само вещество клапана, или происходит склеивание створок с папиллярными мышцами, или развивается рубцовое сокращение хорд с оттягиванием створок клапана книзу. При этом становится невозможным смыкание створок клапана во время систолы левого желудочка. Ведущим патофизиологическим признаком недостаточности митрального клапана является регургитация (забрасывание) крови из левого желудочка в левое предсердие во время систолы. Тонкостенная и функционально более слабая полость левого предсердия вследствие постоянного поступления в нее большого количества крови значительно расширяется. Функция левого желудочка усилена вследствие переполнения его кровью, поступающей из левого предсердия (изотоническая гиперфункция). Усиленные сокращения обусловливают постепенное развитие гипертрофии миокарда левого желудочка. Возможность свободного опорожнения полости не создает благоприятных условий для увеличения количества резидуальной крови. В связи с этим полость левого желудочка увеличивается в меньшей степени, чем полость левого предсердия. Выраженная дилятация наступает лишь в поздней стадии заболевания или при сопутствующем ревматическом поражении миокарда. Расширение полости желудочка без увеличения его тонус приводит к сокращению как ударного, так и минутного объема. Следовательно, нарушается снабжение всех органов кровью, в том числе и самого миокарда. Гипоксия миокарда приводит к ещё большему уменьшению его сократительной способности и снижению объема периферической циркуляции. Нарушения всех жизненно необходимых реакций обмена носят, как и при митральном стенозе, преимущественно циркуляторный характер.
Стеноз правого атриовентрикулярного отверстия Механизм формирования стеноза правого атриовентрикулярного отверстия при ревматическом эндокардите полностью соответствует механизму формирования стеноза левого атриовентрикулярного отверстия, но стеноз правого венозного отверстия развивается значительно реже, чем левого. Если в норме площадь правого венозного отверстия составляет 6 кв. мм, то при стенозе она может уменьшаться до 1 кв. см. Однако уменьшение этого отверстия до 3,5 кв. мм вызывает выраженные нарушения гемодинамики. Стеноз правого атриовентрикулярного отверстия часто сочетается с той или иной степенью недостаточности клапанов. При стенозе правого венозного отверстия полость правого предсердия не может полностью освободиться во время систолы от крови, что приводит к повышению давления в правом предсердии. При значительной степени стеноза давление в полости правого предсердия сильно увеличивается и может достигать 30 мм ртутного столба, что приводит к выраженному растяжению правого предсердия и возникновению мерцательной аритмии. Градиент давлений между правым предсердием и желудочком (во время диастолы последнего) практически не определяемый в норме, резко возрастает при стенозе правого атриовентрикулярного отверстия. Это приводит к повышению давления в полых венах и быстро прогрессирующей недостаточности кровообращения. Следствием пониженного систолического объема и уменьшения внешней работы сердца является появление у таких больных выраженного цианоза, набухания шейных вен, повышения венозного давления, развития портальной гипертензии, увеличения печени, асцита, отека нижних конечностей и др. Характер проявлений декомпенсации при данном пороке такой же, как и при стенозе левого венозного отверстия в поздние стадии заболевания.
Недостаточность трехстворчатого клапана Различают органическую и относительную недостаточность трикуспидального клапана. Первая возникает вследствие ревматического поражения створок клапана, вторая является результатом резкого расширения и гипертрофии правого желудочка. При недостаточности трехстворчатого клапана часть крови во время систолы правого желудочка забрасывается в правое предсердие. Давление в правом предсердии повышается и приближается к давлению в правом желудочке. Соответственно повышается давление в полых венах и в венозной части большого круга кровообращения. С каждой систолой правого желудочка вследствие обратного поступления крови в правое предсердие, толчок ее передается не только в полые вены, но также в шейные и даже печеночные, что сопровождается пульсацией соответствующих сосудов. При недостаточности трикуспидального клапана основная нагрузка падает на значительно менее мощный правый желудочек, и у больных быстро развиваются нарушения кровообращения в большом круге. Характерным является раннее появление цианоза и одышки. Явления застоя в малом круге кровообращения выражены слабо. Так же как и при стенозе правого венозного отверстия, при недостаточности трехстворчатого клапана в сосудах малого круга практически не удается обнаружить гипертензии. Как правило, при данном пороке наблюдается экстрасистолия, часто-мерцательная аритмия, в ряде случаев развивается блокада правой ножки пучка Гисса.
Стеноз устья аорты При стенозе устья аорты нарушается отток крови из левого желудочка в аорту. Стеноз устья аорты прогрессирует медленно. Благодаря значительным компенсаторным возможностям миокарда левого желудочка нарушения гемодинамики наблюдаются только при резком (на 60-70%) сужении выходного отверстия. Обычно площадь выходного отверстия составляет 3 кв. см. При пороке она может уменьшиться до 0,5 кв. см. Минутный объем при компенсированном аортальном стенозе не меняется, при тяжелой степени сужения устья аорты МО уменьшается и не возрастает при физической нагрузке. Систолическое давление обычно понижается, диастолическое не меняется, или слегка превышает нормальное. Для поддержания нормального систолического давления левый желудочек должен производить значительно большую работу, но внешняя работа при этом даже уменьшается. В начальных стадиях аортального стеноза гиперфункция левого желудочка может развиваться без предшествующей дилятации. В дальнейшем усиление сердечных сокращений осуществляется за счет гипертрофии левого желудочка, вызванной дилятацией и удлинением мышечных волокон. При стенозе устья аорты резко увеличивается период изометрического сокращения, удлиняется период изгнания. Относительная скорость повышения давления в период изометрического сокращения и в период изгнания увеличивается в несколько раз. Коронарный кровоток снижен, особенно во время систолы, что объясняется влиянием высокого внутрижелудочкового давления и увеличением сопротивления коронарному кровотоку. Основной причиной коронарной недостаточности при аортальном стенозе считается возникновение диспропорции между повышенной потребностью в питании гипертрофированной мышцы и относительно пониженным ее кровоснабжением. Дополнительным фактором является замедленное наполнение аорты и снижение систолического и среднего давления в ней. Длительная нагрузка и усиливающаяся коронарная недостаточность приводят к уменьшению сократительной способности миокарда и развитию левожелудочковой недостаточности. Количество «достаточной» крови увеличивается и наступает предел возможного диастолического расширения левого желудочка. Повышается давление в левом предсердии с последующим его расширением, возникает относительная недостаточность митрального клапана, так называемая («митрализация» порока), застой в малом круге, затем в большом круге кровообращения. Ослабление левого желудочка приводит к развитию тотальной сердечной недостаточности. Появляется одышка сначала при физическом напряжении, а затем и в покое, головокружения, обмороки; последние могут быть следствием полной атриовентрикулярной блокады. Смерть наступает в результате фибрилляции или резкого учащения сердечных сокращений, предшествующих опорожнению левого желудочка. Таким образом, несмотря на то, что в компенсации данного порока принимает участие такой мощный сократительный элемент миокарда, как левый желудочек, компенсаторные возможности его не беспредельны.
Недостаточность аортальных клапанов Если в этиологии всех разобранных пороков сердца ведущую роль играли поражения эндокарда вследствие ревматического процесса, то возникновение недостаточности аортальных клапанов чаще всего связано с сифилитическим мезоаортитом. Гемодинамические нарушения при аортальной недостаточности определяются отсутствием препятствия на пути обратного тока крови во время диастолы левого желудочка. Объем возвращающейся в полость левого желудочка крови зависит от размеров дефекта клапана, продолжительности диастолы, разности давлений в аорте и желудочке во время диастолы. Обратный ток крови может составлять 60% от исходного. Обратный ток крови и уменьшение периферического сопротивления при недостаточности аортальных клапанов приводит к уменьшению диастолического давления, что сопровождается снижением коронарного кровотока, нарушением питания сердечной мышцы и снижением ее сократительной способности. Чтобы обеспечить нормальный минутный объем в условиях обратного возврата крови в левый желудочек, сердце вынуждено работать с повышенной нагрузкой. Усиление сокращений левого желудочка способствует увеличению диастолического наполнения и растяжению мышечных волокон желудочка. Систолическое давление увеличивается и достигает максимума значительно раньше, чем в норме. Связанное с увеличением систолического выброса повышение систолического давления с одной стороны, и уменьшение диастолического давления с другой стороны, способствует росту пульсового давления в аорте. Большая часть крови изгоняется левым желудочком в начале систолы, меньшая - во втором периоде фазы изгнания, поэтому в аорте давление достигает максимума очень рано, и его падение начинается тогда, когда систола еще не прекратилась. Общая работа желудочка превышает внешнюю, полезную, так как помимо работы по изгнанию эффективного ударного объема, левый желудочек производит работу по изгнанию возвращающейся при каждой диастоле крови. Благодаря большим компенсаторным возможностям левого желудочка порок в течение длительного времени остается компенсированным и только высокое пульсовое давление заставляет предположить наличие аортальной недостаточности. Постепенно развивается дилятация левого желудочка, повышается диастолическое давление в малом круге кровообращения, клиническими проявлениями которого являются приступы сердечной астмы и отек легких.
Общие механизмы компенсации при пороках сердца В условиях целого организма приспособительное усиление сократительной деятельности сердца может осуществляться двумя физиологическими способами - более совершенным - усилением систолы и опорожнением полостей сердца без предшествующего увеличения диастолического объема, и менее совершенным - усилением систолы при увеличении диастолического объема вследствие повышения степени растяжения волокон миокарда во время диастолы. Тотальное напряжение сердца зависит от внутриполостного давления в форме, определяемой геометрическими особенностями полости; для сферы, как известно, действителен закон Лапласа:
где Т – напряженность стенки замкнутой полости, Р – давление внутри полости, r – радиус, h – толщина стенки. Эта формула в принципе отражает сравнительно простую зависимость между напряжением (Т), давлением (Р) и радиусом левого желудочка (r). Если во время сокращения протяженность внутриполостной поверхности уменьшается быстрее, чем повышается давление, то напряжение снижается. В расширенном желудочке, в котором ударный объем составляет лишь сравнительно небольшую часть диастолического объема, а изменение радиуса при систоле невелико, напряжение во время последней может возрасти. Из этого следует, что для одного и того же увеличения ударного объема расширенный желудочек расходует большую энергию, поскольку индекс «время-напряжение» увеличен. При этом возрастает энергетическая «стоимость» работы, и количество энергии, необходимой для увеличения выполняемой работы, может быть необычайно большим. По существу Старлинг анализировал вариабельность «радиуса» в принципе Лапласа: диастолический объем наполнения идентичен с изометрическим конечным объемом и, следовательно, является тем фактором, который лежит в основе зависимости между начальным систолическим давлением и начальным напряжением стенки. Фактически числовое соотношение между напряжением стенки и давлением в полости определяется геометрической формой сокращающейся камеры, которая варьирует при различных кардиопатиях. Вместе с тем в соответствии с законом Лапласа расширение полостей представляет дополнительную нагрузку для сокращающегося волокна, нагрузку, которую может выполнить лишь волокно с сохраненными функциональными свойствами. При всех видах компенсированной недостаточности клапанов сущность гиперфункции состоит в том, что соответствующий желудочек во время систолы выбрасывает больше крови, чем в норме. Это увеличение касается как количества крови, поступающего в сосудистое русло (ударный объем), так и объема крови, возвращающегося во время диастолы через поврежденные клапаны в желудочек (объем возвращающейся крови). Особенностью сердечного цикла в этих условиях является отсутствие повышения внутрижелудочкового давления и этапа напряженного миокарда, так как разрушенные клапаны не позволяют обеспечить герметизацию полостей сердца. В то же время при компенсированных стенозах всех отверстий сущность гиперфункции заключается в том, что из соответствующей полости сердца во время систолы через суженное отверстие выбрасывается нормальное количество крови за счет увеличения внутрижелудочкового или внутрипредсердного давления. Известны два основных типа мышечного сокращения: 1. Мышца сокращается таким образом, что длина ее уменьшается, поперечный диаметр увеличивается, но напряжение мышечных волокон не изменяется. Такое сокращение называется изотоническим. 2. Сокращение мышцы не связано с изменением ее длины (укорочением), развивается лишь та или иная степень напряжения. Такой тип сокращения называется изометрическим. Гиперфункция при недостаточности клапанов сопровождается увеличением амплитуды сердечных сокращений без изменений напряжения, то есть протекает по изотоническому типу, при стенозах - увеличением напряжения без изменений амплитуды сокращений, то есть по изометрическому типу. Длительность гиперфункции (или компенсации порока) будет зависеть от снабжения энергией миокарда при его длительном функционировании в особых (неадекватных) условиях. Так как процессы мышечного сокращения термодинамически обратимы, энергия, затраченная на сокращение мышечных волокон во время систолы, должна быть восполнена во время диастолы, иначе следующее сокращение по своей энергетической характеристике окажется значительно менее эффективным. Восполнению энергии способствует преобразование в процессе мышечного сокращения химической энергии в механическую. Носителем химической энергии, как известно, является АТФ, образующийся в процессе окислительного фосфорилирования. Существуют дополнительные источники образования АТФ. Как показали Эббот и Оберт, мышца при укорочении способна не только преобразовывать химическую энергию в работу, но обратимо превращать работу в химическую энергию в том случае, если эта работа производится вн
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 226; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.77.122 (0.018 с.) |



 ,
,


