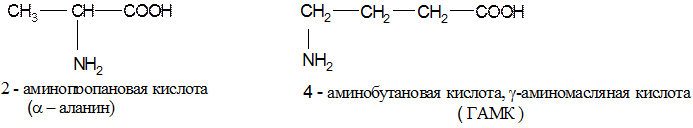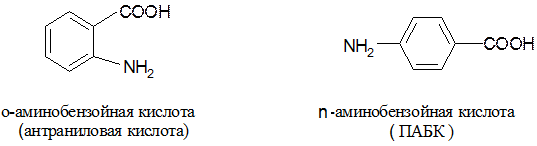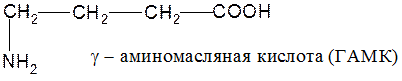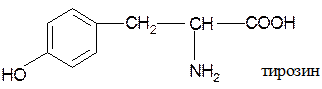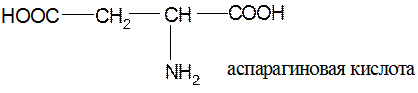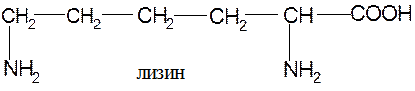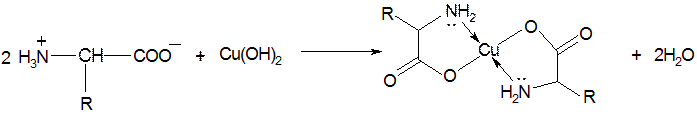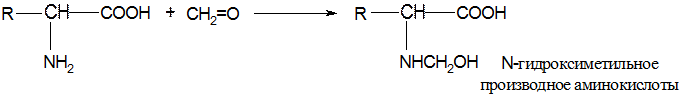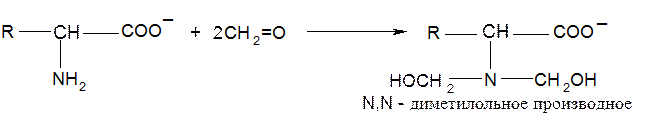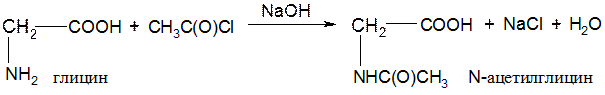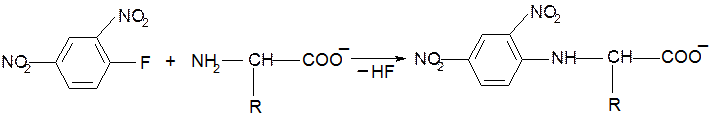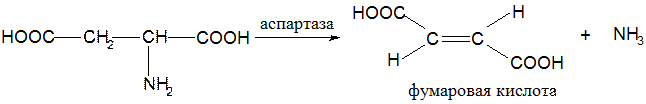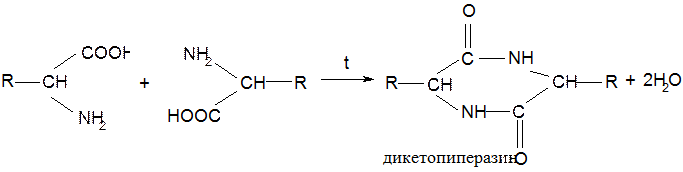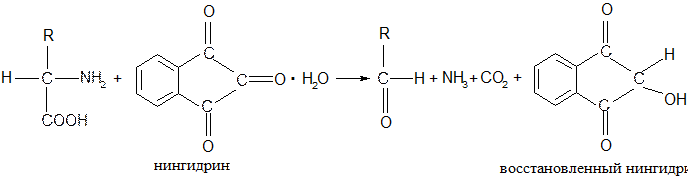Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Алифатические (наиболее распространены и значимыСодержание книги
Поиск на нашем сайте α-аминокислоты)
Ароматические
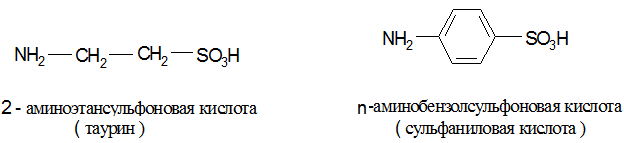
Аминосульфоновые кислоты
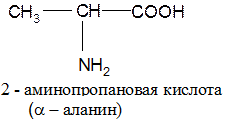
1. В зависимости от взаимного расположения групп NH2 и СООН аминокислоты классифицируют на α, β, γ, δ, ε, ω и т.д. 2. (наиболее распространены и значимы α-аминокислоты).
По количеству NH2 и СООН аминокислоты можно разделить на Нейтральные
Кислые
Основные
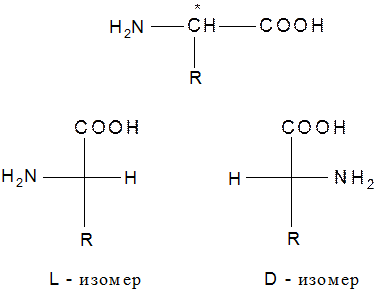
Все алифатические α – аминокислоты (кроме глицина) содержат хиральный атом углерода и могут существовать в виде стереоизомеров (энантиомеров и диастереомеров).
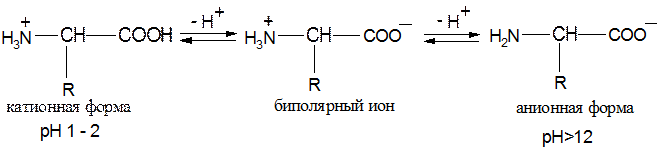
Большинство природных α – аминокислот относятся к L-ряду. D – аминокислоты встречаются в составе белков микроорганизмов и некоторых антибиотиков пептидной природы (грамицидин С). α – Аминокислоты являются амфолитами; в кристаллическом состоянии и в среде, близкой к нейтральной, существуют в виде внутренней соли – биполярного иона (цвиттер – ион):
Изоэлектрическая точка рI – это значение рН, при котором концентрация биполярного иона максимальна, а минимальные концентрации катионной и анионной форм равны между собой: рI = ½ (рКа(СООН) + рКа(NH3+)) Алифатические аминокислоты: рI =6,0 (слабокислая среда) Аминокислоты с слабокислотными функциональными группами (ОН – группа серина, треонина, тирозина и SН – группа цистеина): рI =5,0 – 5,7 Аминокислоты с дополнительной карбоксильной группой (аспарагиновая и глутаминовая кислоты): рI = 3,0 Аминокислоты с дополнительной амино- группой (лизин, аргинин) рI = 9,6 – 10,8 ХИМИЧЕСКИЕ СВОЙСТВА 1. Кислотно- основные (аминокислоты амфотерны):
2. Образование комплексных солей (наиболее устойчивы комплексы с ионами Сu2+, Ni2+, Zn2+). С гидроксидом меди (II) образуется хелатный комплекс синего цвета (используется для выделения и очистки аминокислот):
Реакции по аминогруппе. ● дезаминирование азотистой кислотой (метод определения аминокислоты по объему выделившегося азота метод Ван - Слайка):
● реакция с формалином (используется при формольном титровании – метод Серенсена)
● реакция ацилирования (способ защиты аминогруппы):
● ацилирование аминокислотами аммиака:
●алкилирование (2,4-динитрофторбензол – реактив Сэнджера)
●дезаминирование аминокислот - неокислительное
- окислительное (в присутствии оксидаз и НАД+)
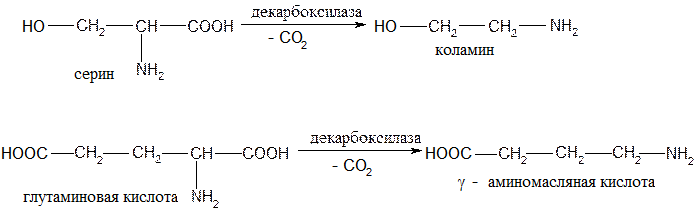
Реакции по карбоксильной группе ●декарбоксилирование
5. Трансаминирование – основной путь биосинтеза α-аминокислот
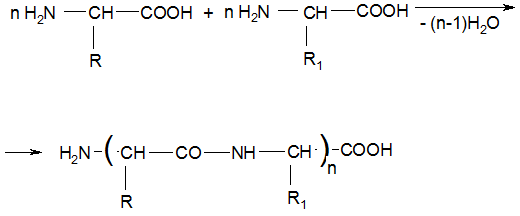
6. Реакции с одновременным участием NH2- и СООН – групп ● дегидратация α-аминокислот
● дегидратация γ- и δ-аминокислот
● нингидриновая реакция
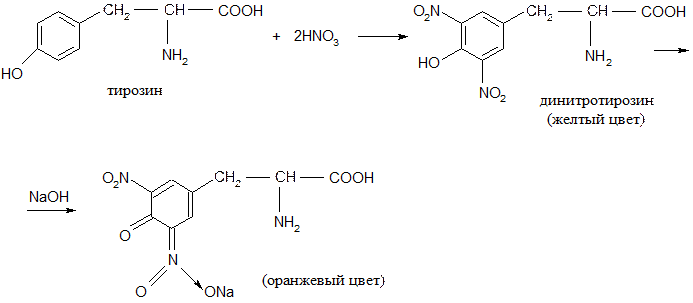
● ксантопротеиновая реакция
ПЕПТИДЫ - это природные или синтетические соединения, молекулы которых построены из остатков α – аминокислот (до 100), соединенных Пептидной связью.
КЛАССИФИКАЦИЯ:
|
||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 309; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.89 (0.007 с.) |