Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Скорость реакции и равновесие
Пусть есть обратимая реакция A + B Равновесными бывают не только химические реакции между газами или растворами, но и процессы растворения металлов, осадков. Например, твердое вещество быстрее всего растворяется, если его поместить в чистый растворитель, когда система далека от равновесия, в данном случае – от насыщенного раствора. Постепенно скорость растворения снижается, и одновременно увеличивается скорость обратного процесса – перехода вещества из раствора в кристаллический осадок. Когда раствор становится насыщенным, система достигает состояния равновесия, при этом скорости растворения и кристаллизации равны, а масса осадка со временем не меняется.
Рис.7.10. Константа равновесия. Важнейший параметр, характеризующий обратимую химическую реакцию – константа равновесия К. Если записать для рассмотренной обратимой реакции A + D
K = [NH3]2 равн/[H2]3равн[N2]равн. Для газообразных соединений вместо концентраций при записи константы равновесия можно использовать давление; очевидно, численное значение константы при этом может измениться, если число газообразных молекул в правой и левой частях уравнения не одинаковы. Значение K может служить характеристикой необратимости реакции в данных условиях. Так, если K очень велика, это значит, что концентрации продуктов реакции намного превышают концентрации исходных веществ при равновесии, т.е. реакция прошла почти до конца. Например, для реакции NiO + H2 = Ni + H2O при 523 К (250° С) К = [Н2О]равн/[Н2]равн = 800 (концентрации твердых веществ постоянны и в выражение для К не входят). Следовательно, в замкнутом объеме после достижения равновесия концентрация паров воды будет в 800 раз больше, чем водорода (здесь концентрации можно заменить пропорциональными им давлениями). Итак, эта реакция при указанной температуре проходит почти до конца. А вот для реакции WO2 + 2H2 =W + 2H2O при той же температуре К = ([Н2]равн/[Н2О]равн)2 = 10–27, следовательно, диоксид вольфрама практически не восстанавливается водородом при 500 К. Условная запись [X] означает, что равновесная концентрация вещества X выражена в единицах моль/л. В общем случае константа равновесия Кс должна быть выражена через активности реагирующих веществ. Для идеальных растворов коэффициенты активности равны единице, и активности будут равны молярным концентрациям. Введение в систему, в которой протекает обратимая реакция, катализатора приведет к снижению энергии активации как прямой, так и обратной реакции на одну и ту же величину. Это означает, что катализатор в равной мере ускоряет обе реакции. Таким образом, для обратимых реакций роль катализатора заключается только в более быстром достижении равновесия. Катализатор не приводит к смещению химического равновесия.
Необходимым признаком химического (термодинамического) равновесия системы является неизменность её состояния во времени при заданных внешних условиях. Химическое равновесие носит динамический характер: какое количество исходных веществ вступает в реакцию, такое же образуется в результате обратной реакции. Достаточным доказательством существования химического равновесия является достижение его с обеих сторон, т.е. в результате протекания как прямого, так и обратного процессов. Химические равновесия чаще всего изучаются при постоянных давлении и температуре. Система стремится к минимуму свободной энергии, который наблюдается в состоянии равновесия. Константа равновесия считается величиной безразмерной.
|
||||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 252; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.136.170 (0.004 с.) |
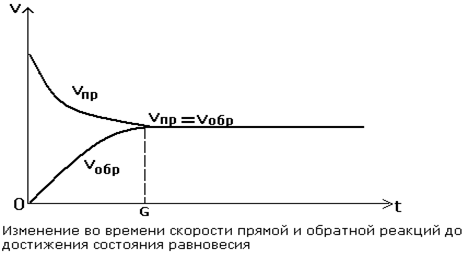
 C + D. Если предположить, что прямая и обратная реакция проходят в одну стадию, то скорости этих реакций будут прямо пропорциональны концентрациям реагентов: скорость прямой реакции v 1 = k 1[A][B], скорость обратной реакции v 2 = k 2[C][D] (квадратными скобками обозначены молярные концентрации реагентов). Видно, что по мере протекания прямой реакции концентрации исходных веществ А и В снижаются, соответственно, уменьшается и скорость прямой реакции. Скорость же обратной реакции, которая в начальный момент равна нулю (нет продуктов C и D), постепенно увеличивается. Рано или поздно наступит момент, когда скорости прямой и обратной реакций сравняются. После этого концентрации всех веществ – А, В, С и D не изменяются со временем. Это значит, что реакция достигла положения равновесия, а неизменяющиеся со временем концентрации веществ называются равновесными. Но, в отличие от механического равновесия, при котором всякое движение прекращается, при химическом равновесии обе реакции – и прямая, и обратная – продолжают идти, однако их скорости равны и поэтому кажется, что никаких изменений в системе не происходит (Рис. 7.10.).
C + D. Если предположить, что прямая и обратная реакция проходят в одну стадию, то скорости этих реакций будут прямо пропорциональны концентрациям реагентов: скорость прямой реакции v 1 = k 1[A][B], скорость обратной реакции v 2 = k 2[C][D] (квадратными скобками обозначены молярные концентрации реагентов). Видно, что по мере протекания прямой реакции концентрации исходных веществ А и В снижаются, соответственно, уменьшается и скорость прямой реакции. Скорость же обратной реакции, которая в начальный момент равна нулю (нет продуктов C и D), постепенно увеличивается. Рано или поздно наступит момент, когда скорости прямой и обратной реакций сравняются. После этого концентрации всех веществ – А, В, С и D не изменяются со временем. Это значит, что реакция достигла положения равновесия, а неизменяющиеся со временем концентрации веществ называются равновесными. Но, в отличие от механического равновесия, при котором всякое движение прекращается, при химическом равновесии обе реакции – и прямая, и обратная – продолжают идти, однако их скорости равны и поэтому кажется, что никаких изменений в системе не происходит (Рис. 7.10.).