
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Задачі до теми «пниктогени і їх сполуки»Содержание книги
Поиск на нашем сайте
1.На розчинення суміші фосфору та срібла витратили 256 мл розчину нітратної кислоти (ρ = 1,03 г/мл) з масовою часткою кислоти 5,5 %. Виділилось 4,1 л (н. у.) газу. Визначте масу фосфору у вихідній суміші. 2. Газ, одержаний під час каталітичного окиснення 20 л амоніаку (н. у.) повністю окиснили киснем повітря. Продукт реакції розчинили у воді, маса якої становила 3,24 кг, за наявності кисню. Визначте масову частку (%) розчиненої речовини в одержаному розчині. 3.Яку масу фосфор(У) оксиду розчинили в 300 мл розчину фосфатної кислоти з масовою часткою розчиненої речовини 85% і густиною 1,7 г/мл, якщо масова частка кислоти зросла на 7%? 4. Срібло, маса якого становила 21,6 г, розчинили в концентрованій нітратній кислоті. Газ, що виділився, пропустили через 200 мл розчину калій гідроксиду (концентрація 3 моль/л). Вкажіть сумарну масу солей, що утворились у розчині. 5. Суміш цинку й аргентум нітрату прожарили на повітрі. Маса суміші у результаті цього не змінилася. Визначте масову частку солі у суміші (%). Самостійна робота до змістового модуля 1.5. „Карбон і Силіцій та їх сполуки” Завдання 1. Вкажіть йони, які зумовлюють загальну твердість води: а) SO42-; б) Ca2+; в) Mg2+; г) Ca2+ і Mg2+; д) Al3+. 2. Виберіть правильне твердження. Карбон моно оксид … а) не горить; б) не виявляє відновних властивостей; в) не виявляє окисних властивостей; г) не взаємодіє з оксидами металів; д) не сполучається з хлором. 3. Виберіть правильне твердження. Силікатну кислоту добувають дією …. а) води на SiO2; б) хлоридної кислоти на розчин натрій силікату або калій силікату; в) лугу на розчин натрій силікату; г) хлоридної кислоти на силіцій (ІУ) оксид; д) калій хлориду на натрій силікат. 4. Вкажіть рівняння реакції, яка не є окисно-відновною: а) 2Mg + Si = Mg2Si; б) MgO + SiO2 = MgSiO3; в) Si + O2 = SiO2; г) Si + 2KOH + H2O = K2SiO3 + 2H2↑; д) 2CO + O2 = 2CO2. 5. Виберіть групу речовин, які реагують з карбон (ІУ) оксидом: а) Zn(OH)2, KOH, K2O; б) KOH, C, ZnO; в) Ca(OH)2, MgO, MgCl2; г) MgSiO3, SiO2, FeO; д) Al(OH)3, Ba(OH)2, BaO. 6. Визначте і вкажіть невідомі речовини у схемі перетворень Х1 Si ↑ H2SiO3: X2 а) X1 - SiO2; X2 – K2SiO3; б) X1 - K2SiO3; X2 – SiO2; в) X1 – SiH4; X2 – SiO2; г) X1 - MgSi; X2 - MgSiO3; д) X1 – MgSiO3; X2 – SiO2. 7. Установіть відповідність між реагентами і продуктами реакції. Реагенти Продукти реакції А. CO2(надл.) + Ca(OH)2 →; 1. Na2CO3 + NaCl + H2O. Б. CO2 + Ca(OH)2(надл.) →; 2. NaCl + CO2 + H2O. В. CaCO3 + CO2 + H2O →; 3. NaCl + CO2. Г. NaHCO3 + HCl →; 4. Ca(HCO3)2. Д. Na2CO3 + HCl →; 5. CaCO3 + H2O. 8. Установіть відповідність між реагентами і продуктами реакції. Реагенти Продукти реакції А. Магній силіцид + хлорид на кислота; 1. калій силіцид + водень. Б. Силіцій + калій гідроксид + вода; 2. силіцій тетрафорид + вода. В. Силіцій (ІУ) оксид + плавникова кислота; 3. силіцій карбід. Г. силіцій + вуглець; 4. магній хлорид + силан. Д. Силіцій (ІУ) оксид + калій оксид; 5. калій силікат + водень. 6. калій силікат.
ЗАДАЧІ до теми «Карбон і Силіцій та їх сполуки» 1. У результаті випалювання 270 кг вапняку маса твердого залишку виявилась на 100 кг меншою за вихідну масу вапняку. Обчисліть і вкажіть масову частку кальцій карбонату у вапняку (%): а) 80,3%; 6)83,2%; в) 84,2%; г) 82,4%; д) 85%. 2. Суміш кремнію і вуглецю, маса якої становить 100 г, помістили в а) 28%; 6)74%; в) 36%; г) 42%; д) 58%. 3..Суміш СО2 і СО, масові частки газів у якій однакові, за нормальних умов займає об'єм 4,032 л. Два літра (н. у.) цієї суміші пропустили крізь 20 г розчину натрій гідроксиду з масовою часткою лугу 28%. Яка сіль при цьому утворилась? Визначте її масу. 4. Прожарили суміш амоній карбонату та магній карбонату. Виявили 5. Після прожарювання суміші кальцій карбонату та магній карбонату
ЗМІСТОВНИЙ МОДУЛЬ 2. „ХІМІЯ МЕТАЛІВ”
Самостійна робота до змістового модуля 2.1. „Лужні та лужно-земельні метали” Завдання 1. Вкажіть основний промисловий спосіб добування натрію: а) електроліз розчину NaC; б) електроліз розплаву NaCl; в) електроліз розчину NaOH; г) електроліз розчину Na2SO4; д) електроліз розплаву Na2SO4. 2. Вкажіть електронну формулу йону Na+: а) 1s22s22p63s1; б) 1s22s22p6; в) 1s22s22p63s2; г) 1s22s22p4; д) 1s22s22p5; 3. Вкажіть схему реакції, що відповідає процесу, який відбувається на аноді під час електролізу розплаву кальцій хлориду: а) Ca+2 + 2e- → Ca0; б) 2Cl- - 2e- → Cl2; в) Cl- - 1e- → Cl0; г) 2Cl- - 2e- → Cl0; д) 2H2O – 4e- → O2 + 4H+. 4. Визначте і вкажіть формули речовин А і В у схемі перетворень Ca → A а) CaCl2, Ca(OH)2; б) CaO, Ca(OH)2; в) Ca3N2, CaO; г) CaC2, CaSO3; д) Ca3P2, CaO. 5. Позначте формули речовин, під час взаємодії яких можна одержати кальцій гідроксид: а) Ca3(PO4)2, NaOH; б) Ca(NO3)2, Al(OH)3; в) CaCl2, KOH; г) CaSO4, Zn(OH)2; д) CaCO3, NaOH. 6. Вкажіть формули пари сполук лужних металів, які під час нагрівання не розкладаються: а) KNO3, KOH; б) KOH, K2CO3; в) K2SO4, KHCO3; г) KHCO3, NaOH; д) Na2SO4, NaHCO3. 7. Установіть відповідність між реагентами та продуктами реакцій. Реагенти Продукти реакцій А. Ca3P2 + H2O →; 1. CaO + H2. Б. CaO + H2O →; 2. Ca(OH)2 + H2. В. Ca + H2O →; 3. Ca(OH)2 + PH3. Г. CaH2 + H2O →; 4. Ca3(PO4)2. Д. Ca(OH)2 + P2O5; 5. Ca(OH)2. 6. Ca3(PO4)2+ H2O. 8. Установіть відповідність між типом реакції, яку потрібно провести та схемою перетворення.
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 473; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.28.160 (0.01 с.) |

 B
B 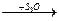 CaSO4
CaSO4


