
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Второе начало термодинамики. Энтропия. Эффекты переноса.Содержание книги
Поиск на нашем сайте
Коэффициент диффузии численно равен массе вещества, переносимого в единицу времени через единицу площади перпендикулярно направлению распространения при градиенте плотности равном единице. Коэффициент динамической вязкости численно равен силе внутреннего трения, действующий на единицу площади трущихся слоёв, при градиенте скорости равном 1. Коэффициент динамической вязкости
В системе СГС единицей измерения вязкости служит Пуаз (П). 1П=
Единица вязкости названа в честь знаменитого ученого Пуазейля
Второе начало термодинамики. Энтропия. Эффекты переноса. Второе начало термодинамики может быть сформулировано несколькими способами. В наиболее очевидной формулировке второе начало гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому. Более строго, невозможны такие процессы, единственным конечным результатом которых был бы переход тепла от тела, менее нагретого, к телу, более нагретому. Второе начало термодинамики может быть также сформулировано следующим образом: невозможны такие процессы, единственным конечным результатом которых явилось бы отнятие от некоторого тела определенного количества тепла и превращения этого тепла полностью в работу. Первое начало термодинамики, выражая закон сохранения энергии и превращения энергии, не позволяет установить направление протекания т/д процессов. Кроме того, можно представить множество процессов, не противоречащих I началу т/д, в которых энергия сохраняется, а в природе они не осуществляются. Возможные формулировки второго начало т/д: 1) закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимой процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает Δ S ≥ 0 (необратимый процесс) 2) Δ S ≥ 0 (S = 0 при обратимом и Δ S ≥ 0 при необратимом процессе) В процессах, происходящих в замкнутой системе, энтропия не убывает. 2) Из формулы Больцмана S= 3) По Кельвину: не возможен круговой процесс, единственным результатом которого является превращения теплоты, полученной от нагревателя в эквивалентную ей работу. 4) По Клаузиусу: не возможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Для описания т/д систем при 0 К используют теорему Нернста-Планка (третье начало т/д): энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к 0 К
Из теоремы Нернста-Планка следует, что C p = C v = 0 при 0 К Энтропия S – это отношение полученной или отданной теплоты к температуре, при которой происходил этот процесс:
где dQ- количество теплоты. T-температура системы. Энтропия является количественной мерой степени молекулярного беспорядка в системе. Сообщение системе тепла приводит к усилению теплового движения молекул и следовательно к увеличению степени беспорядка в системе. Чем выше температура (т.е. больше внутренняя энергия системы), тем относительно меньшей сказывается доля беспорядка, обусловленного сообщением данного количества тепла dQ. При температуре абсолютного нуля энтропия всякого вещества равна 0. (теорема Нериста) или третье начало термодинамики. Отсюда вытекает, что энтропия всякого тела стремится к нулю при стремлении к нулю температуры. lim T→0 Явлениями переноса называются необратимые процессы, в результате которых происходит пространственный перенос энергии, массы, количества движения. К явлениям переноса относятся: а) диффузия (перенос массы) б) теплопроводность (перенос энергии) в) внутреннее трение (перенос количества движения) а)Диффузия. Явления проникновения молекул одного вещества в межмолекулярное пространство другого (перемешивание вещества) называется диффузией. Перенос массы, выравнивается концентрация молекул. Описывается процесс диффузии уравнением Фика.
где ∆ M - переносимая масса;
∆S – площадь; ∆t- время; Д- коэффициент диффузии, зависящий от рода вещества, температуры, давления. Знак минус говорит о том, что масса переносится в сторону уменьшения убывания плотности.
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 226; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.236.144 (0.006 с.) |

 зависит от рода жидкости и от её температуры. С повышением температуры
зависит от рода жидкости и от её температуры. С повышением температуры 
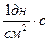
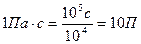
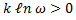 , следовательно, возрастание энтропии означает переход системы из менее вероятного состояния в более вероятное.
, следовательно, возрастание энтропии означает переход системы из менее вероятного состояния в более вероятное.
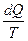

 (16)
(16) S- приращение энтропии.
S- приращение энтропии.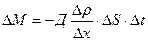 (17)
(17) градиент плотности;
градиент плотности;


