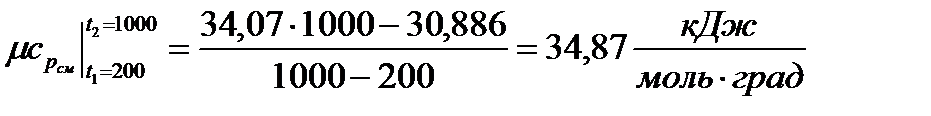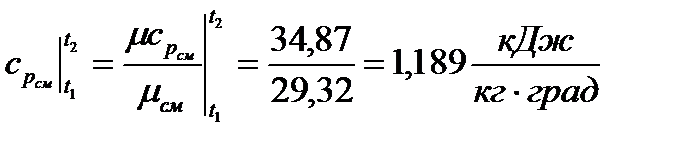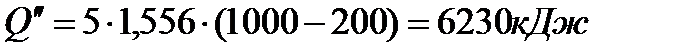Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
РАЗДЕЛ 3. Основы теории горения.Содержание книги Поиск на нашем сайте
ТЕМА 3.1. Основы термохимии. Понятие о процессе сгорания. Уравнения химических реакций горения. Теоретически необходимое количество кислорода, окислителя и воздуха. Коэффициент избытка окислителя и воздуха. Теплотворность. Определение теплотворности, количества тепла, топлива в ДВС и коэффициента избытка воздуха. Рассмотрите принцип образования тепла в авиационных двигателях за счет химической энергии горючего. Уясните основные этапы горения: скрытое горение; видимое горения. Четко усвойте уравнения химических реакций горения. Научитесь рассчитывать теоретически необходимое количество кислорода, окислителя и воздуха. Детально разберите понятия топлива, топливо-воздушной смеси, коэффициента избытка воздуха, теплотворности. Вопросы для самоконтроля: 1. Понятие о процессе сгорания. Основные периоды горения. 2. Дать определение фронта пламени. 3. Уравнения химических реакций горения. 4. Теоретически необходимое количество кислорода, окислителя и воздуха. 5. Коэффициент избытка окислителя и воздуха. 6. «Богатая» и «бедная» топливовоздушные смеси. 7. Дать определение теплотворности топлива. 8. Определениетеплотворности углеводородного топлива.
Требования к выполнению контрольной работы При выполнении контрольной работы необходимо придерживаться следующих правил: – к решению задач контрольного задания следует приступать только после изучения соответствующего раздела курса – задание составлено по вариантной системе. Номер варианта определяется кафедрой; – условия задач переписывать полностью; – в процессе решения сначала приводить формулы, затем подставлять в них соответствующие численные значения; размерность приводить только для результата вычисления; – вычисления проводить только в международной системе СИ; – решения иллюстрировать схемами и графиками (если требуется по условию); – оставить поля для замечаний рецензента и 1…2 чистыестраницы для работы над ошибками. – в тексте работы приводить ссылки на использованную литературу, а в конце контрольной работы – список использованной литературы. Контрольная работа подписывается студентом. Прием контрольных работ на рецензию прекращается за 10 дней до начала лабораторно-экзаменационной сессии.Работы, выполненные по чужому варианту, не рассматриваются.
Задание 1 Газовые смеси и теплоемкости Дано: Газовая смесь имеет следующий (1)* процентный состав (2); давление смеси (4) в барах, объем смеси (5), температура смеси (6) в °С.
Требуется определить: 1) (3) состав смеси; 2) газовые постоянные компонентов и смеси; 3) среднюю молекулярную массу смеси через объемные и массовые доли; 4) парциальные давления компонентов через объемные и массовые доли; 5) массу смеси и компонентов; 6) парциальные объемы и плотности компонентов; 7) плотность компонентов и смеси при заданных условиях через объемные и массовые доли; 8) плотности компонентов и смеси при нормальных условиях через объемные и массовые доли; 9) истинные мольную, объемную (для 1 м3) и массовую теплоемкости смеси при р = const и v = const для вышеуказанной температуры смеси; 10) средние мольную, объемную и массовую теплоемкости при р = const и v = const для интервала температур (7); 11) затрату тепла на нагревание (охлаждение) при р = const двух молей, 5 м3 и 7 кг смеси в вышеуказанном интервале температур. *Примечание: Данные (1), (2), (3) и т.д. взять из таблицы в соответствии с вариантом.
Таблица данных и ответов к контрольному заданию
Пример решения задания
Дано: 1. Смесь имеет следующий объемный состав:
2. Объем смеси Vсм= 3 м3 давление смеси р см= 1 бар (105 н/м2);. температура смеси t cм = 100°С (Тсм = 373К). 3. Температура, при которой определяется истинная теплоемкость смеси t = 2000°С (Т = 2273К). 4. Интервал температур, для которого определяется средняя теплоемкость смеси: t 1 = 200°С (Т 1 = 473К), t 2 = 1000°С (Т 2 = 1273К).
Решение. 1. Определение массового состава смеси:
Определение объемного состава смеси при известном массовом составе:
2. Определение газовых постоянных компонентов смеси:
3. Определение газовой постоянной смеси:
4. Определение средней молекулярной массы смеси: а) через объемные доли:
проверка:
б) через массовые доли:
5. Определение парциальных давлений компонентов: а) через объемные доли:
б) черезмассовые доли:
6. Определение массы смеси:
7. Определение массы компонентов:
8. Определение парциальных объемов компонентов:
9. Определение парциальной плотности компонентов (при pi и Т см):
10. Определение плотности компонентов при заданных условиях (при pi и Т см):
11. Определение плотности смеси при заданных условиях (при pсм и Т см): а) через объемные доли:
б) через массовые доли:
в) через парциальные плотности компонентов:
12. Определение плотности компонентов при нормальных физических условиях (при р = 760 мм рт. ст. = 1,013 бар и t = 0° С; Т = 273° К):
13. Определение плотности смеси при нормальных условиях: а) через объемные доли:
б) через массовые доли:
(Проверка 14. Определение истинных теплоемкостей смеси (при t = 2000°С): а) мольная:
б) объемная
в) массовая
15. Определение средних теплоемкостей смеси: а) мольная:
где
Средняя мольная теплоемкость при постоянном давлении в заданном интервале температур:
По закону Майера:
Средняя мольная теплоемкость при постоянном объеме в заданном интервале температур:
б) объемная
в) массовая
Примечание. Средние мольные теплоемкости берутся из таблиц для температур t 1 = 200° С и t 2 = 1000° С.
16. Определение затраты тепла на нагревание в процессе: а) двух молей смеси:
б) 5м3смеси:
в) 7кг смеси:
Приложения для выполнения контрольной работы: Таблица1.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 153; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.0.175 (0.01 с.) |

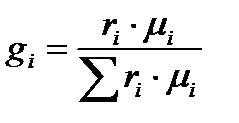
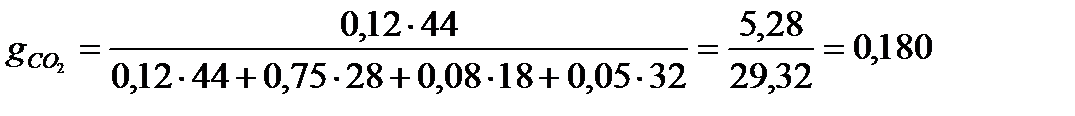 ;
; ;
;  ;
;  ;
;


 ;
;  ;
; ;
; 






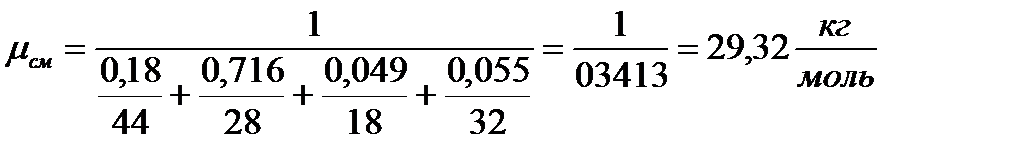





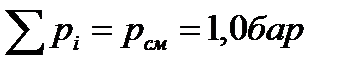











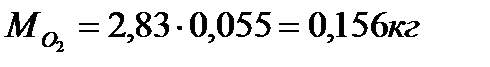

 (при р см и Т см)
(при р см и Т см)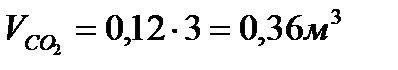






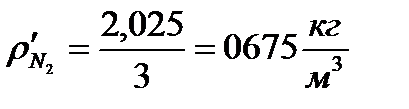

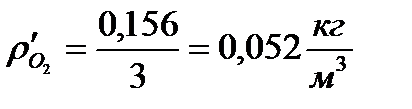













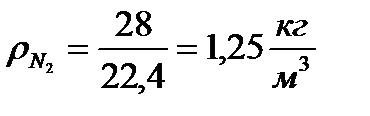





 )
)





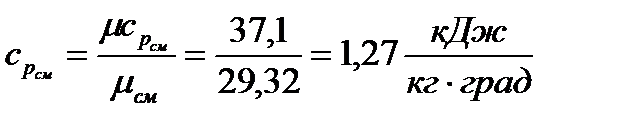

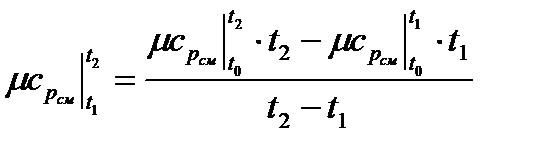
 ;
;