
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Температура плавления (замерзания) - температура, при которой давление насыщенного пара над твердой и жидкой фазами равны между собой.Содержание книги
Поиск на нашем сайте
При практическом измерении температуры плавления руководствуются следующим определением: "Под температурой плавления вещества подразумевается интервал температур между началом плавления - появлением первой капли жидкости и концом плавления - полным переходом вещества в жидкое состояние" (Государственная Фармакопея XI, т.1. М., "Медицина", 1987, с. 16.). Чистые вещества плавятся при постоянной температуре, значение которой определяется природой вещества. В присутствии примесей образцы плавятся в интервале температур. Измеряя температуру плавления можно идентифицировать вещество, установить степень его чистоты. По разнице в температурах плавления растворителя и раствора вещества в данном растворителе можно определить, например, молярную массу растворенного вещества. Измерение температуры плавления можно использовать и для других целей. При измерении температуры плавления смесей (в том числе растворов), плавящихся в интервале температур, определяют температуру конца плавления (исчезновения последнего кристалла), при измерении температуры замерзания смесей (растворов) определяют температуру начала замерзания (появления первого кристалла). Если температуру плавления измерять капиллярным методом, в котором исследуемое вещество находится в стеклянном капилляре, а ртутный резервуар термометра опущен в масляную баню, в момент полного плавления вещества в капилляре температуры бани и внутри капилляра могут не совпадать. Для точного определения температуры плавления в этом случае измеряют температуру исчезновения последнего кристалла при нагревании и температуру появления первого кристалла при охлаждении. Если эти температуры не совпадают (и разница не превышает 2 ОС), за температуру плавления принимают их среднее арифметическое значение. УСТРОЙСТВО УСТАНОВКИ ДЛЯ ОПРЕДЕЛЕНИЯ Установка состоит из масляной (парафиновой) бани; термометра; стеклянного капилляра, заполненного исследуемым веществом; плитки; подставки; штатива.
Операцию повторяют насколько раз, пока высота слоя вещества не будет равна 3 мм. Необходимо, чтобы столбик вещества в капилляре был плотным без видимых разрывов. Подготовленный таким образом капилляр с помощью резинового кольца укрепляют на термометре так, чтобы столбик вещества находился на уровне середины ртутного резервуара термометра, а резиновое кольцо при погружении термометра с капилляром в масляную баню не касалось масла. Термометр с капилляром закрепляют в лапке штатива и опускают в предварительно нагретую баню. При этом термометр не должен касаться дна и стенок бани, а уровень жидкости в бане должен быть выше резервуара термометра примерно на 5 мм. Масляную баню медленно нагревают со скоростью примерно 1,5 ОС в минуту. Отмечают температуру (t1), когда в капилляре исчезает последний кристаллик исследуемого вещества. Затем отключают плитку, заменяют ее на подставку, следя за тем, чтобы капилляр, закрепленный на термометре, не извлекался из масляной бани. Отмечают температуру (t2), когда в капилляре появится первый кристалл. Если разница в температурах t1 и t2 превышает 2 ОС, опыт следует повторить, уменьшая скорость нагревания и охлаждения. Температуру плавления рассчитывают по формуле:
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ ПО ТЕМЕ: "ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ КАПИЛЛЯРНЫМ МЕТОДОМ". 1. Физико-химическое определение понятия "температура плавления" (замерзания). 2. Определение понятия "температура плавления" по Фармакопее. 3. Какую температуру принимают за температуру плавления для смеси веществ, которая может плавиться в широком интервале температур? 4. Какие (какая) величины измеряются непосредственно в опыте при определении температуры плавления капиллярным методом? 5. Почему при измерении температуры плавления капиллярным методом в опыте определяют две величины: температуру исчезновения последнего кристалла при нагревании и температуру появления первого кристалла при охлаждении? 6. Какая из двух температур: температура исчезновения последнего кристалла при нагревании t1 или температура появления первого кристалла при охлаждении t2 может быть выше? Почему? 7. Если температура исчезновения последнего кристалла при нагревании t1 и температура появления первого кристалла при охлаждение t2 не одинаковы, токакаяразница в значениях этих температур допустима? 8. Если при измерении температуры плавления капиллярным методом, t1 и t2 отличаются между собой более чем на 2 (4) градуса, как добиться допустимой разницы температур? 9. Если в капилляре последний кристалл при нагревании исчезает при температуре t1, а первый кристалл при охлаждении появляется при температуре t2 (t1 10. Состав установки для определения температуры плавления капиллярным методом. 11. Размеры капилляра. 12. Заполнение капилляра веществом. Требования к заполнению. 13. Почему при заполнении капилляра веществом следует следить за тем, чтобы столбик вещества был плотным без видимых разрывов? Как это достигается? 14. Если при расплавлении вещества в капилляре появился пузырек воздуха, как от него освободиться? 15. Требования к закреплению капилляра на термометре. 16. Требования к закреплению термометра с капилляром при погружении их в масляную баню. 17. Основные этапы определения температуры плавления капиллярным методом. 18. С какой скоростью следует нагревать масляную баню? 19. Какое требование следует соблюдать при перенесении масляной бани с термометром и капилляром с плитки на подставку? 20. Практическое значение измерения температуры плавления. 2. "Экстрагирование иода из водного раствора органическим растворителем" (Практический навык). Экстрагирование – процесс извлечения вещества, растворенного в одном растворителе, другим растворителем (экстрагентом), который не смешивается с первым и лучше растворяет извлекаемое вещество. Экстрагирование можно использовать для: 1) выделения вещества из смеси; 2) очистки раствора вещества от примесей; 3) разделения смеси на компоненты. Экстрагирование основано на законе распределения Нернста, согласно которому, если экстрагируемое вещество обладает одинаковой величиной частиц в обоих растворителях и не вступает с ними в химическое взаимодействие:
где
К – коэффициент распределения.
Используя закон распределения, можно рассчитать массу вещества, оставшегося после однократной экстракции в первом растворителе (m1) и перешедшего в экстрагент m0 – масса извлекаемого вещества в исходном растворе; V1 – объем исходного раствора; V2 - объем экстрагента; К - коэффициент распределения.
|
||||
|
Последнее изменение этой страницы: 2016-12-09; просмотров: 365; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.231.97 (0.009 с.) |

 Исследуемое вещество помещают в капилляр диаметром 1 мм и длиной 6 см, запаянный с одного конца. Заполнение капилляра веществом проводят так: небольшое количество хорошо измельченного вещества помещают на чистую поверхность и, прикасаясь открытым концом капилляра к веществу, вводят его в капилляр небольшими порциями. Затем перемещают вещество к запаянному концу, постукивая этим концом по твердой поверхности, либо бросая капилляр запаянным концом вниз в вертикально расположенную стеклянную трубку высотой не менее 50 см.
Исследуемое вещество помещают в капилляр диаметром 1 мм и длиной 6 см, запаянный с одного конца. Заполнение капилляра веществом проводят так: небольшое количество хорошо измельченного вещества помещают на чистую поверхность и, прикасаясь открытым концом капилляра к веществу, вводят его в капилляр небольшими порциями. Затем перемещают вещество к запаянному концу, постукивая этим концом по твердой поверхности, либо бросая капилляр запаянным концом вниз в вертикально расположенную стеклянную трубку высотой не менее 50 см.
 t2), то как по этим двум температурам следует определить tпл?
t2), то как по этим двум температурам следует определить tпл?
 – концентрация извлекаемого вещества в экстракте;
– концентрация извлекаемого вещества в экстракте; – концентрация извлекаемого вещества в рафинате;
– концентрация извлекаемого вещества в рафинате; по формулам:
по формулам: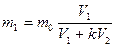 ;
;  , где
, где


