
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Фотоколориметричне визначення фенолу в повітрі ( метод з діазотованим паранітроаніліном)Содержание книги
Поиск на нашем сайте
ТЕОРЕТИЧНА ЧАСТИНА 1.1
Особливість фізико-хімічних методів аналізу полягає в тому, що перебіг використаної для аналізу хімічної реакції контролюють за зміною будь-якої фізичної властивості. Взагалі, фізико-хімічні методи аналізу класифікують за типом фізико-хімічних явищ, що лежать в їх основі [8]. Оптичні методи аналізу грунтуються на вимірюванні оптичних властивостей аналізованого середовища (інтенсивності забарвлення, оптичної густини, коефіцієнта заломлення, спектральних характеристик і ін.). Електрохімічні методи аналізу - сукупність методів якісного та кількісного аналізу речовин, що ґрунтуються на процесах, які протікають на електродах або у міжелектродному просторі. Хроматографічні методи є ефективними методами розділення і аналізу складних за складом газоподібних і рідких сумішей [6] Фотоколориметричне визначення фенолу в повітрі (метод з діазотованим паранітроаніліном) Фотоколориметрія – це метод кількісного аналізу, ґрунтується на вимірюванні ступеня поглинання або пропускання немонохроматичного світла речовиною, яку визначають. У фотоколориметрії вимірювання інтенсивності світлових потоків проводять за допомогою фотоелементів. Фотоелементи – прилади, що перетворюють світлову енергію в електричний струм. Зміна інтенсивності світлового потоку викликає зміну електричного струму виробленого фотоелементом. Фотоколориметричні методи – це кількісне визначення концентрації речовини з поглинання світла у видимій та ближній ультрафіолетовій області спектра. Поглинання світла вимірюють на фотоелектричних колориметрах (КФК-2, КФК-3, ФЕК-56М та інших) [14]. Принцип методу. Метод ґрунтується на взаємодії фенолу і діазотованого паранітроаніліну з утворенням сполуки, забарвленої в червоний колір, також на поглинанні фенолу з повітря розчином карбонату натрію, витяганні фенолу з отриманого розчину бутилацетатом і вимірюванні масової концентрації. Для визначення використовують прилад колориметр фотоелектричний концентраційний КФК-2 (рис.1.1) [7]. Визначення фенолу в повітрі методом газової хроматографії Хроматографічні методи – це фізико-хімічні методи розділення компонентів складних сумішей газів, парів, рідин або розчинених речовин, який ґрунтується на використанні сорбційних процесів в динамічних умовах. Хроматографія – це високоефективний фізико-хімічний метод розділення і аналізу, в якому речовина розподіляється між двома фазами:
рухомою і нерухомою. Хроматографічні методи класифікують за такими ознаками:- за агрегатним станом суміші, в якій проводять її розділення на компоненти – газова, рідинна і газорідинна хроматографія;- за механізмом розділення – адсорбційна, розподільча, йонообмінна, осадова, окисно-відновна, адсорбційно-комплексоутворююча хроматографія; - за формою проведення хроматографічного процесу – колоночна, капілярна, площинна (паперова, тонкошарова і мембранна) [3]. Серед хроматографічних методів для визначення фенолу застосовується газова хроматографія Газова хроматографія – це різновид хроматографії, метод поділу летких компонентів, при якому рухомою фазою служить інертний газ (газ-носій), що протікає через нерухому фазу з великою поверхнею.
За допомогою газової хроматографії можливе визначення в повітрі і таких висококиплячих забруднювачів, як феноли і їх похідні [4]. Чутливість визначення не нижче 10-4 % в аналізованому об'ємі розчину. Визначення грунтується на поглинанні твердих частинок або пари фенолів розчином лугу у вигляді фенолятів, а потім гідролізуються кислотою і відганяються з водяними парами, і водний розчин фенолів аналізують методом газової хроматографії. Ступінь визначення фенолів з лужного розчину складає 88-95 % [4].
Рис. 1.5 Газовий хроматограф 3380
Рис. 1.6 Оптична схема газового хроматографа 3380 1 – джерело газу-носія (рухомої фази); 2 – регулятор витрати газу носія; 3 – пристрій
підсилювач; 7 – реєструючий прилад; 8 – витратомір
Опис вибраного методу (метод з діазотованим паранітроаналіном) Реактиви і розчини 1. Вуглекислий натрій. 2. Соляна кислота, 4%-ий розчин. Готують додаванням 9,1 мл концентрованої соляної кислоти до 89,2 мл води. 3. Поглинальний розчин, 0,8%-ий розчин вуглекислого натрію. Термін зберігання розчину 6 місяців. 4. Натрій азотнокислий, 25%-ий розчин. 10 г азотнокислого натрію розчиняють в 30 мл води. 5. Паранітроанілін, 0,1%-ий розчин. Наважку 0,100 г паранітроаніліну, попередньо висушеного при температурі 60°С протягом 2 годин, розчиняють в 100 мл 4%-вої НСl і охолоджують до 0 - 5°С. 6. Діазотований паранітроанілін. Перед роботою до 12,5 мл охолодженого паранітроаніліну доливають 2,5 мл розчину азотнокислого натрію і через 2 хв доводять об’єм до 50 мл водою. Розчин може зберігатися не більше 3 днів в холодильнику. 7. Вихідний стандартний розчин. В мірну колбу на 100 мл вливають 20 мл поглинального розчину, колбу зважують на аналітичних вагах, вливають 30 – 50 мг безкольорового свіжоперегнаного фенолу і знову зважують. Після цього доводять об’єм рідини в колбі до мітки поглинальним розчином. За різницею зважування знаходять вміст фенолу в 1 мл розчину. 8. Робочий стандартний розчин з вмістом фенолу 10 мкг/мл. Готують розведенням вихідного розчину поглинаючим розчином. Розчин використовують свіжоприготовлений
Відбір проб Для визначення разової концентрації фенолу досліджуване повітря протягують через поглинальний пристрій Ріхтера, який містить 6 мл поглинального розчину, зі швидкістю 3 л/хв. Протягом 20 хв. Термін збереження відібраних проб не довше 12 годин. Хід аналізу Рівень розчину в поглинальному пристрої доводять до 6 мл дистильованою водою. Для аналізу 5 мл проби поміщають в пробірку, добавляють 0,4 мл діазотованого паранітроаніліну, вміст пробірки ретельно струшують і вимірюють оптичну густину розчину в кюветах шириною 10 мм при при довжині хвилі 494 нм відносно води. Час, від додавання останнього реактиву до вимірювання оптичної густини проби, повинен бути однаковим. Одночасно проводять вимірювання оптичної щільності нульової проби, для чого 5 м л поглинаючого розчину аналізують аналогічно пробам. Величина оптичної щільності нульового розчину повинна бути не більше 0,010. У тому випадку, якщо вона перевищує це значення, необхідно перевірити якість приготованих реактивів, чистоту посуду і вимірювальних кювет. Кількість фенолу в пробі визначають за допомогою калібрувального графіка по різних вимірах оптичної щільності розчинів проби і нульового.
Для побудови калібрувального графіку готують серію стандартних розчинів в мірних колбах ємкістю 100 мл Розчини для приготування шкали стандартів при визначенні фенолу
Розрахункова частина
1. Середнє арифметичне значення:
де
Х= 2. Абсолютна похибка визначення:
де ∆ х1 = 0,0032 – 0,0034 = - 0,0002 мг/м3 ∆ х2 = 0,0034 – 0,0034 = 0 мг/м3 ∆ х3 = 0,0030 – 0,0034 = - 0,0004 мг/м3
Середнє значення абсолютної похибки всієї серії
3. Стандартне відхилення окремого визначення (S) S =
S = 4. Стандартне відхилення середнього арифметичного Sх Sx =
S = 5. Інтервал довірчих значень
де
S
Значення коефіцієнта Стьюдента
Таким чином, істинне значення вимірюваної величини знаходиться в довірчому інтервалі:
За результатами розрахунків метрологічних характеристик створюємо ілюстрації до відповідних розрахунків (рис. 2.1 і рис.2.2)
Рис. 2.1 Графік концентрацій фенолу в повітрі
Рис. 2.2 Графік абсолютних похибок визначення фенолу у повітрі
Курсова робота виконана за темою “Визначення фенолу у повітрі фізико-хімічними методами аналізу”. В процесі курсової розглянули фізико-хімічні методи аналізу визначення фенолу, зроблена порівняльна таблиця методів, а також вивченні правила техніки безпеки при проведенні аналізів. За основний метод вибрано фотоколориметричний метод з діазотованим паранітроаніліном. Проведена статистична обробка даних. Концентрація фенолу в повітрі становить
1. Білецький В. С. Мала гірнича енциклопедія 1987 – 156ст. 2. Лестус Л. В. Методи вимірювання параметрів навколишнього середовища. Миргород – МХПК ПолтНТУ, 2013 3. Алесковского В. Б. Физико-химические методы анализа 1983- 365 с. 4. Афанасьев Ю.А., Фомин С.А. Мониторинг и методы контроля окружающей среды. Учебное пособие. Часть 2. – М.: МНЭПУ, 2001 – 337 с. 5. Бабко А.К., Пятницкий И.В. Количественный анализ. – М.: Высшая школа, 1962 – 510 с. 6. Беккер А.А., Агаев Т.Б. Охрана и контроль загрязнения природной среды. – Л.: Гидрометеоиздат.ю 1989 – 286 с. 7. Берленд М. Е., Сидоренко Г. И. Руководство по контролю загрязнения атмосферы. Ленинград Гидрометиоиздат 1979 - 8. Быховская М.С., Гинзбург С.Л., Хализова О.Д. Методы определения вредных веществ в воздухе и других середах. Часть 2. – М.: Медгиз, 1960 – 316 с. 9. Крешков А.П. Основы аналитической химии. Физико-химические (инструментальные) методы анализа. – М.: Химия, 1970 – 472 с. 10. Лейте В. Определение загрязнений воздуха в атмосфере и на робочем месте. Ленинград “Химия”Ленинградское отделение 1980 – 340 с. 11. Паспорт КФК – 2. Руководство по эксплуатации 12. Перегуд Е. А., Горелик Д. О. Инструментальные методы контроля загрязнения атмосферы. – Л.: Химия, 1981- 381 с. 13. Пешкова В.М., Громова М.И. Практическое руководство по спектрофотометрии и колориметрии. – Изд-во Московского университета, 1965 – 136 с. 14. Руководство по контролю загрязненной атмосферы. – Л.: Гидрометеоиздат, 1979
ТЕОРЕТИЧНА ЧАСТИНА 1.1
Особливість фізико-хімічних методів аналізу полягає в тому, що перебіг використаної для аналізу хімічної реакції контролюють за зміною будь-якої фізичної властивості. Взагалі, фізико-хімічні методи аналізу класифікують за типом фізико-хімічних явищ, що лежать в їх основі [8]. Оптичні методи аналізу грунтуються на вимірюванні оптичних властивостей аналізованого середовища (інтенсивності забарвлення, оптичної густини, коефіцієнта заломлення, спектральних характеристик і ін.). Електрохімічні методи аналізу - сукупність методів якісного та кількісного аналізу речовин, що ґрунтуються на процесах, які протікають на електродах або у міжелектродному просторі. Хроматографічні методи є ефективними методами розділення і аналізу складних за складом газоподібних і рідких сумішей [6] Фотоколориметричне визначення фенолу в повітрі (метод з діазотованим паранітроаніліном) Фотоколориметрія – це метод кількісного аналізу, ґрунтується на вимірюванні ступеня поглинання або пропускання немонохроматичного світла речовиною, яку визначають. У фотоколориметрії вимірювання інтенсивності світлових потоків проводять за допомогою фотоелементів. Фотоелементи – прилади, що перетворюють світлову енергію в електричний струм. Зміна інтенсивності світлового потоку викликає зміну електричного струму виробленого фотоелементом. Фотоколориметричні методи – це кількісне визначення концентрації речовини з поглинання світла у видимій та ближній ультрафіолетовій області спектра. Поглинання світла вимірюють на фотоелектричних колориметрах (КФК-2, КФК-3, ФЕК-56М та інших) [14]. Принцип методу. Метод ґрунтується на взаємодії фенолу і діазотованого паранітроаніліну з утворенням сполуки, забарвленої в червоний колір, також на поглинанні фенолу з повітря розчином карбонату натрію, витяганні фенолу з отриманого розчину бутилацетатом і вимірюванні масової концентрації. Для визначення використовують прилад колориметр фотоелектричний концентраційний КФК-2 (рис.1.1) [7].
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 433; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.83.96 (0.01 с.) |



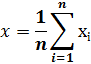
 - результат одиничного вимірювання (визначення);
- результат одиничного вимірювання (визначення); - вибірка (кількість паралельних вимірювань, визначень)
- вибірка (кількість паралельних вимірювань, визначень)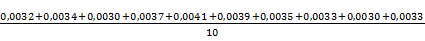 =0,0034мг/м3
=0,0034мг/м3
 – істинне (або середнє арифметичне) значення
– істинне (або середнє арифметичне) значення х4 = 0,0037 – 0,0034 = 0,0003 мг/м3
х4 = 0,0037 – 0,0034 = 0,0003 мг/м3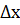 7 = 0,0035 – 0,0034 = 0,0001 мг/м3
7 = 0,0035 – 0,0034 = 0,0001 мг/м3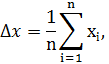
 =
= 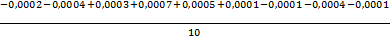 = 0,0008мг/м3
= 0,0008мг/м3
 =
=  = 0,00036 мг/м3
= 0,00036 мг/м3 =
= 
 = 0,00003 мг/м3
= 0,00003 мг/м3 = ±
= ± 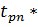 S
S 
 - коефіцієнт Стьюдента при довірчій імовірності Р у залежності від кількості визначень n.
- коефіцієнт Стьюдента при довірчій імовірності Р у залежності від кількості визначень n. - стандартне відхилення середнього арифметичного.
- стандартне відхилення середнього арифметичного.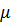 =
= 
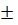 0,00006 мг/м3
0,00006 мг/м3
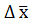
 0,00006 мг/м3
0,00006 мг/м3







