Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Влияние заместителей в бензольном кольце на основность ⇐ ПредыдущаяСтр 3 из 3
- повышают электронную плотность в кольце, уменьшают сопряжение между ароматической системой и неподеленной парой электронов, увеличивается электронная плотность на атоме азота, - увеличивается устойчивость аммонийного катиона.
- уменьшают электронную плотность в бензольном кольце, увеличивают сопряжение между ароматической системой и неподеленной парой электронов, уменьшается электронная плотность на атоме азота, - уменьшается устойчивость аммонийного катиона.
- М-эффект сильнее передается в п-положение -I- эффект сильнее в о-положении, особенно для акцепторов (о-эффект заместителя) Заместитель о- м- п- CH3O 4.52 4.23 5.34 H 4.62 Cl 2.65 3.52 3.98 NO2 0.26 2.47 1.02
Влияние заместителей при атоме азота на основность Аналогично алифатическому ряду - алкильные заместители увеличивают основность (+I); - при ацилировании основность резко снижается, т.к. неподеленная пара е- сопрягается и с ароматической системой, и π-связью карбоксильной группы; -алкилирование непосредственно по N дает меньшее увеличение основности, чем при введение алкильной группы по бензольному кольцу, т.к. изменяется геометрия аминогруппы, сопряжение усиливается, сольватация катиона меньше.
III. Нуклеофильность аминов (взаимодействие с электрофилами) 1. Алкилирование (см. способы получения) 2. Ацилирование ( синтез новых, нетоксичных соединений, защита от окисления, уменьшение активности аминогруппы и синтез монопродуктов). Общая схема:
Выбор ацилирующего агента зависит от субстрата. а) активные амины (с донорами)
N-(4-этоксифенил)-ацетамид б) неактивные амины(с акцепторными заместителями)
в) современный ацилирующий агент – метилхлорформиат (метиловый эфир хлоругольной кислоты)
2 CH3OH + 2 COCl2 + CaCO3 → 2 CH3OCOCl + CaCl2 +CO2 + H2O фосген г) бензоилирование – метод Шоттена-Баумана
д) введение остатка бензолсульфокислоты (только хлорангидридами!!!)
Реакция - в основе пробы Хильсберга для разделения аминов через имиды сульфокислот.
3. Реакция с азотистой кислотой (с диазотирующей смесью) – идентификация!!!
4. Изонитрильная реакция (качественная реакция на первичные амины)
Реакция с карбонильными соединениями (алифатическими и ароматическими)
Алкилирование и солеобразование идет по алифатическому центру.
Ацилирование идет по алифатическому центру, а солеобразование по ароматическому, а не по амидному.
IV. SE аром. по бензольному кольцу Высокореакционные соединения. Донорные свойства параллельно нуклеофильности
Аминогруппа и ее производные – сильные донорные заместители, ацетамидная группа – самый слабый донор. О- и п-ориентанты. Аммонийный катион не имеет неподеленной пары электронов, акцептор за счет индуктивного эффекта, м-ориентант.
устойчив
Алкилирование и ацилирование по атому С
Ацилирование защищает аминогруппу от дезактивации AlCl3 (как кислотой Льюиса). 2. Галогенирование (хлорирование, бромирование и иодирование как для π-избыточной системы)
Качественная реакция Ацилирование предотвращает окисление, снижает донорные свойства аминогруппы и дает возможность получить монопроизводные.
Нитрование а) нитрующей смесью (сильное окисление, требуется защита)
б) разбавленной азотной кислотой (без окисления)
Сульфирование а) серной кислотой и олеумом
Синтез п-изомера этим методом через ацилирование. б) метод запекания
При высокой температуре - разрушение соли.
в) сульфотриоксид в инертном растворителе (ДХЭ)
П-аминобензолсульфокислота (сульфаниловая кислота) При низкой температуре не происходит разрушение субстрата и окисления.
Сульфаниловая кислота - цвиттер-ион (рентгено-структурный анализ, спектральные методы анализа, высокая Тпл. с разложением, нерастворима в водных растворах кислот)
5. Сульфохлорирование ( с окислением, требуется предварительная защита)
Синтез стрептоцида и альбуцида
Сульфаниламиды - биоизостеры п-аминобензойной кислоты. Это объясняет высокую биологическую активность сульфаниламидных препаратов.
Как высокореакционноспособные соединения вступают в реакцию SЕ аром. со слабыми электрофилами. Реакция азосочетания
7. Реакция третичных аминов с альдегидами и азотистой кислотой (см. выше). V. Окисление Легко окисляются с образованием различных продуктов: Основание Шиффа
|
||||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 1492; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.107.90 (0.014 с.) |
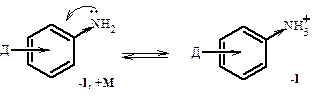 Доноры увеличивают основность, т.к.
Доноры увеличивают основность, т.к.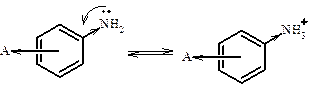 Акцепторы уменьшают основность, т.к.
Акцепторы уменьшают основность, т.к.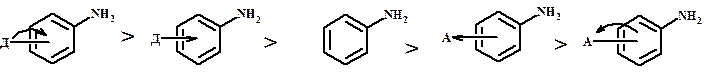

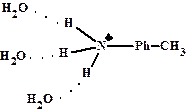
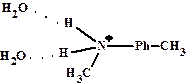
 RCOX = RCOCl, (RCO)2O, RCOOH, RCOOCH3 – уменьшение ацилирующей способности.
RCOX = RCOCl, (RCO)2O, RCOOH, RCOOCH3 – уменьшение ацилирующей способности.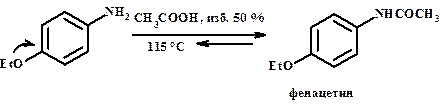 Ацилирование кислотой – процесс обратимый, сдвиг равновесия – избыток кислоты, отгон продукта органическими растворителями, отгон воды с кислотой, применение водоотнимающих средств.
Ацилирование кислотой – процесс обратимый, сдвиг равновесия – избыток кислоты, отгон продукта органическими растворителями, отгон воды с кислотой, применение водоотнимающих средств.





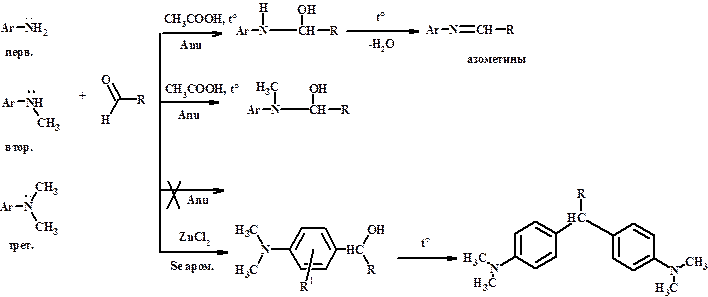
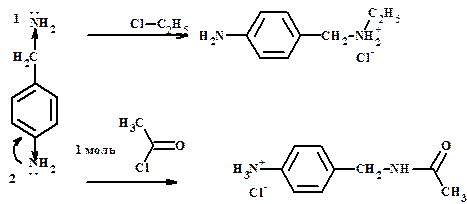 Нуклеофильность меняется параллельно основности. Направление реакции зависит от силы центра.
Нуклеофильность меняется параллельно основности. Направление реакции зависит от силы центра.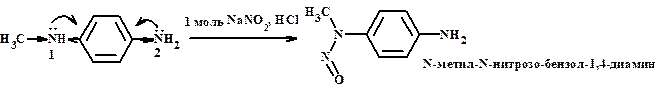

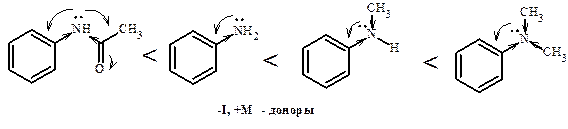

 σ –комплекс в п-положении
σ –комплекс в п-положении