
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
II. По степени замещенности NСтр 1 из 3Следующая ⇒
АРОМАТИЧЕСКИЕ АМИНЫ Ароматические амины – производные аммиака, в котором атомы Н заменены на арильный радикал. КЛАССИФИКАЦИЯ I. По характеру радикала 1. Ароматические амины ArNH2 2. Ароматические соединения с аминогруппой в боковой цепи Ar(CH2)nNH2 3. Жирноароматические амины ArNHAlk II. По степени замещенности N 1. Первичные амины ArNH2 2. Вторичные амины ArNHAr, ArNHAlk 3. Третичные амины ArNH(Alk)2 и т.д. 4. Четвертичные аммонийные соли и основания
НОМЕНКЛАТУРА 1. Тривиальная – отдельные названия (анилин, толуидин…) 2. Систематическая (ИЮПАК) – производные анилина или бензоламина 3. Радикально-функциональная – алкилариламин
Анилин п-толуидин о-анизидин о-фенилендиамин Бензоламин 2-метиланилин 2-метоксианилин 1,2-бензолдиамин Фениламин о-толиламин о-метоксифениламин о-фенилендиамин
- бензиламин - N-метиланилин 1-фенилметанамин 1-фенилпропан-2-амин Метилфениламин бензиламин -
Ацетат 2,5-ксилидиния - Ацетат 2.5-диметиланилиния гидросульфат диметил-п-хлорфенилметиламмония ИЗОМЕРИЯ I. Структурная изомерия
В бензольном кольце п- изомер м-изомер
Изомерия углеродного скелета
II. Пространственная изомерия 1. изомерия (σ-связь С-С в sp3) 2. а) при наличии Асимметрического атома С (S) 1-фенил-1-этанамин
б) для четвертичных аммонийных солей С различными заместителями Отсутствует превращение пирамидальных конфигураций из одной в другую, как в аминах, где энергетический барьер всего 25 кДж/моль.
(R)-аллилбензилметилфениламмоний
ФИЗИЧЕСКИЕ СВОЙСТВА Ароматические амины – бесцветные жидкости или кристаллические вещества со специфическими запахами. Мало или нерастворимы в воде. Легко окисляются и темнеют. Токсичны (для анилина ПДК -0,1 мг/м3), некоторые концерогенны, как бензидин и β-нафтиламин.
Соли аминов – типичные ионные соединения. Нелетучие твердые вещества с высокой Тпл., многие растворимы в воде (галогениды, нитраты, сульфаты и др.) Различие в растворимости аминов и их солей используются для обнаружения аминов и выделения аминов из смеси соединений, не являющихся основаниями.
СПОСОБЫ ПОЛУЧЕНИЯ I. Способы получения первичных аминов Восстановление нитросоединений Промышленный и лабораторный способ, доступны исходные вещества. При выборе восстановителя и условий проведения реакции учитывать восстановление других групп. Скорость восстановления групп: C=C < C=O < COOH < C≡N < CONH2 < NO2 а) каталитическое гидрирование водородом
Глубина восстановления зависит от условий ведения процесса.
б) химическое восстановление активным водородом Me + HX, где Me = Sn, Zn, Fe - железом в присутствии электролита (хлорида аммония) Не восстанавливаются альдегиды, производные кислот, азосоединения.
Производство анестезина, новокаина. - оловом (или цинком) в соляной кислоте (лабораторный синтез)
- хлоридом олова Избирательное восстановление полинитросоединений, не восстанавливаются галогены в кольце.
- сульфидом и гидросульфидом аммония и щелочных металлов Неселективное моновосстановление полинитросоединений, не восстанавливает гидроксигруппу
Аммонолиз галогенопроизводных а) с алифатическими галогенопроизводными
Недостатки метода: смесь первичных, вторичных и третичных аминов, т.к. скорость каждой последующей стадии выше. Избыток аммиак и карбоната аммония увеличивает выход первичного амина. Разделение смеси – фракционная перегонка, химические методы. б) с ароматическими галогенопроизводными
3. Расщепление амидов по Гофману (синтез с уменьшением цепи).
4. Восстановление нитрилов и оксимов [H] = LiAlH4, H2/Ni Re, Na мет. в спирте
5. Восстановительное аминирование ароматических карбонильных соединений
ЭЛЕКТРОННОЕ СТРОЕНИЕ
Неподеленная электронная пара атома азота вступает в сопряжение с ароматической π- системой (+М).
Данное электронное строение позволяет предположить следующую реакционную способность: 1. Кислотность N-H 4. SEаром. 2. Основность 5. окисление 3. Нуклеофильность ХИМИЧЕСКИЕ СВОЙСТВА I. Кислотность N-H-связи Ароматические амины слабые кислоты, рКа ~30-35, сильнее, чем NH3 и алканы.
II. Основность C минеральными и органическими кислотами донорно-акцепторным механизмом путем присоединения протона образуют четвертичные аммонийные соли.
Основность зависит от факторов: величина е-плотности на N, устойчивость катиона, сольватация исходного и конечного состояния. Влияние бензольного кольца
РКа 9.24 10.62 9.36 4.62 0.8 --
Введение арильного заместителя снижает основность атома азота, т.к. - уменьшается индуктивный эффект, -неподеленная пара электронов связана мезомерным эффектом, - нейтральная форма резонансно стабилизирована, а катион – нет.
Нейтр. Форма катион
N-(4-этоксифенил)-ацетамид б) неактивные амины(с акцепторными заместителями)
в) современный ацилирующий агент – метилхлорформиат (метиловый эфир хлоругольной кислоты)
2 CH3OH + 2 COCl2 + CaCO3 → 2 CH3OCOCl + CaCl2 +CO2 + H2O фосген г) бензоилирование – метод Шоттена-Баумана
д) введение остатка бензолсульфокислоты (только хлорангидридами!!!)
Реакция - в основе пробы Хильсберга для разделения аминов через имиды сульфокислот.
3. Реакция с азотистой кислотой (с диазотирующей смесью) – идентификация!!!
4. Изонитрильная реакция (качественная реакция на первичные амины)
Нитрование а) нитрующей смесью (сильное окисление, требуется защита)
б) разбавленной азотной кислотой (без окисления)
Сульфирование а) серной кислотой и олеумом
Синтез п-изомера этим методом через ацилирование. б) метод запекания
При высокой температуре - разрушение соли.
в) сульфотриоксид в инертном растворителе (ДХЭ)
П-аминобензолсульфокислота (сульфаниловая кислота) При низкой температуре не происходит разрушение субстрата и окисления.
Сульфаниловая кислота - цвиттер-ион (рентгено-структурный анализ, спектральные методы анализа, высокая Тпл. с разложением, нерастворима в водных растворах кислот)
5. Сульфохлорирование ( с окислением, требуется предварительная защита) Синтез стрептоцида и альбуцида
Сульфаниламиды - биоизостеры п-аминобензойной кислоты. Это объясняет высокую биологическую активность сульфаниламидных препаратов.
Как высокореакционноспособные соединения вступают в реакцию SЕ аром. со слабыми электрофилами. Реакция азосочетания
7. Реакция третичных аминов с альдегидами и азотистой кислотой (см. выше). V. Окисление Легко окисляются с образованием различных продуктов: Основание Шиффа БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ Наличие свободной аминогруппы обеспечивает токсичность соединения, введение ацильной защиты снижает токсичность препарата. Биологически активные соединения этого ряда представлены:
1.сульфаниламидными препаратами (стрептоцид, альбуцид и др.), обладающими антимикробным действием:
Стрептоцид альбуцид 2. производными β-фенилэтиламина, симпатомимитическими лекарственными веществами (расширяют зрачок глаза, усиливают сердцебиение, увеличивают давление крови):
(сильный (гормон, увеличивает (алкалоид, стимулятор ЦНС) стимулятор ЦНС) артериальное давление) 3. жаропонижающие вещества:
4. отдельные препараты: Анестезин (анестетик) Хлоракон (противосудорожный препарат) 5. рентгеноструктурные препараты: Триомбраст
АРОМАТИЧЕСКИЕ АМИНЫ Ароматические амины – производные аммиака, в котором атомы Н заменены на арильный радикал. КЛАССИФИКАЦИЯ I. По характеру радикала 1. Ароматические амины ArNH2 2. Ароматические соединения с аминогруппой в боковой цепи Ar(CH2)nNH2 3. Жирноароматические амины ArNHAlk II. По степени замещенности N 1. Первичные амины ArNH2 2. Вторичные амины ArNHAr, ArNHAlk 3. Третичные амины ArNH(Alk)2 и т.д. 4. Четвертичные аммонийные соли и основания
НОМЕНКЛАТУРА 1. Тривиальная – отдельные названия (анилин, толуидин…) 2. Систематическая (ИЮПАК) – производные анилина или бензоламина 3. Радикально-функциональная – алкилариламин
|
|||||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 774; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.195.110 (0.07 с.) |


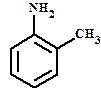

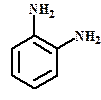



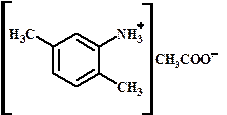
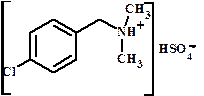

 1. положение заместителя
1. положение заместителя


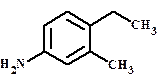
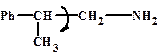 Конформационная
Конформационная Оптическая изомерия
Оптическая изомерия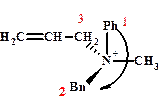


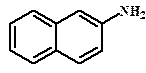




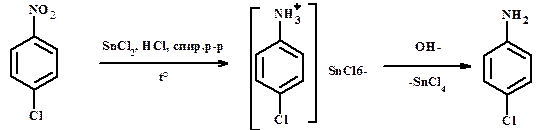



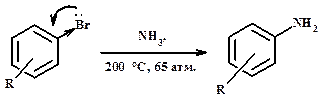 Низкая реакционная способность объясняется действием мезомерного эффекта, связь С-Hal укорачивается, реакция возможна при высокой температуре, с применением сильного основного реагента.
Низкая реакционная способность объясняется действием мезомерного эффекта, связь С-Hal укорачивается, реакция возможна при высокой температуре, с применением сильного основного реагента. При наличии электроноакцепторного заместителя, особенно в о- и п-положениях ускоряется процесс замещения.
При наличии электроноакцепторного заместителя, особенно в о- и п-положениях ускоряется процесс замещения.


 По σ-связям C-N и N-H из-за разности электроотрицательности индуктивным эффектом электронная плотность смещена к атому азота (-I).
По σ-связям C-N и N-H из-за разности электроотрицательности индуктивным эффектом электронная плотность смещена к атому азота (-I). +M >> -I, следовательно, аминогруппа – сильный донор, вызывает перераспределение электронной плотности в кольце, о- и п-положениях δ-заряд.
+M >> -I, следовательно, аминогруппа – сильный донор, вызывает перераспределение электронной плотности в кольце, о- и п-положениях δ-заряд.



 Ароматические амины менее основные, чем алифатические.
Ароматические амины менее основные, чем алифатические.




















 Фенамин Адреналин Эфедрин
Фенамин Адреналин Эфедрин Мефенаминовая кислота Парацетамол Фенацетин Фенетидин
Мефенаминовая кислота Парацетамол Фенацетин Фенетидин




 Триомбрин
Триомбрин 



