
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислотно-основные индикаторыСодержание книги
Поиск на нашем сайте
В титриметрическом методе анализа для определения конца титрования (точки эквивалентности) применяют индикаторы. В методе кислотно-основного взаимодействия с этой целью используют такие вещества, окраска которых меняется в кислой и щелочной среде. Их называют кислотно-основные индикаторы или рН-индикаторы. Кислотно-основные индикаторы представляют собой слабые органические кислоты или основания, протонированные и непротанированные формы которых различаются по структуре и окраске. Существуют одноцветные (например, фенолфталеин) и двуцветные (например, метиловый оранжевый) индикаторы. Окраска каждого из индикаторов изменяется в пределах определенного узкого интервала значений рН, его называют интервале значений рН, его называют интервале перехода окраски индикатора. Для двуцветных индикаторов он рассчитывается по формуле: ∆рН=рКи±1, где Ки – константа диссоциации индикатора. В пределах интервала перехода наиболее резко изменение индикатора наблюдается при определенном значении рН, которое называется показателем титрования и обозначается рТ. Величина рТ находится приблизительно в середине интервала перехода и фактически отождествляется м рКи. Выбирают индикатор для титрования так, чтобы интервал перехода окраски индикатора (или рТ) ближе всего совпадал бы с рН титруемого раствора в точке эквивалентности. Поэтому для правильного выбора индикатора необходимо проследить характер кривой титрования, величину скачка титрования и установить рН, соотвествующее точке эквивалентности. Для сужения интервала перехода и получения более резкого перехода окраски применяют смешанные индикаторы, которые составляют из индикатора и красителя. При определенном значении рН цвет красителя является дополнительным к цвету индикатора. В результате в этой точке окраска будет серой, а переход от окрашенного раствора к серому – контрастным. Так как в кислотно-основных титрованиях обычно в качестве титранта применяют либо сильную кислоту, либо сильное основание, при выборе индикатора для титрования кислот и оснований можно пользоваться следующими общими указаниями: 1. При титровании сильных кислот и оснований (~0,1 н.) можно применять любой индикатор с рН интервала перехода в пределах 4,3 – 9,7 (от метилового оранжевого до фенолфталеина). При титровании более концентрированных растворов, чем 0,1 н., можно применять любой индикатор с рН интервала перехода 3,3 – 10,7. 2. При титровании слабой кислоты сильным основанием конец титрования наблюдается в интервалах рН=7,74 – 10. В этих случаях можно использовать, например, индикаторы: феноловый красный, тимоловый голубой, фенолфталеин, тимолфталеин. 3. При титровании слабого основания сильной кислотой конец титрования наблюдается в интервале рН=6,26-4. В этих случаях применяют, например, индикаторы: п-нитрофенол, метиловый красный, метиловый оранжевый. 4. При титровании многоосновных кислот или многокислотных оснований нужно рассчитать значения рН для каждой точки эквивалентности и подобрать соответствующие индикаторы. Например, при титровании фосфорной кислоты первая точка эквивалентности соответствует рН=4,33; вторая – 9,57; третья – 12,72. Следовательно, для титрования до NaH2PO4 нужно применять метиловый оранжевый, до Na2HPO4 – фенолфталеин, до Na3PO4 – тимоловый голубой. Наиболее широко применяемые в кислотно-основном титровании индикаторы и интервалы их перехода представлены далее.
Важнейшие кислотно-основные индикаторы
Редокс-индикаторы Для определения конца титрования (точки эквивалентности) в редоксиметрии используют: а) безиндикаторное титрование (при исчезновении или появлении окраски титранта или титруемого вещества); б) специфические индикаторы; в) окислительно-восстановительные (редокс-индикаторы). Специфические индикаторы – это вещества, которые образуют интенсивно окрашенные соединения с одним из компонентов окислительно-восстановительной реакции. Например, при титровании йода используют специфический индикатор – крахмал, образующий темно-синее соединение с I-3-ионами. При титровании Fe(III) раствором соли Ti(III) в качестве индикатора используют роданид – ионы, которые образуют с Fe(III) комплексы, окрашенные в интенсивно-красный цвет; конечную точку титрования определяют по исчезновению окраски. Окислительно-восстановительные редокс-индикаторы – это соединения, в основном, органические, способные к окислению и восстановлению, причем их окисленная и восстановленная формы имеют разную окраску. В качестве редокс – индикаторов применяют также комплексы органических лигандов с металлами, способными изменять степень окисления. Для сопряженной редокс-пары: Indox+ne↔IndRed потенциал рассчитывают по уравнению Нернста (при 250С):
где Е0-стандартный потенциал, В; N – число отданных или принятых электронов; [Indox]–концентрация окисленной формы индикатора (моль/л) [IndRed]-концентрация восстановленной формы индикатора (моль/л). Приняв предельные соотношения окисленной и восстановленной форм индикатора, при которых заметна окраска одной из форм, равным 10:1 и 1:10, область перехода окраски можно охарактеризовать как область значений потенциала: ∆Е=Е0(Indox/IndRed)± Так же, как и при кислотно-основном титровании, интервал перехода окраски индикатора должен лежать внутри скачка титрования. Например, для дихроматометрического определения Fe(II) в 0,1 М H2SO4 пригодны индикаторы, изменяющие окраску в интервале 0,85-1,25 В, в том числе широко известный дифениламин (Е0=0,76В) или дифениламинсульфокислота (Е0=0,85В). Важнейшие редокс-индикаторы
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 1892; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.58.32.115 (0.008 с.) |

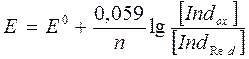 ,
,



