Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гипертрофия миокарда. Особенности гипертрофированного сердца, механизмы его декомпенсации.Содержание книги
Поиск на нашем сайте
Как и при острой, так и при хронической сердечной недостаточности все эндогенные механизмы компенсации гемодинамических нарушений можно подразделить на интракардиальные: компенсаторная гиперфункция сердца (механизм Франка-Старлинга, гомеометрическая гиперфункция), гипертрофия миокарда и экстракардиальные: разгрузочные рефлексы Бейнбриджа, Парина, Китаева, активация выделительной функции почек, депонирование крови в печени и селезенке, потоотделение, испарение воды со стенок легочных альвеол, активация эритропоэза и др. Такое деление в некоторой степени условно, поскольку реализация как интра-, так и экстракардиальных механизмов находится под контролем нейрогуморальных регуляторных систем. Гипертрофия миокарда - это увеличение массы сердца за счет увеличения размеров кардиомиоцитов. Существуют три стадии компенсаторной гипертрофии сердца. Первая, аварийная, стадия характеризуется, прежде всего, увеличением интенсивности функционирования структур миокарда и, по сути, представляет собой компенсаторную гиперфункцию еще не гипертрофированного сердца. Интенсивность функционирования структур - это механическая работа, приходящаяся на единицу массы миокарда. Увеличение интенсивности функционирования структур закономерно влечет за собой одновременную активацию энергообразования, синтеза нуклеиновых кислот и белка. Указанная активация синтеза белка происходит таким образом, что вначале увеличивается масса энергообразующих структур (митохондрий), а затем - масса функционирующих структур (миофибрилл). В целом увеличение массы миокарда приводит к тому, что интенсивность функционирования структур постепенно возвращается к нормальному уровню.
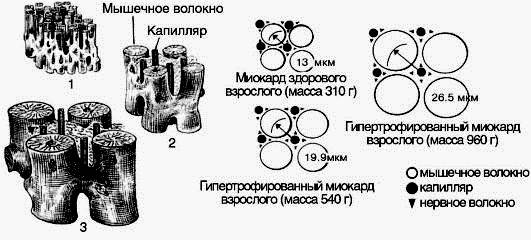
Третья стадия прогрессирующего кардиосклероза и декомпенсации характеризуется нарушением синтеза белков и нуклеиновых кислот в миокарде. В результате нарушения синтеза РНК, ДНК и белка в кардиомиоцитах наблюдается относительное уменьшение массы митохондрий, что ведет к торможению синтеза АТФ на единицу массы ткани, снижению насосной функции сердца и прогрессированию хронической сердечной недостаточности. Ситуация усугубляется развитием дистрофических и склеротических процессов, что способствует появлению признаков декомпенсации и тотальной сердечной недостаточности, завершающейся гибелью пациента. Компенсаторная гиперфункция, гипертрофия и последующая декомпенсация сердца - это звенья единого процесса. Механизм декомпенсации гипертрофированного миокарда включает следующие звенья: 1. Процесс гипертрофии не распространяется на коронарные сосуды, поэтому число капилляров на единицу объема миокарда в гипертрофированном сердце уменьшается (рис. 15-11). Следовательно, кровоснабжение гипертрофированной сердечной мышцы оказывается недостаточным для выполнения механической работы. 2. Вследствие увеличения объема гипертрофированных мышечных волокон уменьшается удельная поверхность клеток, в связи с этим ухудшаются условия для поступления в клетки питательных веществ и выделения из кардиомиоцитов продуктов метаболизма.
Рис. 5-11. Гипертрофия миокарда: 1 - миокард здорового взрослого; 2 - гипертрофированный миокард взрослого (масса 540 г); 3 - гипертрофированный миокард взрослого (масса 960 г) 3. В гипертрофированном сердце нарушается соотношение между объемами внутриклеточных структур. Так, увеличение массы митохондрий и саркоплазматического ретикулума (СПР) отстает от увеличения размеров миофибрилл, что способствует ухудшению энергоснабжения кардиомиоцитов и сопровождается нарушением аккумуляции Са2+ в СПР. Возникает Са2+-перегрузка кардиомиоцитов, что обеспечивает формирование контрактуры сердца и способствует уменьшению ударного объема. Кроме того, Са2+-перегрузка клеток миокарда повышает вероятность возникновения аритмий. 4. Проводящая система сердца и вегетативные нервные волокна, иннервирующие миокард, не подвергаются гипертрофии, что также способствует возникновению дисфункции гипертрофированного сердца. 5. Активируется апоптоз отдельных кардиомиоцитов, что способствует постепенному замещению мышечных волокон соединительной тканью (кардиосклероз). В конечном итоге гипертрофия утрачивает приспособительное значение и перестает быть полезной для организма. Ослабление сократительной способности гипертрофированного сердца происходит тем скорее, чем сильнее выражены гипертрофия и морфологические изменения в миокарде. Компенсаторная гиперфункция сердца -↑ работы сердца при длительном воздействии перегрузки. Стадии: 1. Аварийная стадия - кратковременная, патологические реакции преобладают над компенсаторными. Характеризуется ↑ нагрузки на сердце, ↓ гликогена в миокарде, ↓ креатинфосфата, ↓ внутриклеточного K и ↑Na, распад гликогена и накопление лактата, гликолиз, активируется анаэробный синтез АТФ, активируется анаэробный ресинтез АТФ, растет масса миофибрилл, растет потребление кислорода, ↑ нагрузки на единицу мышечной массы сердца - ↑ интенсивности функционирования структур (ИФС); активация генетического аппарата, ↑ синтеза нукл к-т и белка с нарастанием кол-ва митохондрий → гипертрофия миокарда в течение нескольких недель. Клинически - острая недостаточность сердца 2. Стадия завершившейся гипертрофии и относительно устойчивой гиперфункции. Процесс гипертрофии завершён, масса миокарда ↑ и уже не растёт, ИФС нормализована, нормальная активность генетического аппарата, гемодинамика компенсирована. Клинически - нормализация гемодинамики. 3. Стадия постепенного истощения и прогрессирующего кардиосклероза. Развивается при прогрессировании процесса с ↑ нагрузки на сердце. Развивается комплекс изнашивания гипертрофированного сердца. Избирательная гибель кардиомиоцитов с замещением их соед. тканью. Основная причина комплекса изнашивания – рост митохондрий отстаёт от миофибрилл и часть миокарда остаётся энергетически необеспеченной; энергии не хватает и возникает истощение. Клинически: недостаточность сердца и кровообращения. Общие черты внутрисердечной гемодинамики при серд недостаточности: ↑ остаточного диастолического объёма вследствие неполной систолы ↑ диастолического давления в желудочках дилатация сердца ↓МОК (может быть и ↑). Основные особенности гипертрофированного миокарда: 1. нарушение регуляции гипертрофированного сердца (отставание роста рецепторов и др. нервных окончаний от роста миокарда) 2. ↓ сосудистой обеспеченности миокарда (отставание роста мелких сосудов от роста мышечных кл-к) 3. развитие относительной коронарной недостаточности 4. ↑ массы кардиомиоцитов по сравнению с их поверхностью. Причина – относительный недостаток ферментов, субстратов-белков 5. ↓ уровня энергообеспечения кл-к миокарда (отставание ↑ кол-ва митохондрий от роста массы миофибрилл) 6. ↓ сократительной способности миокарда Гипертрофия миокарда Гипертрофия миокарда — явление приспособительное, направленное на выполнение повышенной работы без существенного повышения нагрузки на единицу мышечной массы миокарда. Однако при экспериментальном пороке сердца повышение нагрузки и изменения гемодинамики развиваются остро, что бывает и у человека, например, при травматических пороках, острой перегрузке нетренированных людей, гипертензивных кризах. По динамике изменения обмена, структуры и функции миокарда в компенсаторной гиперфункции сердца можно выделить три основные стадии (Ф.З.Меерсон). Аварийная стадия развивается непосредственно после возникновения порока, характеризуется сочетанием выраженных патологических изменений в миокарде и явлений острой недостаточности сердца с мобилизацией резервов миокарда и организма в целом. В этой стадии наблюдается быстрое (в течение недель) увеличение массы сердца на 30-70%. Стадия относительно устойчивой гиперфункции. В этой стадии постепенно уменьшаются и даже исчезают патологические изменения обмена и структуры миокарда, нормализуется гемодинамика, масса миокарда увеличена на 100-120% и больше не растет. Гипертрофированное сердце приспособилось к новым условиям нагрузки, имеется полная компенсация. Эта фаза длительная. Стадия постепенного истощения и прогрессирующего кардиосклероза характеризуется глубокими обменными и морфологическими изменениями, которые исподволь накапливаются в энергообразующих и сократительных структурах мышечной клетки, гибелью части мышечных волокон и заменой их соединительной тканью. Эти изменения приводят к недостаточности сердца и в дальнейшем к недостаточности кровообращения. Особенности гипертрофированного миокарда. Гипертрофированное сердце отличается от нормального такими структурными, обменными и функциональными признаками: o Гипертрофированное сердце увеличено в объеме (главным образом за счет цитоплазмы). o Резко ограничена способность ядра высокодифференцированной клетки к делению, происходит относительное уменьшение массы ядра. o Ухудшается пластическое обеспечение клетки. o Длительная и интенсивная нагрузка на сердечное мышечное волокно приводит к его истощению и нарушению функции. o Вследствие нарушения образования энергии митохондриями и использования энергии сократительным аппаратом возникают изменения сократительной функции мышечного волокна. o Ухудшается сосудистое обеспечение гипертрофированного миокарда, поскольку увеличение мышечных волокон чаще всего не сопровождается адекватным увеличением капиллярной сети. o Кардиомиоциты замещаются соединительной тканью и, если 20-30% массы сердца будет заменено соединительной тканью, нормальная работа сердца невозможна. Гипертрофия миокарда. Длительное увеличение нагрузки на сердечную мышцу сопровождается увеличением нагрузки на единицу мышечной массы, повышением интенсивности функционирования ее структур (ИФС). В ответ на это активизируется генетический аппарат мышечных и соединительнотканных клеток. К концу первых суток усиливается синтез белков, что ведет к быстрому увеличению объема мышечного волокна, его гипертрофии и, как правило, сопровождается гипертрофией того отдела сердца, который испытывает повышенную нагрузку. При этом увеличивается объем каждого сердечного мышечного волокна, общее же число волокон остается неизменным. Гипертрофия миокарда ведет к снижению нагрузки на единицу мышечной массы до нормального уровня, нормализации ИФС. При снижении нагрузки, например при ликвидации стеноза, восстановлении клапанов, масса миокарда уменьшается до нормы. Это указывает на то, что интенсивность синтеза белков в клетках миокарда в значительной степени регулируется уровнем нагрузки. Кроме того, этот процесс контролируется механизмами нервно-гуморальной регуляции. Гипертрофия миокарда — явление приспособительное, направленное на выполнение повышенной работы без существенного повышения нагрузки на единицу мышечной массы миокарда. Это весьма совершенное приспособление. Так, гипертрофия сердца у спортсмена, например, позволяет ему выполнять очень большую работу. При этом наряду с гипертрофией изменяется и нервная регуляция сердца, что значительно расширяет диапазон его адаптации и благоприятствует выполнению значительных нагрузок. Гипертрофированное сердце отличается от нормального по ряду обменных, функциональных и структурных признаков, которые, с одной стороны, позволяют ему длительное время преодолевать повышенную нагрузку, а с другой — создают предпосылки для возникновения патологических изменений. Увеличение массы сердца происходит вследствие утолщения каждого мышечного волокна, что сопровождается изменением соотношения внутриклеточных структур. Объем клетки при этом увеличивается пропорционально кубу линейных размеров, а поверхность — пропорционально их квадрату, что приводит к уменьшению клеточной поверхности на единицу массы клетки. Известно, что через поверхность клетки происходит ее обмен с внеклеточной жидкостью — поглощение кислорода, питательных веществ, выведение продуктов метаболизма, обмен воды и электролитов. В силу перечисленных изменений возникают условия для ухудшения снабжения мышечного волокна, особенно его центральных отделов. Клеточная мембрана играет большую роль в проведении возбуждения и в сопряжении процессов возбуждения и сокращения, осуществляемом через тубулярную систему и саркоплазматический ретикулум. Поскольку рост этих образований при гипертрофии мышечного волокна также отстает, то создаются предпосылки для нарушения процессов сокращения и расслабления кардиомиоцитов: вследствие замедления выхода ионов кальция в миоплазму ухудшается сокращение, а в результате затруднения обратного транспорта ионов кальция в ретикулум — расслабление, иногда могут возникать локальные контрактуры отдельных кардиомиоцитов. При гипертрофии увеличение объема клетки происходит в большей степени, чем объема ядра. Способность ядра высокодифференцированной клетки к делению резко ограничена. При этом увеличиваются только линейные размеры ядер за счет увеличения числа хромосом, что сопровождается некоторым увеличением содержания ДНК. А так как роль ядра заключается в обеспечении белкового синтеза, а следовательно, и процессов восстановления внутриклеточных структур, то относительное уменьшение ядра может привести к нарушению синтеза белков и ухудшению пластического обеспечения клетки. В процессе развития гипертрофии масса митохондрий вначале увеличивается быстрее, чем масса сократительных белков, создавая условия для достаточного энергетического обеспечения и хорошей компенсации функции сердца. Однако в дальнейшем, по мере усугубления процесса, увеличение массы митохондрий начинает отставать от роста массы цитоплазмы. Митохондрии начинают работать с предельной нагрузкой, в них развиваются деструктивные изменения, снижается эффективность их работы, нарушается окислительное фосфорилирование. Это ведет к ухудшению энергетического обеспечения гипертрофированной клетки. Увеличение массы мышечных волокон зачастую не сопровождается адекватным увеличением капиллярной сети, особенно в случаях быстрого развития недостаточности сердца. Крупные венечные артерии также не обладают необходимым приспособительным ростом. Поэтому во время нагрузки ухудшается сосудистое обеспечение гипертрофированного миокарда. В гипертрофированном сердце нарушена структура вставочных дисков и z-полос, что имеет своим следствием изменение электрической активности миокарда, ухудшение координированности сокращения сердца в целом. При развитии гипертрофии миокарда в процесс обязательно вовлекается нервный аппарат сердца. Наблюдается усиленное функционирование внутрисердечных и экстракардиальных нервных элементов. Однако рост нервных окончаний отстает от роста массы сократительного миокарда. Происходит истощение нервных клеток; нарушаются трофические влияния, уменьшается содержание норадреналина в миокарде, что ведет к ухудшению его сократительных свойств, затруднению мобилизации его резервов. Следовательно, нарушается и регуляторное обеспечение сердца. Гипертрофированное сердце вследствие увеличения массы его сократительного и энергообеспечивающего аппарата способно длительное время выполнять значительно большую работу, чем сердце нормальное, сохраняя при этом нормальный метаболизм. Однако способность приспосабливаться к изменяющейся нагрузке, диапазон адаптационных возможностей у гипертрофированного сердца ограничены. Уменьшен функциональный резерв. Это делает гипертрофированное сердце в силу указанной выше несбалансированности внутриклеточных и тканевых структур более ранимым при различных неблагоприятных обстоятельствах. Длительная и интенсивная нагрузка на сердечное мышечное волокно ведет к его истощению и нарушению функции. При этом могут возникнуть нарушения сократительной функции мышечного волокна вследствие нарушения образования энергии митохондриями и нарушения использования энергии сократительным аппаратом. При разных формах недостаточности сердца один из этих патологических вариантов может преобладать, в частности при длительной гиперфункции сердца ведущим является нарушение использования энергии. При этом наряду с плохой сократимостью наблюдается затруднение расслабления мышечного волокна, возникновение мышечных локальных контрактур, а в дальнейшем — дистрофия и гибель кардиомиоцитов. Повышенная нагрузка неравномерно распределяется между различными группами мышечных волокон: более интенсивно функционирующие волокна быстрее выходят из строя, гибнут и замещаются соединительной тканью (кардиосклероз), а оставшиеся принимают на себя все более повышенную нагрузку. Кардиосклероз ведет к сдавлению кардиомиоцитов, изменению механических свойств сердца, еще большему ухудшению диффузии, углублению обменных нарушений. Считается, что при замене соединительной тканью 20—30% массы сердца его нормальная работа невозможна. Дистрофические изменения сердечной мышцы сопровождаются расширением полостей сердца, снижением силы сердечных сокращений — возникает миогенная дилатация сердца, сопровождающаяся увеличением остающейся во время систолы в полостях сердца крови и переполнением вен. Повышенное давление крови в полостях правого предсердия и отверстиях полых вен прямым действием на синусно-предсердный узел и рефлекторно (рефлекс Бейнбриджа) вызывает тахикардию, которая усугубляет обменные нарушения в миокарде. Поэтому расширение полостей сердца и тахикардия служат грозными симптомами начинающейся декомпенсации. При оценке биологического значения гипертрофии миокарда следует обратить внимание на внутреннюю противоречивость данного явления. С одной стороны, это весьма совершенный приспособительный механизм, который обеспечивает длительное выполнение сердцем повышенной работы в нормальных и патологических условиях, а с другой — особенности структуры и функции гипертрофированного сердца служат предпосылкой для развития патологии. Преобладание одной из сторон в каждом конкретном случае определяет особенности протекания патологического процесса. По динамике изменений обмена, структуры и функции миокарда в компенсаторной гипертрофии сердца выделяют три основные стадии (Ф. 3. Меерсон). 1. Аварийная стадия развивается непосредственно после повышения нагрузки, характеризуется сочетанием патологических изменений в миокарде (исчезновение гликогена, снижение уровня креатинфосфата, уменьшение содержания внутриклеточного калия и повышение содержания натрия, мобилизация гликолиза, накопление лактата) с мобилизацией резервов миокарда и организма в целом. В этой стадии повышены нагрузка на единицу мышечной массы и интенсивность функционирования структуры (ИФС)-, происходит быстрое, в течение недель, увеличение массы сердца вследствие усиленного синтеза белков и утолщения мышечных волокон. 2. Стадия завершившейся гипертрофии и относительно устойчивой гиперфункции. В этой стадии процесс гипертрофии завершен, масса миокарда увеличена на 100 — 120% и больше не прибавляется, ИФС нормализовалась. Патологические изменения в обмене и структуре миокарда не выявляются, потребление кислорода, образование энергии, содержание макроэргических соединений не отличаются от нормы. Нормализовались гемодинамические показатели. Гипертрофированное сердце приспособилось к новым условиям нагрузки и в течение длительного времени компенсирует ее. 3. Стадия постепенного истощения и прогрессирующего кардиосклероза характеризуется глубокими обменными и структурными изменениями, которые исподволь накапливаются в энергообразующих и сократительных элементах клеток миокарда. Часть мышечных волокон гибнет и замещается соединительной тканью, ИФС снова возрастает. Нарушается регуляторный аппарат сердца. Прогрессирующее истощение компенсаторных резервов приводит к возникновению хронической недостаточности сердца, а в дальнейшем — к недостаточности кровообращения. Хроническая, или застойная, недостаточность сердца развивается исподволь, чаще всего вследствие метаболических нарушений в миокарде при длительной гиперфункции сердца или различных видах поражения миокарда. При этом вследствие недостаточного выброса крови из сердца уменьшается кровенаполнение органов на путях притока. Одновременно вследствие неспособности сердца перекачать всю притекающую к нему кровь развивается застой на путях оттока, т. е. в венах. Поскольку объем венозного сосудистого русла примерно в 10 раз больше объема артериального, в венах скапливается значительное количество крови. При нарушении работы преимущественно одного желудочка сердца недостаточность кровообращения приобретает некоторые специфические черты и называется соответственно недостаточностью по левожелудочковому или правожелудочковому типу. В первом случае застой крови наблюдается в венах малого круга, что может привести к отеку легких, во втором — в венах большого круга кровообращения, при этом увеличивается печень, появляются отеки на ногах, асцит. Однако нарушение сократительной функции сердца не всегда сразу ведет к развитию недостаточности кровообращения. В некоторых случаях как приспособительное явление вначале рефлекторно снижается периферическое сопротивление в артериолах большого круга кровообращения, что облегчает прохождение крови к большинству органов. Может наблюдаться рефлекторный спазм легочных артериол, в результате чего уменьшается приток крови в левое предсердие и одновременно снижается давление в системе легочных капиллярных сосудов. Последнее представляет собой механизм защиты легочных капиллярных сосудов от переполнения кровью и предупреждает развитие отека легких. Отмечается характерная последовательность вовлечения в процесс различных отделов сердца. Так, выход из строя наиболее мощного левого желудочка быстро ведет к декомпенсации левого предсердия, застою крови в малом круге кровообращения, сужению легочных артериол, развитию легочной гипертензии. Затем менее сильный правый желудочек вынужден преодолевать повышенное сопротивление в малом круге, что в итоге приводит к его декомпенсации и развитию недостаточности по правожелудочковому типу ("легочное сердце"). Гемодинамические показатели при хронической недостаточности сердца изменяются следующим образом: снижается минутный объем крови сердца (с 5 — 5,5 до 3 — 4 л/мин); в 2 — 4 раза замедляется скорость кровотока; артериальное давление меняется мало (что можно объяснить адекватным увеличением периферического сопротивления сосудов), венозное давление повышено; капиллярные сосуды и посткапиллярные вены расширены, ток крови в них замедлен, а давление повышено из-за снижения насосной функции сердца. Возникает ряд патологических изменений и со стороны других систем. Замедление кровотока в большом круге кровообращения и нарушение кровообращения в легких приводит к тому, что в крови, протекающей по сосудам, повышается количество восстановленного гемоглобина. Это придает коже и слизистой оболочке характерный синюшный цвет — цианоз. Тканям не хватает кислорода, гипоксия сопровождается накоплением недоокисленных продуктов обмена и углекислоты — развивается ацидоз. Ацидоз и гипоксия ведут к нарушению регуляции дыхания, возникает одышка. С целью компенсации гипоксии стимулируется эритроцитопоэз, увеличивается общий объем циркулирующей крови и относительное содержание клеток крови в ней, что, однако, способствует повышению вязкости крови и ухудшает ее гемодинамические свойства. Вследствие повышения давления в венозных капиллярных сосудах и ацидоза в тканях развивается отек, который, в свою очередь, усиливает гипоксию, так как при этом увеличивается диффузионный путь от капиллярного сосуда к клетке. Развитию застойного отека способствуют общие нарушения водно-электролитного обмена, сопровождающиеся задержкой в организме натрия и воды, что является еще одним примером двойственности и внутренней противоречивости механизмов компенсации при патологическом процессе. Механизмы, которые эволюционно возникли для обеспечения достаточного содержания в организме солей и жидкости при угрозе обезвоживания или кровопотере, при недостаточности сердца действуют во вред. У больных с недостаточностью кровообращения избыток потребляемой соли не выводится почками, как это свойственно здоровому человеку, а задерживается в организме вместе с эквивалентным количеством воды (вторичный альдостеронизм). Следует отметить, что длительное существование недостаточности кровообращения вследствие нарушения питания тканей в итоге ведет к глубокому и необратимому нарушению внутриклеточного метаболизма, сопровождающемуся нарушением белкового синтеза, в том числе и синтеза дыхательных ферментов, появлению гипоксии гистотоксического типа. Эти явления характерны для терминальных фаз недостаточности кровообращения. В сочетании со значительным нарушением функции пищевого канала при прогрессировании недостаточности кровообращения наступает тяжелое истощение — сердечная кахексия.
|
|||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 4734; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.012 с.) |