
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Неорганические вяжущие веществаСодержание книги
Поиск на нашем сайте Физико-химические свойства вяжущих веществ. Воздушные и гидравлические вяжущие вещества. Значение степени дисперсности. Гипсовые вяжущие вещества. Ступенчатая дегидратация двухводного сульфата кальция. Полуводный сульфат кальция. Физико-химическая природа процессов схватывания и твердения. Портландцемент, его получение и процессы, происходящие при его обжиге. Состав цементного клинкера и взаимодействие его с водой. Процессы схватывания и твердения. Основные составляющие цементного камня. Коррозия бетона и методы борьбы с ней. Взаимодействие составных частей цементного камня с водой. Сульфатная, угольно-кислотная, магнезиальная коррозия. Методы защиты бетона от коррозии. Технико-экономическое значение борьбы с коррозией бетона. Органические полимеры Получение полимеров. Реакции полимеризации. Полиэтилен, полипропилен, поливинилхлорид, полистирол. Реакции поликонденсации. Фенолформальдегидные смолы, карбамидоформальдегидные смолы, эпоксидные смолы, фурановые смолы. Кремнийорганические полимеры. Битумы и дегти. Физико-химические свойства полимеров. Особенности внутреннего строения полимеров. Пластические массы и полимербетоны, заполненные полимеры, наполнители, добавки к бетонам. Полимерные покрытия и клеи. Способы переработки пластических масс и получения элементов строительных конструкций. Стойкость и старение различных полимерных материалов в условиях длительной эксплуатации. Физиологическая активность полимерных материалов. ЛИТЕРАТУРА Основная 1. Путинский Г.П. Курс химии. – М.: Высшая школа, 1985. 2. Курс общей химии. / Под ред. Н.В. Коровина. – М.: Высшая школа, 1981. Дополнительная 1. Глинка Н.Л. Общая химия. – Л.: Химия, 1977-1983. 2. Введение в общую химию. / Под ред. Г.П. Лучинского. – М.: Высшая школа, 1980. 3. Фролов В.В. Химия. – М.: Высшая школа, 1979. 4. Харин А.Н., Катаева Н.А., Харина Л.Т. Курс химии. – М.: Высшая школа, 1983. 5. Курс химии. Ч. 2, специальная для строительных вузов. / Под ред. В.А. Киреева. – М.: Высшая школа, 1974. 6. Левант Г.Е. и Райцын Г.А. Практикум по общей химии. – М.: Высшая школа, 1978. 7. Павлов Н.Н. Теоретические основы общей химии. – М.: Высшая школа. 1978. 8. Васильева З.Г., Грановская А.А., Таперова А.А. Лабораторные работы по общей и неорганической химии. – М.: Химия, 1979. 9. Глинка Н.Л. Задачи и упражнения по общей химии. – Л.: Химия, 1985. 10. Гольбрайх З.Е. Сборник задач и упражнений по химии. – М.: Высшая школа, 1384.
КОНТРОЛЬНЫЕ ЗАДАНИЯ Каждый студент выполняет вариант контрольных заданий, обозначенный двумя последними цифрами номера студенческого билета (шифра). Например, номер студенческого билета 86594, две последние цифры 94, им соответствует вариант контрольного задания 94. КОНТРОЛЬНОЕ ЗАДАНИЕ 1 Моль. Эквиваленты и эквивалентные массы простых С 1 января 1963 г. в СССР введена Международная система единиц измерения (СИ), состоящая из шести основных единиц: метр (м) – длина, килограмм (кг) – масса, секунда (с) – время, ампер (А) – сила тока, кельвин (К) – термодинамическая температура, кандела (кд) – сила света. XIV Генеральная конференция по мерам и весам (1971) утвердила в качестве седьмой основной единицы Международной системы моль (моль) – единицу количества вещества. Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде – 12 массой 0,012 кг. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц. Моль вещества соответствует постоянной Авогадро NA = (6,022045 ± 0,000031) × 1023 моль-1 структурных элементов. При применении понятия "моль" следует указывать, какие структурные элементы имеются в виду, например, моль атомов Н, моль молекул Н2, моль протонов, моль электронов и т.п. Так, заряд моля электронов равен 6,022 × 1023 е- и отвечает количеству электричества, равному 1 фараде (F). Масса моля атомов или масса моля молекул (мольная или молярная масса), выраженная в граммах (г/моль), есть грамм-атом данного элемента или соответственно грамм-молекула данного вещества в прежнем понимании. Пример 1. Выразите в молях: а) 6,02 × 1021 молекул С02; б) 1,20 × 1024 атомов кислорода; в) 2,00 × 1023 молекул воды. Чему равна мольная (молярная) масса указанных веществ? Решение. Моль – это количество вещества, в котором содержится число частиц любого определенного сорта, равное постоянной Авогадро (6,02 × 1023). Отсюда а) 6,02 × 1021, т.е. 0,01 моль; б) 1,20 × 1024, т.е. 2 моль; в) 2,00 × 1023, т.е. 1/3 моль. Масса моля вещества выражается вкг/моль или г/моль. Мольная (молярная) масса вещества в граммах численно равна его относительной молекулярной (атомной) массе, выраженной в атомных единицах массы (а.е.м.). Так как молекулярные массы С02 и H2O и атомная масса кислорода соответственно равны 44; 18 и 16 а.е.м., то их мольные (молярные) массы равны: а) 44 г/моль; б) 18 г/моль; в) 16 г/моль. Пример 2. Определите эквивалент (Э) и эквивалентную массу mЭ азота, серы и хлора в соединениях NH3, H2S и HCl. Решение. Масса вещества и количество вещества – понятия неидентичные. Масса выражается в килограммах (граммах), а количество вещества в молях. Эквивалент элемента (Э) – это такое количество вещества, которое соединяется с 1 моль атомов водорода или замещает то же количество атомов водорода в химических реакциях. Масса 1 эквивалента элемента называется его эквивалентной массой (mЭ). Таким образом, эквиваленты выражаются в молях, а эквивалентные массы – в г/моль. В данных соединениях с 1 моль атомов водорода соединяется 1/3 моль азота, 1/2, моль серы и 1 моль хлора. Отсюда Э(N) = 1/3 моль, Э(S) = 1/2 моль, Э(Cl) = 1 моль. Исходя из мольных масс этих элементов, определяем их эквивалентные массы: mЭ(N) = 1/3 × 14 = 4,67 г/моль; mЭ(S) = 1/2 • 32 = 16 г/моль; mЭ(Cl) = 1 • 35,45 = 35,45 г/моль. Пример 3. На восстановление 7,09 г оксида двухвалентного металла требуется 2,24 л водорода (н.у.). Вычислите эквивалентную массу оксида и эквивалентную массу металла. Чему равна атомная масса металла? Нормальные условия по Международной системе единиц (СИ): давление 1,013 х 105 Па (760 мм рт. ст. =1 атм), температура 273 К или 0°С. Решение. Согласно закону эквивалентов массы (объемы) реагирующих друг с другом веществ т1 и т2 пропорциональны их эквивалентным массам (объемам): Если одно из веществ находится в газообразном состоянии, то, как правило, его количество измеряется в объемных единицах (см3, л, м3). Объем, занимаемый при данных, условиях мольной или эквивалентной массой газообразного вещества, называется мольным или, соответственно, эквивалентным объемом этого вещества. Мольный объем любого газа при н.у. равен 22,4 л. Отсюда эквивалентный объем водорода Из уравнения (3) находим эквивалентную массу оксида металла Согласно закону эквивалентов Пример 4. Сколько металла, эквивалентная масса которого 12,16 г/моль, взаимодействует с 310 см3 кислорода (н.у.)? Решение. Так как мольная (молярная) масса О2 (32 г/моль) при н.у. занимает объем 22,4 м, то объем эквивалентной массы кислорода (8 г/моль) будет 22,4: 4 = откуда mМе= 12,16 • 310/5600=0,673 г. Пример 5. Вычислите эквиваленты и эквивалентные массы H2SO4 и Аl(ОН)3 в реакциях, выраженных уравнениями: H2SO4 + КОH = KHSO4 + Н2О (1) H2SO4 + Mg = MgSO4 + Н2 (2) Аl(ОH)3+ HС1 = Аl(ОН)2С1+ Н2О (3) Аl(ОН)3+ 3HNO3 = Аl(NО3)3+ 3H2O (4) Решение. Эквивалент (эквивалентная масса) сложного вещества, как и эквивалент (эквивалентная масса) элемента, может иметь различные значения и зависит от того, в какую реакцию обмена вступает это вещество. Эквивалентная масса кислоты (основная) равна мольной массе (М), деленной на число атомов водорода, замещенных в данной реакции на металл (на число вступающих в реакцию гидроксильных групп). Следовательно, эквивалентная масса H2SO4 в реакции (1) Мн2so4=98 г/моль, а в реакции (2) Мн2so4/2 = 49 г/моль. Эквивалентная масса Аl(OH)3 в реакции (3) МAl(OH)3 = 78 г/моль, а в реакции (4) МAl(OH)3/3= 26 г/моль. Задачу можно решить и другим способом. Так как Н2S04 взаимодействует с одной эквивалентной массой КОН и двумя эквивалентными массами магния, то ее эквивалентная масса равна в реакции (1) М/1 г/моль и в реакции (2) M/2 г/моль. Аl(ОН)3 взаимодействует с одной эквивалентной массой HCl и тремя эквивалентными массами НNО3, поэтому его эквивалентная масса в реакции (3) равна М/1 г/моль, в реакции (4) M/3 г/моль. Эквиваленты H2SO4 в уравнениях (1) и (2) соответственно равны 1 моль и ½ моль; эквиваленты Аl(ОН)3 в уравнениях (3) и (4) соответственно равны 1 моль и 1/3 моль. Пример 6. Из 3,85 г нитрата металла получено 1,60 г его гидроксида. Вычислите эквивалентную массу металла (mЭМе). Решение. При решении задачи следует иметь в виду: а) эквивалент (эквивалентная масса) гидроксида равен сумме эквивалентов (эквивалентных масс) металла и гидроксильной группы; б) эквивалент (эквивалентная масса) соли равен сумме эквивалентов (эквивалентных масс) металла и кислотного остатка. Вообще эквивалент (эквивалентная масса) химического соединения равен сумме эквивалентов (эквивалентных масс) составляющих его частей. Учитывая сказанное, подставляем соответствующие данные в уравнение (1) примера 3: Пример 7. В какой массе Са(ОН)2 содержится столько же эквивалентов, сколько в 312 г А1(ОН)3? Решение. Эквивалентная масса Аl(ОН)3 равна 1/3 его мольной массы, т.е. 78/3 = 26 г/моль. Следовательно, в 312 г Аl(ОН)3 содержится 312/26 =12 эквивалентов. Эквивалентная масса Ca(OH)2 равна 1/2 его мольной массы, т.е. 37 г/моль. Отсюда 12 эквивалентов составляют 37 г/моль × 12 моль = 444 г. Пример 8. Вычислите абсолютную массу молекулы серной кислоты в граммах. Решение. Моль любого вещества (см. пример 1) содержит постоянную Авогадро NA структурных единиц (в нашем примере молекул). Мольная масса H2SO4 равна 98,0 г/моль. Следовательно, масса одной молекулы 98/(6,02 • 1023) =1,63 • 10-22 г. Контрольные вопросы 1.Определите эквивалент и эквивалентную массу фосфора, кислорода и брома в соединениях РH3, H2О, НВr. 2.В какой массе NaOH содержится столько же эквивалентов, сколько в 140 г КОН? Ответ: 100г. 3.Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите эквивалентную массу этого металла. Ответ: 32,5 г/моль. 4.Из 1,3 г гидроксида металла получается 2,85 г его сульфата. Вычислите эквивалентную массу этого металла. Ответ: 9 г/моль. 5.Оксид трехвалентного элемента содержит 31,58% кислорода. Вычислите эквивалентную, мольную и атомную массы этого элемента. 6.Чему равен при н.у. эквивалентный объем водорода? Вычислите эквивалентную массу металла, если на восстановление 1,017 г его оксида израсходовалось 0,28 л водорода (н.у.). Ответ: 32, 68 г/моль. 7.Выразите в молях: а) 6,02 • 1022 молекул C2H2; б) 1,80 • 1024 атомов азота; в) 3,01 • 1023 молекул NH3. Какова мольная масса указанных веществ? 8.Вычислите эквивалент и эквивалентную массу H3PO4 в реакциях образования: а) гидрофосфата; б) дигидрофосфата; в) ортофосфата. 9.В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите эквивалентные массы металла и его оксида. Чему равна мольная и атомная масса это го металла? 10.Чему равен при н.у. эквивалентный объем кислорода? На сжигание 1,5 г двухвалентного металла требуется 0,69 л кислорода (н.у.). Вычислите эквивалентную массу, мольную массу и атомную массу этого металла. 11.Из 3,31 г нитрата металла получается 2,78 г его хлорида, вычислите эквивалентную массу этого металла. Ответ: 103,6 г/моль. 12.Напишите уравнения реакций Fе(ОН)3 с хлороводородной (соляной) кислотой, при которых образуются следующие соединения железа: а) хлорид дигидроксожелеза; б) дихлорид гидроксожелеза; в) трихлорид железа. Вычислите эквивалент и эквивалентную массу Fе(ОН)3 в каждой из этих реакций. 13.Избытком гидроксида калия подействовали на растворы: а) дигидрофосфата калия; б) нитрата дигидроксовисмута (III), Напишите уравнения реакций этих веществ с КОН и определите их эквиваленты и эквивалентные массы. 14.В каком количестве Сr(ОН)3 содержится столько же эквивалентов, сколько в 174,96 г Мg(ОН)2? Ответ: 174 г. 15.Избытком хлороводородной (соляной) кислоты подействовали на растворы: а) гидрокарбоната кальция; б) дихлорида гидроксоалюминия. Напишите уравнения реакций этих веществ с HCl и определите их эквиваленты и эквивалентные массы. 16.При окислении 16,74 г двухвалентного металла образовалось 21,54 г оксида. Вычислите эквивалентные массы металла и его оксида. Чему равны мольная и атомная массы металла? 17.При взаимодействии 3,24 г трехвалентного металла с кислотой выделяется 4,03 л водорода (н.у.). Вычислите эквивалентную, мольную и атомную массы металла. 18.Исходя из мольной массы углерода и воды, определите абсолютную массу атома углерода и молекулы воды в граммах. Ответ: 2,0 × 10-23 г, 3,0 • 10-23 г. 19.На нейтрализацию 9,797 г ортофосфорной кислоты израсходовано 7,998 г NаОН. Вычислите эквивалент, эквивалентную массу и основность Н3РО4 в этой реакции. На основании расчета напишите уравнение реакции. Ответ: 0,5 моль, 49 г/моль, 2. 20.На нейтрализацию 0,943 г фосфористой кислоты Н3РОз израсходовано 1,291 г КОН. Вычислите эквивалент, эквивалентную массу и основность кислоты. На основании, расчета напишите уравнение реакции. Ответ: 0,5 моль, 41 г/моль, 2. Строение атома Пример 1. Что такое квантовые числа? Какие значения они могут принимать? Решение. Движение электрона в атоме носит вероятностный характер. Околоядерное пространство, в котором с наибольшей вероятностью (0,9–0,95) может находиться электрон, называется атомной орбиталью (АО). Атомная орбиталь, как любая геометрическая фигура, характеризуется тремя параметрами (координатами), получившими название квантовых чисел (n, l, ml). Квантовые числа принимают не любые, а определенные, дискретные (прерывные) значения. Соседние значения квантовых чисел различаются на единицу. Квантовые числа определяют размер (n), форму (l) и ориентацию (ml) атомной орбитали в пространстве. Занимая ту или иную атомную орбиталь, электрон образует электронное облако, которое у электронов одного и того же атома может иметь различную форму (рис. 1). Формы электронных облаков аналогичны АО. Их также называют электронными или атомными орбиталями. Электронное облако характеризуется четырьмя квантовыми числами (n, l, ml и ms). Эти квантовые числа связаны с физическими свойствами электрона, и число n (главное квантовое число) характеризует энергетический (квантовый) уровень электрона; число l (орбитальное) – момент количества движения (энергетический подуровень), число ml (магнитное) - магнитный момент, ms – спин. Спин электрона возникает за счет вращения его вокруг собственной оси. Электроны в атоме должны отличаться хотя бы одним квантовым числом (принцип Паули), поэтому в АО могут находиться не более двух электронов, отличающихся своими спинами (ms = ±1/2). В табл. 1 приведены значения и обозначения квантовых чисел, а также число электронов на соответствующем энергетическом уровне в подуровне. Таблица 1. Значения квантовых чисел и максимальное число электронов
Рис. 1. Формы s-, p- и d- электронных облаков (орбиталей) Пример 2. Составьте электронные формулы атомов элементов с порядковыми номерами 16 и 22. Покажите распределение электронов этих атомов по квантовым (энергетическим) ячейкам. Решение. Электронные формулы отображают распределение электронов в атоме по энергетическим уровням, подуровням (атомным орбиталям). Электронная конфигурация обозначается группами символов nlx, где n – главное квантовое число, l – орбитальное квантовое число (вместо него указывают соответствующее буквенное обозначение – s, p, d, f), x – число электронов в данном подуровне (орбитали). При этом следует учитывать, что электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией – меньшая сумма n+1 (правило Клечковского). Последовательность заполнения энергетических уровней и подуровней следующая: Так как число электронов в атоме того или иного элемента равно его порядковому номеру в таблице Д.И. Менделеева, то для элементов №16 (сера) и №22 (титан) электронные формулы имеют вид: Электронная структура атома может быть изображена также в виде схем размещения электронов в квантовых (энергетических) ячейках, которые являются схематическим изображением атомных орбиталей (АО). Квантовую ячейку обозначают в виде прямоугольника
Пример 3. Изотоп 101-го элемента – менделевия (256) был получен бомбардировкой a-частицами ядер атомов эйнштейния (253). Составьте уравнение этой ядерной реакции и напишите его в сокращенной форме. Решение. Превращение атомных ядер обусловливается их взаимодействием с элементарными частицами или друг с другом. Ядерные реакции связаны с изменением состава ядер атомов химических элементов. С помощью ядерных реакций можно из атомов одних элементов получить атомы других. Превращения атомных ядер как при естественной, так и при искусственной радиоактивности записывают в виде уравнений ядерных реакций. При этом следует помнить, что суммы массовых чисел (цифры, стоящие у символа элемента вверху слева) и алгебраические суммы зарядов (цифры, стоящие у символа элемента внизу слева) частиц в левой и правой частях равенства должны быть равны. Данную ядерную реакцию выражают уравнением: Часто применяют сокращенную форму записи. Для приведенной реакции она имеет вид: 253Es(a, n)256Md. В скобках на первом месте пишут бомбардирующую частицу, а на втором, через запятую, - частицу, образующуюся при данном процессе. В сокращенных уравнениях частицы Пример 4. Исходя из сокращенных уравнений ядерных реакций (табл. 2), напишите их полные уравнения. Решение. Ответ на вопрос отражен в табл. 2. Таблица 2.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-12; просмотров: 237; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.027 с.) |

 (1)
(1) (2)
(2)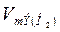 , молекула которого состоит из двух атомов, т.е. содержит два моля атомов водорода, равен 22,4: 2 =11,2 л. В формуле (2) отношение
, молекула которого состоит из двух атомов, т.е. содержит два моля атомов водорода, равен 22,4: 2 =11,2 л. В формуле (2) отношение 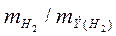 заменяем равным ему отношением
заменяем равным ему отношением  , где
, где 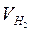 – объем водорода,
– объем водорода,  (3)
(3) :
: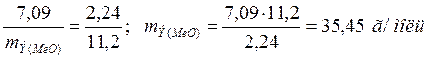
 , отсюда
, отсюда 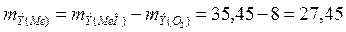 г/моль. Мольная масса металла определяется из соотношения mЭ=А/В, где тЭ – эквивалентная масса, А – мольная масса металла, В – стехиометрическая валентность элемента; А – тЭВ = 27,45 • 2 = 54,9 г/моль. Так как атомная масса в а.е.м. численно равна мольной (молярной) массе, выражаемой в г/моль, то искомая атомная масса металла 54,9 а.е.м.
г/моль. Мольная масса металла определяется из соотношения mЭ=А/В, где тЭ – эквивалентная масса, А – мольная масса металла, В – стехиометрическая валентность элемента; А – тЭВ = 27,45 • 2 = 54,9 г/моль. Так как атомная масса в а.е.м. численно равна мольной (молярной) массе, выражаемой в г/моль, то искомая атомная масса металла 54,9 а.е.м.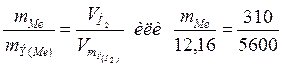 ,
, ;
;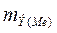 =15 г/моль
=15 г/моль

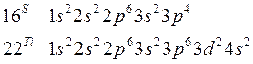
 , кружка
, кружка  или линейки
или линейки 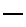 , а электроны в этих ячейках обозначают стрелками. В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами
, а электроны в этих ячейках обозначают стрелками. В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами 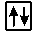 ,
,  или
или  . В данном пособии применяют прямоугольники. Орбитали данного подуровня заполняются сначала по одному электрону с одинаковыми спинами, а затем по второму электрону с противоположными спинами (правило Хунда):
. В данном пособии применяют прямоугольники. Орбитали данного подуровня заполняются сначала по одному электрону с одинаковыми спинами, а затем по второму электрону с противоположными спинами (правило Хунда):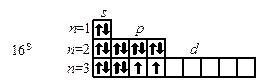


 обозначают соответственно a, p, d, n.
обозначают соответственно a, p, d, n.


