
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные законы теплового излученияСодержание книги Поиск на нашем сайте
Закон Стефана — Больцмана — закон излучения абсолютно чёрного тела. Определяет зависимость мощности излучения абсолютно чёрного тела от его температуры. Формулировка закона:
где
где Закон излучения Кирхгофа Зако́н смеще́ния Ви́на даёт зависимость длины волны, на которой поток излучения энергии чёрного тела достигает своего максимума, оттемпературы чёрного тела. λmax = b/T ≈ 0,002898 м·К × T −1 (K), где T — температура, а λmax — длина волны с максимальной интенсивностью. Коэффициент b, называемый постоянной Вина, в системе СИ имеет значение 0,002898 м·К. Для частоты света
где α ≈ 2,821439… Гц/К — постоянная величина, k — постоянная Больцмана, h — постоянная Планка, T — температура (в кельвинах). Тепловизоры — это приборы, способные видеть инфракрасное (ИК) или тепловое излучение. Те объекты, которые излучают тепло, имеют на дисплее приборов желто-оранжево-красные цвета, а все холодные объекты почти неразличимы. медицине ИК-термография выявляет опухоли и воспалительные процессы, нарушения кровообращения, травмы и даже анализирует психические процессы. 24. модель атома Томсона и Резерфорда.Теория Бора. Первая попытка создания модели атома на основе накопленных экспериментальных данных (1903 г.) принадлежитДж. Томсону. Он считал, что атом представляет собой электронейтральную систему шарообразной формы радиусом, примерно равным 10–10 м. Положительный заряд атома равномерно распределен по всему объему шара, а отрицательно заряженные электроны находятся внутри него (рис. 6.1.1). Для объяснения линейчатых спектров испускания атомов Томсон пытался определить расположение электронов в атоме и рассчитать частоты их колебаний около положений равновесия. Однако эти попытки не увенчались успехом. Через несколько лет в опытах великого английского физика Э. Резерфорда было доказано, что модель Томсона неверна. Совместно с Гансом Гейгером и Эрнстом Марсденом в 1909 году, он провел эксперимент Гейгера — Марсдена, который продемонстрировал существование ядра в атоме. Резерфорд попросил Гейгера и Марсдена в этом эксперименте искать альфа-частицы с очень большими углами отклонения, что не ожидалось от модели атома Томсона в то время. Такие отклонения, хотя и редкие, были найдены, и оказались гладкой функцией угла отклонения высокого порядка. Резерфорд смог интерпретировать эти данные, что привело его к разработке модели атома Резерфорда в 1911 году: очень маленького положительно заряженного ядра, содержащего большую часть массы атома, с обращающимися вокруг него лёгкими электронами. · Атом может находиться только в особенных стационарных, или квантовых, состояниях, каждому из которых отвечает определенная энергия. В стационарном состоянии атом не излучает электромагнитных волн. · Излучение и поглощение энергии атомом происходит при скачкообразном переходе из одного стационарного состояния в другое, при этом имеют место два соотношения:
1. Правило квантования момента импульса: 2. Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарнойорбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах:
25. классификация спектров.строение сложных атомов. Классификация спектров. Все спектры делятся на два основных класса: спектры испускания (или эмиссионные) и спектры поглощения. Каждый класс, в свою очередь, подразделяется на непрерывные (сплошные), полосатые и линейчатые спектры. Атом состоит из атомного ядра и электронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом.[1] В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам.[2][3] Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в в периодической системе и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Число Z также определяет суммарный положительный электрический заряд (Ze) атомного ядра и число электронов в нейтральном атоме, задающее его размер.[4] Атомы различного вида в разных количествах, связанные межатомными связями, образуют молекулы. 26. рентгеновское излучение:тормозное и характеристическое.рентгеновские трубки и аппараты.рентгеноструктурный анализ биологических объектов Рентгеновское излучение (синоним рентгеновские лучи) — это электромагнитное излучение с широким диапазоном длин волн (от 8·10-6 до 10-12 см). Рентгеновское излучение возникает при торможении заряженных частиц, чаще всего электронов, в электрическом поле атомов вещества. Образующиеся при этом квантырентгеновского излучения имеют различную энергию и образуют непрерывный спектр. Характеристическое излучение возникает при переходе электрона с одного внутреннего слоя на другой. Однако все внутренние слои сложных атомов полностью заполнены. Следовательно, для возникновения характеристического излучения необходимо, чтобы на каком-нибудь внутреннем слое отсутствовал электрон. Это происходит за счет выбивания электрона с какого-нибудь внутреннего слоя электроном, ускоренным в рентгеновской трубке. Характеристическое излучение имеет линейчатый спектр
Рентгенострукту́рный ана́лиз (рентгенодифракционный анализ) — один из дифракционных методов исследования структуры вещества. В основе данного метода лежит явление дифракции рентгеновских лучей на трехмерной кристаллической решётке.
Явление дифракции рентгеновских лучей на кристаллах открыл Лауэ, теоретическое обоснование явлению дали Вульф и Брэгг(условие Вульфа-Брэгга). Как метод, рентгеноструктурный анализ разработан Дебаем и Шеррером. Метод позволяет определять атомную структуру вещества, включающую в себя пространственную группу элементарной ячейки, её размеры и форму, а также определить группу симметрии кристалла. 27. люминесценция.применение в биологии и медицине. Люминесценция (лат. lumen, luminis свет) — «холодное» свечение некоторых веществ (люминофоров). Излучение света происходит при наличии в атомах избыточной энергии, в зависимости от способа сообщения которой различают фото-, электро-, хемилюминесценцию и т.д. Широко распространенный вид Л. — биолюминесценция, возникающая в результате биохимических реакций. Явление Л. широко используется в лабораторной диагностике, санитарно-биохимических и других исследованиях. В диагностической и санитарно-гигиенической практике находит применение регистрация хемилюминесценции, сопровождающей процессы пероксидного окисления липидов биологических мембран, а также генерацию активных форм кислорода фагоцитирующими клетками. Регистрация Л. позволяет получать важную информацию о физико-химических свойствах биологических объектов в норме и патологии. Молекулярные механизмы работы цепи переноса электронов в митохондриях, целых клетках и даже в тканях изучают по изменению синей (440 нм) флюоресценции восстановленных пиридиннуклеотидов, возбуждаемой при 365 нм. При изучении структуры нуклеиновых кислот применяют акридиновый оранжевый и другие зонды. При этом определение положения максимума Л. в спектре позволяет судить о структуре нуклеиновой кислоты. Так, максимум Л. акридинового оранжевого и двуспиральной нативной ДНК располагается в зеленой области спектра (530 нм), тогда как в одноцепочечной ДНК и РНК он смещается в красную область (640 нм). Микрофлюориметрически с помощью зондов анализируют ДНК непосредственно в клетках. В медицинской технике распространение получили неорганические люминофоры — вещества, способные к фото-, рентгенофлюоресценции и т.д. Люминофоры используются в люминесцентных лампах. При изготовлении рентгеновских экранов применяют цинккадмийсульфидные люминофоры, способные к рентгенолюминесценции. 28. индуцированное излучение.оптические квантовые генераторы.применение лазеров в стоматологии. Вы́нужденное излуче́ние, индуци́рованное излучение — генерация нового фотона при переходе квантовой системы (атома, молекулы, ядра и т. д.) из возбуждённого в стабильное состояние (меньшийэнергетический уровень) под воздействием индуцирующего фотона, энергия которого была равна разности энергий уровней. Созданный фотон имеет ту же энергию, импульс, фазу и поляризацию, что и индуцирующий фотон (который при этом не поглощается). Оба фотона являются когерентными. Большой вклад в разработку вопроса о вынужденном излучении (испускании) внес А. Эйнштейн. Гипотеза Эйнштейна состоит в том, что под действием электромагнитного поля частоты ω молекула (атом) может: · перейти с более низкого энергетического уровня · перейти с более высокого энергетического уровня · кроме того, как и в отсутствие возбуждающего поля, остаётся возможным самопроизвольный переход молекулы (атома) с верхнего на нижний уровень с испусканием фотона энергией Лазеры — оптические квантовые генераторы луч лазера — это высокоточный бесконтактный, бескровный, стерильный и бактерицидный хирургический инструмент, позволяющий значительно сократить процесс послеоперационного заживления. I. Кариесология II. Эндодонтия. Эктомия пульпы — моментальное выпаривание пульпы III. Имплантология. Раскрытие импланта бескровным методом IV. Ортодонтия. V. Заболевания слизистой оболочки полости рта. VI. Пародонтология VII. Ортопедия 29.строение атомного ядра.свойства ядерных сил.энергии связи ядра. Атомное ядро состоит из нуклонов — положительно заряженных протонов и нейтральныхнейтронов, которые связаны между собой при помощи сильного взаимодействия. Протон и нейтрон обладают собственным моментом количества движения (спином), равным Атомное ядро, рассматриваемое как класс частиц с определённым числом протонов и нейтронов, принято называть нуклидом.
Количество протонов в ядре называется его зарядовым числом Экспериментально было обнаружено, что для всех стабильных ядер масса ядра меньше суммы масс составляющих его нуклонов, взятых по отдельности. Эта разница называется дефектом массы или избытком массы и определяется соотношением:
где Согласно принципу эквивалентности массы и энергии дефект массы представляет собой массу, эквивалентную работе, затраченной ядерными силами, чтобы собрать все нуклоны вместе при образовании ядра. Эта величина равна изменениюпотенциальной энергии нуклонов в результате их объединения в ядро. Энергия, эквивалентная дефекту массы, называется энергией связи ядра и равна:
где Другим важным параметром ядра является энергия связи, приходящаяся на один нуклон ядра, которую можно вычислить, разделив энергию связи ядра на число содержащихся в нём нуклонов:
Ядерные силы — это силы, удерживающие нуклоны в ядре, представляющие собой большие силы притяжения, действующие только на малых расстояниях. Они обладают свойствами насыщения, в связи с чем ядерным силам приписывается обменный характер (с помощью пи-мезонов). Ядерные силы зависят от спина, не зависят от электрического заряда и не являются центральными силами 30. радиоактивность.закон радиоактивного распада. Закон радиоактивного распада — физический закон, описывающий зависимость интенсивности радиоактивного распада от времени и количества радиоактивных атомов в образце Естественной радиоактивностью называется самопроизвольное превращение ядер неустойчивых изотопов одного химического элемента в ядра изотопов других химических элементов. Радиоактивность впервые обнаружена А. Беккерелем у солей урана. Естественная радиоактивность, как правило, наблюдается у ядер тяжелых элементов, располагающихся в таблице Менделеева за свинцом. Существуют и легкие радиоактивные ядра Скорость распада различных радиоактивных элементов неодинакова и характеризуется периодом полураспада. Период полураспада — это промежуток времени Т, в течение которого распадается половина первоначального количества ядер (рис. 22.2).
Рис. 22.2 Если в начальный момент времени t0=0 было N0 радиоактивных ядер, то через промежуток времени, равный периоду полураспада t1=T, число нераспавшихся ядер
31. ионизирующее излучение.дозиметрия.защита о ионизирующих излучений.биологические основы действия ионизирующего излучения а организм. Ионизи́рующее излуче́ние — в самом общем смысле — различные виды микрочастиц и физическихполей, способные ионизировать вещество Дози́метр — прибор для измерения эффективной дозы или мощности ионизирующего излучения за некоторый промежуток времени. Само измерение называетсядозиметрией. Ионизация, создаваемая излучением в клетках, приводит к образованию свободных радикалов. Свободные радикалы вызывают разрушения целостности цепочек макромолекул (белков и нуклеиновых кислот), что может привести как к массовой гибели клеток, так и канцерогенезу и мутагенезу. Наиболее подвержены воздействию ионизирующего излучения активно делящиеся (эпителиальные, стволовые, также эмбриональные) клетки. В медицине Для получения картины внутренних органов и скелета используют рентгенография, рентгеноскопия, компьютерная томография. Для лечения опухолей и других патологических очагов используют лучевую терапию: облучение гамма-квантами, рентгеном, электронами, тяжёлыми ядерными частицами, такими как протоны, тяжёлые ионы, отрицательные π-мезоны и нейтроныразных энергий. Введение в организм радиофармацевтических препаратов, как с лечебными, так и с диагностическими целями. 32. применение радиоактивных изотопов в медицине.метод меченых атомов. Примение изотопов Одним из наиболее выдающихся исследований, проведенных с помощью «меченых атомов», явилось исследование обмена веществ в организмах. Было доказано, что за сравнительно небольшое время организм подвергается почти полному обновлению. Слагающие его атомы заменяются новыми. Лишь железо, как показали опыты по изотопному исследованию крови, является исключением из этого правила. Железо входит в состав гемоглобина красных кровяных шариков. При введении в пищу радиоактивных атомов железа было установлено, что свободный кислород, выделяемый при фотосинтезе, первоначально входил в состав воды, а не углекислого газа. Радиоактивные изотопы применяются в медицине как для постановки диагноза, так и для терапевтических целей. Радиоактивный натрий, вводимый в небольших количествах в кровь, используется для исследования кровообращения, йод интенсивно отлагается в щитовидной железе, особенно при базедовой болезни. Наблюдая с помощью счетчика за отложением радиоактивного йода, можно быстро поставить диагноз. Большие дозы радиоактивного йода вызывают частичное разрушение аномально развивающихся тканей, и поэтому радиоактивный йод используют для лечения базедовой болезни. Интенсивное гамма-излучение кобальта используется при лечении раковых заболеваний (кобальтовая пушка). Не менее обширны применения радиоактивных изотопов в промышленности. Одним из примеров этого может служить следующий способ контроля износа поршневых колец в двигателях внутреннего сгорания. Облучая поршневое кольцо нейтронами, вызывают в нем ядерные реакции и делают его радиоактивным меченые атомы (изотопные индикаторы) содержат изотопы, которые по своим свойствам (радиоактивности, атомной массе) отличаются от других изотопов данного элемента. В ходе эксперимента радиоактивные атомы распадаются. Распад данного атома представляет собой случайное событие; число распадов в секунду пропорционально числу радиоактивных атомов, существующих в настоящий момент. В аналитической форме сказанное записывается в виде dN/dt = -N; (1) где N — число радиоактивных атомов, существующих в данное время, t — время, N, — постоянная, характерная для выбранного изотопа. Интегрируя уравнение (1), получаем N = N0e-t (2) где N0 — число.радиоактивных атомов в начальный момент. Из формулы (2) может быть определено время т, за которое число N уменьшается вдвое: = ln2/ (3) Время называют периодом полураспада элемента. В течение каждого периода полураспада число атомов изотопа уменьшается в два раза.
|
|||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 332; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.255.103 (0.01 с.) |


 - степень черноты (для всех веществ
- степень черноты (для всех веществ  , для абсолютно черного тела
, для абсолютно черного тела  ). При помощи закона Планка для излучения, постоянную
). При помощи закона Планка для излучения, постоянную 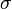 можно определить как
можно определить как
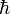 — постоянная Планка,
— постоянная Планка, 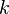 — постоянная Больцмана,
— постоянная Больцмана,  — скорость света.
— скорость света.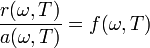
 (в герцах) закон смещения Вина имеет вид:
(в герцах) закон смещения Вина имеет вид:


 (модель атома Бора)
(модель атома Бора)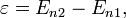 где
где  — излучённая (поглощённая) энергия,
— излучённая (поглощённая) энергия, 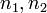 — номера квантовых состояний. В спектроскопии
— номера квантовых состояний. В спектроскопии  и
и  называются термами.
называются термами.


 м — боровский радиус.
м — боровский радиус.
 — энергетическая постоянная Ридберга (численно равна 13,6 эВ).
— энергетическая постоянная Ридберга (численно равна 13,6 эВ). Схема рентгеновской трубки для структурного анализа: 1 - металлический стакан анода (обычно заземляется); 2 - бериллиевые окна для выхода рентгеновского излучения; 3 - термоэмиссионный катод; 4 - стеклянная колба; 5 - выводы катода, к которым подводится напряжение накала, а также высокое (относительно анода) напряжение; 6 - электростатическая система фокусировки электронов; 7 - анод; 8 - патрубки для подсоединения системы охлаждении
Схема рентгеновской трубки для структурного анализа: 1 - металлический стакан анода (обычно заземляется); 2 - бериллиевые окна для выхода рентгеновского излучения; 3 - термоэмиссионный катод; 4 - стеклянная колба; 5 - выводы катода, к которым подводится напряжение накала, а также высокое (относительно анода) напряжение; 6 - электростатическая система фокусировки электронов; 7 - анод; 8 - патрубки для подсоединения системы охлаждении на более высокий
на более высокий  с поглощением фотона энергией
с поглощением фотона энергией 
 [сн 1] и связанным с ним магнитным моментом.
[сн 1] и связанным с ним магнитным моментом. — это число равно порядковому номеру элемента, к которому относится атом, в таблице Менделеева. Количество протонов в ядре определяет структуру электронной оболочки нейтрального атома и, таким образом, химические свойства соответствующего элемента. Количество нейтронов в ядре называется его изотопическим числом
— это число равно порядковому номеру элемента, к которому относится атом, в таблице Менделеева. Количество протонов в ядре определяет структуру электронной оболочки нейтрального атома и, таким образом, химические свойства соответствующего элемента. Количество нейтронов в ядре называется его изотопическим числом 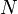 . Ядра с одинаковым числом протонов и разным числом нейтронов называются изотопами. Ядра с одинаковым числом нейтронов, но разным числом протонов — называются изотонами. Термины изотоп и изотон используются также применительно к атомам, содержащим указанные ядра, а также для характеристики нехимических разновидностей одного химического элемента. Полное количество нуклонов в ядре называется его массовым числом
. Ядра с одинаковым числом протонов и разным числом нейтронов называются изотопами. Ядра с одинаковым числом нейтронов, но разным числом протонов — называются изотонами. Термины изотоп и изотон используются также применительно к атомам, содержащим указанные ядра, а также для характеристики нехимических разновидностей одного химического элемента. Полное количество нуклонов в ядре называется его массовым числом  (
( ) и приблизительно равно средней массе атома, указанной в таблице Менделеева. Нуклиды с одинаковым массовым числом, но разным протон-нейтронным составом принято называтьизобарами. Большая энергия связи нуклонов, входящих в ядро, говорит о существовании ядерных сил, поскольку известные гравитационные силы слишком малы, чтобы преодолеть взаимное электростатическое отталкиваниепротонов в ядре. Связь нуклонов осуществляется чрезвычайно короткоживущими силами, которые возникают вследствие непрерывного обмена частицами, называемыми пи-мезонами, между нуклонами в ядре.
) и приблизительно равно средней массе атома, указанной в таблице Менделеева. Нуклиды с одинаковым массовым числом, но разным протон-нейтронным составом принято называтьизобарами. Большая энергия связи нуклонов, входящих в ядро, говорит о существовании ядерных сил, поскольку известные гравитационные силы слишком малы, чтобы преодолеть взаимное электростатическое отталкиваниепротонов в ядре. Связь нуклонов осуществляется чрезвычайно короткоживущими силами, которые возникают вследствие непрерывного обмена частицами, называемыми пи-мезонами, между нуклонами в ядре. ,
, и
и  — массы свободного протона и нейтрона,
— массы свободного протона и нейтрона,  — масса ядра.
— масса ядра. ,
,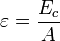




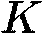







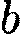 и др.
и др.




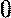

 Спустя еще такой же промежуток времени t2=2T числонераспавшихся ядер
Спустя еще такой же промежуток времени t2=2T числонераспавшихся ядер 













