
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Квантово-механическое описание атома водородаСодержание книги
Поиск на нашем сайте
· Стационарное уравнение Шредингера для атома водорода:
· Физический смысл квантовых чисел: - главное квантовое число
- наиболее вероятное удаление электрона от ядра в возбужденном атоме возрастает пропорционально
· Орбитальное (азимутальное) квантовое число
Обычно
Из формулы связи орбитальных механического и магнитного моментов (
где - правило отбора для квантового числа · магнитное (орбитальное магнитное) квантовое число
где Из квантования проекции орбитального механического моментаследует квантованиепроекции орбитального магнитного момента
· Спиновое и магнитное спиновые числа: - спиновое кантовое число
- модуль собственного магнитного момента электрона:
- спиновое магнитное квантовое число
- проекция магнитного спинового момента принимает два значения:
· Квантовое число суммарного спин-орбитального момента
суммарный момент
Кратность вырождения состояний в атоме водорода с учетом спина
Основные положения построения таблицы Д.И.Менделеева 1.Распределение электронов по уровням энергии происходит в соответствии с принципом Паули. 2.Энергетическое состояние в отсутствие внешних полей зависит от квантовых чисел 3.При увеличении порядкового номера химического элемента
4.Наиболее удаленные от ядра электроны наименее связаны с ядром, поэтому химические свойства элементов зависят от числа и состояния валентных электронов. Совокупность электронов с одним и тем же числом
Совокупность электронов с одним и тем же числом Максимальное число электронов в оболочках и подоболочках
Глава 10. Основы теории конденсированных сред Внутренняя энергия молекулы · Внутреннюю энергию молекулыможно представить суммой
где
где
где момент импульса может принимать только дискретные значения
где
Резонансное поглощение · Ширина энергетического уровня( · Естественная (или Лоренцова) ширина спектральной линии поглощения:
Статистические свойства носителей заряда в твердых телах.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 970; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.119.149 (0.007 с.) |

 .
. :
: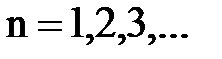 ;
;  ;
; :
: .
. :
: ;
;  определяет орбитальный механический момент импульса
определяет орбитальный механический момент импульса .
.  - состояния обозначаются буквами:
- состояния обозначаются буквами: ) следует квантование орбитального магнитного момента:
) следует квантование орбитального магнитного момента: ,
, - магнетон Бора,
- магнетон Бора,  - масса электрона;
- масса электрона;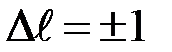 .
. :
: ;
;  ,
, - проекция момента импульса на произвольно выбранную ось.
- проекция момента импульса на произвольно выбранную ось.
 : для электрона
: для электрона  ;
;  ;
; ,
,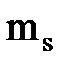 ; для электрона
; для электрона  ;
;  ,
, ,
, ;
; .
. .
. и
и  и, в меньшей степени, от квантовых чисел
и, в меньшей степени, от квантовых чисел  и
и  , следовательно, вырождение уровней снимается.
, следовательно, вырождение уровней снимается. происходит последовательное заполнение электронами данного уровня (определяемого числами
происходит последовательное заполнение электронами данного уровня (определяемого числами  , называется оболочкой(слоем),в которой может содержаться
, называется оболочкой(слоем),в которой может содержаться 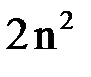 электронов. Оболочки с разными
электронов. Оболочки с разными 
 , называется подоболочкой;максимальное количество электронов в ней
, называется подоболочкой;максимальное количество электронов в ней  .
.
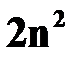





 ,
, - энергия электронного взаимодействия, зависящая от конфигурации электронной оболочки,
- энергия электронного взаимодействия, зависящая от конфигурации электронной оболочки,  ;
;  - энергия связи молекулы;
- энергия связи молекулы; - энергия колебательного движения ядер; при малых отклонениях ядер атомов от положения равновесия описывается соотношением для гармонического осциллятора
- энергия колебательного движения ядер; при малых отклонениях ядер атомов от положения равновесия описывается соотношением для гармонического осциллятора ,
, - колебательное квантовое число;
- колебательное квантовое число;  - частота колебаний;
- частота колебаний; - энергия вращательного движения
- энергия вращательного движения  ,
, - момент инерции молекулы относительно оси, проходящей через центр ее масс;
- момент инерции молекулы относительно оси, проходящей через центр ее масс;  - угловая скорость вращения;
- угловая скорость вращения;  - момент импульса молекулы;
- момент импульса молекулы; ,
, - вращательное квантовое число.
- вращательное квантовое число. ):
):  .
. или
или 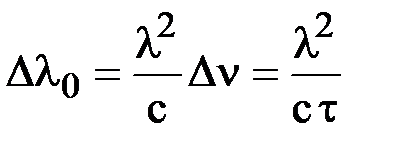 .
.


