
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Какое количество теплоты выделится при окислении 800 г глюкозы?Содержание книги
Поиск на нашем сайте
Н Н DН обр.(С2Н6) = 2DНатомиз + 3DНатомиз-Ес-с - 6Е с-н Ø РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
Решение Q р-ции = Qобр.прод. – Q обр. реаг. = Q обр. Са(ОН)2 – (Q обр.СаО + Q обр. Н2О) = 986,8 – (635,7 + 285,8) = 65,3 кДЖ/моль Ответ. 65,3 кДж/моль.
С6Н12О6 (тв.) + 6О2 (г.) = 6СО2 (г.) + 6Н2О (ж.), Н = –2803 кДж. Какое количество теплоты выделится при окислении 800 г глюкозы? Решение
Ответ. 12 458 кДж.
3. Определите количество теплоты, которое выделится при образовании 120 г MgO в результате реакции горения магния, с помощью термохимического уравнения. 2 Mg + O2 = 2MgO + 1204 кДж Решение 1) Определяем количества оксида магния, используя формулу для нахождения количества вещества через массу. ν = m / M
ν(MgO) = 120г: 40 г/моль = 3 моль
2) Составляем пропорцию с учетом коэффициентов в уравнении реакции
По уравнению 2 моль MgO - 1204 кДж
По условию 3 моль MgO - Q Отсюда Q= (3 * 1204):2 = 1803кДж Ответ: При образовании 120г оксида магния выделится 1803 кДж энергии.
В результате реакции, термохимическое уравнение которой 2 C2H2+ 5O2 = 4CO2 +2H2O + 2610 кДж выделилось 652,5 кДж теплоты. Определите массу сгоревшего ацетилена. Решение 1) Установим пропорциональные отношения между количеством вещества ацетилена и количеством теплоты.
По уравнению 2 моль C2H2 ---------- 2610 кДж
По условию х моль ---------- 652,5 кДж
Решаем пропорцию х=(2 * 652,5):2610 2) Определяем массу ацетилена по формуле m= n * M
m = 0,5 моль * 26 г/моль = 13 г. Ответ: масса сгоревшего ацетилена 13 г.
В результате горения 48 г метана выделилось 2406 кДж теплоты. Составьте термохимическое уравнение этой реакции. Решение 1. Запишем уравнение реакции горения метана в общем виде CH4 + 2O2 = CO2 +2H2O + Q
2. Определим количество 48 г метана
ν = m / M
ν(CH4) = 48г: 16 г/моль = 3 моль
3. Составляем пропорцию с учетом коэффициентов в уравнении реакции
По условию 3моль CH4 - 2406 кДж
По уравнению 1 моль CH4 - Q
Решаем пропорцию Q=(1*2406):3=802кДж
Ответ: термохимическое уравнение реакции горения метана CH4+ 2O2 = CO2 +2H2O + 802 кДж
6. Рассчитайте тепловой эффект реакции: 4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(ж), если ΔH0обр NH3(г) и H2O(ж) равны соответственно -286 и -46 кДж/моль. Решение 1. O2 и N2 – простые вещества, следовательно тепловой эффект образования их равен нулю. 2. Согласно следствию из закона Гесса, тепловой эффект реакции равен разности между суммами теплот образования продуктов реакции и теплот образования исходных веществ с учетом стехиометрических коэффициентов: ΔH0 = 6·(-286) – 4·(-46)=-1532 кДж. 2. Термохимическое уравнение будет иметь вид 3. 4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(ж)+1532 кДж Ответ: в результате данной реакции выделится 1532 кДж.
Определить тепловой эффект реакции гидролиза нитрида магния Mg3N2(тв.) + 6H2O(ж.) = 3Mg(OH)2(тв.) + 2NH3(г.). Решение DH = DHобр.прод. – DHобр.исх. Используя справочные данные, находим теплоты образования продуктов и исходных веществ: DH обр. (Mg3N2(тв.)) = –461,5 кДж/моль; DH обр. (Mg(OH)2(тв.)) = –924,66 кДж/моль; DH обр. (H2O(ж.) = –285,77 кДж/моль; DH обр. (NH3(г.) = –46,19 кДж/моль; Отсюда DH0 = [3×(–924,66) + 2×(–46,19)] – [–461,5 + 6×(–285,77)] == –689,86 кДж/моль.
8. Вычислить стандартную энтальпию реакции: 2C2H5OH(жидк.) = C2H5OC2H5(жидк.) + H2O(жидк.) по значениям стандартных энтальпий сгорания веществ: DH0сгор. C2H5OH = -1368 кДж/моль; DH0сгор. C2H5OC2H5 = -2727 кДж/моль. Решение Запишем выражение второго следствия из закона Гесса с учетом того, что стандартная энтальпия сгорания воды равна нулю:
Подставим значения стандартных энтальпий сгорания веществ, участвующих в реакции: Ответ:
При сгорании некоторого количества газообразного углеводорода образовалось 4,48 л оксида углерода (IV) (н.у.) и 3,6 г воды и выделилось 137,5 кДж теплоты. Определите теплоту сгорания углеводорода, если известно, что его плотность по воздуху равна 1,448. Решение 1) Определяем простейшую формулу сгоревшего углеводорода: С х Н у + О2 → х СО2 + 0,5у Н2О ν(СО2) = 4,48 / 22,4 = 0,2 моль; ν(Н2О) = 3,6/ 18 = 0,2 моль. ν(С) = 0,2 моль; ν(Н) = 0,2 · 2 = 0,4 моль. х: у = 0,2: 0,4 = 1: 2. Простейшая формула углеводорода СН2. 2) Рассчитываем молярную массу и определяем молекулярную формулу углеводорода: М(С х Н у) = Dвоздух · 29 = 1,448 · 29 = 42 г/моль. М(фрагмента СН2) = 14 г/моль Молекулярная формула углеводорода (СН2) n: n = М(СхНу) / М(фрагмента СН2) = 42 / 14 = 3. Углеводород (СН2)3 или С3Н6. 3) Записываем термохимическое уравнение реакции горения углеводорода и определяем теплоту сгорания: С3Н6(газ) + 4,5 О2(газ) → 3 СО2(газ) + 3 Н2О(ж) + Q(сгорания) ν(С3Н6) =ν(СО2) / 3 = 0,2 / 3 = 0,0667 моль. Q(сгорания С2Н6) = Q / ν(С2Н6) = 137,5 / 0,0667 = 2061 кДж/моль. Ответ: Q(сгорания С2Н6) = 2061 кДж/моль.
При сжигании 9 г органического вещества образовалось 13,2 г оксида углерода(IV) и 5,4 г воды и выделилось 140 кДж теплоты. Определите молекулярную формулу вещества, если его теплота сгорания равна 2800 кДж/моль. Решение 1) Судя по продуктам сгорания исходное вещество содержало углерод, водород и,возможно, кислород. Рассчитываем количества образовавшихся веществ, и записываем схему горения: ν(СО2) = 13,2 / 44 = 0,3 моль. ν(Н2О) = 5,4 / 18 = 0,3 моль. С х Н у О z + О2 →СО2 + Н2О 2) Рассчитываем количества веществ элементов, входящих в состав исходного вещества и определяем его простейшую формулу: ν(С) = ν(СО2) = 0,3 моль. ν(Н) = 2 · ν(Н2О) = 0,3 · 2 = 0,6 моль. m(O) = m(вещества) – m(С) – m(Н) = 9 – 0,3 · 12 – 0,6 · 1 = 4,8 г. ν(О) = 4,8 / 16 = 0,3 моль. х: у: z = 0,3: 0,6: 0,3 = 1: 2: 1. Простейшая формула вещества СН2О. 3) Определяем молярную массу вещества и его молекулярную формулу: ν(исходного вещества) = Q(выделившееся при сгорании взятого количества): Q(сгорания) = 140 / 2800 = 0,05 моль. М(исходного вещества) = 9 / 0,05 = 180 г/моль. Молекулярная формула (СН2О) n; n = 180 / 30 = 6. С6Н12О6. Ответ: С6Н12О6. Ø ТЕСТЫ ПО ТЕМЕ: «ОСНОВЫ ТЕРМОХИМИИ. ТЕПЛОВЫЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ».
Тест 1 1. При стандартных условиях теплота образования равна 0 для: а) водорода; б) воды; в) пероксида водорода; г) алюминия. 2. Реакция, уравнение которой N2 + O2 = 2NO – Q, относится к реакциям: а) эндотермического соединения; б) экзотермического соединения; в) эндотермического разложения; г) экзотермического разложения. Ключ к тесту 1 2 3 4 5 6 7 8 9 10 А, г а г б в а, в г в а б Тест 2 1. При стандартных условиях теплота образования равна 0 для: а)углекислого газа;б) железа;в) пероксида водорода; г) кислорода. 2. Реакция, уравнение которой N2 + 3Н2 = 2NН3 + Q, относится к реакциям: а) эндотермического соединения; б) экзотермического соединения; в) эндотермического разложения; г) экзотермического разложения. 3. При соединении 11,16 г железа с серой выделилось 20,06 кДж теплоты. Определить теплоту образования сульфида железа. а) 838; б) 100; в) 364,6; г) 419. 4. Эндотермической является реакция: а) горения водорода; б) разложения воды; в) горения углерода; г) горения метана. 5. Известны тепловые эффекты следующих процессов: 2С2Н2 (г.) + 5О2 (г.) = 4СО (г.) + 2Н2О (ж.) + 2600 кДж, Н2О (ж.) = Н2О (г.) – 40 кДж. Какую массу воды (в г), находящейся при температуре кипения, можно испарить за счет теплоты, полученной при полном сгорании 89,6 л (н.у.) ацетилена? а) 72; б) 1170; в) 2340; г) 4680. 6. Какое определение неверно для данной реакции: СaCO3 а) гомогенная; б) эндотермическая; в) реакция соединения; г) окислительно-восстановительная. 7. Вычислить теплоту реакции получения гидроксида кальция из оксида кальция и воды, если теплота образования оксида кальция равна +635,7 кДж/моль, теплота образования воды равна +285,8 кДж/моль, а теплота образования гидроксида кальция равна +986,8 кДж/моль. а) 65,3; б) 786; в) 503; г) 393. 8. Дано термохимическое уравнение:2SO2 + O2 = 2SO3 + 198 кДж. В результате реакции выделилось 495 кДж теплоты. Какая масса (в г) сернистого газа прореагировала с кислородом? а) 160; б) 640; в) 320; г) 320. 9. Термохимическое уравнение реакции горения метана имеет вид:СН4 (г.) + 2О2 (г.) = СО2 (г.) + 2Н2О (г.), 1) 23 2) 46 3) 92 4) 184
Моль HCl, равно
1) 184,6 кДж 2) 276,9 кДж 3) 369,2 кДж 4) 461,5 кДж
26. Теплота образования 1 моль оксида магния из простых веществ составляет 600 кДж. Объем кислорода (н.у.), затраченный для получения 2400 кДж теплоты, равен
1) 11,2 л 2) 22,4 л 3) 33,6 л 4) 44,8 л
27. Теплота образования оксида алюминия равна 1676 кДж/моль. Определите тепловой эффект реакции, в которой при взаимодействии алюминия с кислородом получено 25,5 г Al2O3.
1) 140 кДж 2) 209,5 кДж 3) 419 кДж 4) 838 кДж
Ответы: 1-2, 2-4, 3-1, 4-4, 5-3, 6-2, 7-1, 8-3, 9-1, 10-4, 11-4, 12-2, 13-3, 14-3, 15-2, 16-3, 17-1, 18-3, 19-3, 20-1, 21-2, 22-2, 23-4, 24-1, 25-3, 26-4, 27-3, 28-1, 29-1, 30-2, 31-3.
Источники информации:
2. http://himekoscho.ucoz.ru/load/termokhimicheskie_uravnenija/27-1-0-130
3. http://maratakm.narod.ru
4. http://www.hemi.nsu.ru/text211.htm
5. Енякова Т.М.,Кардычко Ю.С. "Алгоритмы как инструмент дифференцированного подхода к учащимся" Журнал "Химия в школе" №1,2004
6. Новоженов В.А. «Введение в неорганическую химию» Барнаул. Изд-во. Алт.унив-та., 2001
Н Н DН обр.(С2Н6) = 2DНатомиз + 3DНатомиз-Ес-с - 6Е с-н Ø РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
Решение Q р-ции = Qобр.прод. – Q обр. реаг. = Q обр. Са(ОН)2 – (Q обр.СаО + Q обр. Н2О) = 986,8 – (635,7 + 285,8) = 65,3 кДЖ/моль Ответ. 65,3 кДж/моль.
С6Н12О6 (тв.) + 6О2 (г.) = 6СО2 (г.) + 6Н2О (ж.), Н = –2803 кДж. Какое количество теплоты выделится при окислении 800 г глюкозы? Решение
Ответ. 12 458 кДж.
3. Определите количество теплоты, которое выделится при образовании 120 г MgO в результате реакции горения магния, с помощью термохимического уравнения. 2 Mg + O2 = 2MgO + 1204 кДж Решение 1) Определяем количества оксида магния, используя формулу для нахождения количества вещества через массу. ν = m / M
ν(MgO) = 120г: 40 г/моль = 3 моль
2) Составляем пропорцию с учетом коэффициентов в уравнении реакции
По уравнению 2 моль MgO - 1204 кДж
По условию 3 моль MgO - Q Отсюда Q= (3 * 1204):2 = 1803кДж Ответ: При образовании 120г оксида магния выделится 1803 кДж энергии.
|
||||
|
Последнее изменение этой страницы: 2016-04-25; просмотров: 3839; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.007 с.) |

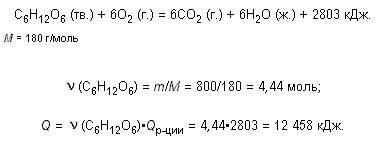
 = 2×
= 2× 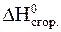 C2H5OH -
C2H5OH - 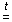 CaO + CO2 – Q.?
CaO + CO2 – Q.?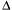 Н = –802,2 кДж.
Н = –802,2 кДж.


