Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сегмент 14. Белки – структурно-функциональная основа жизни
Как уже отмечено в сегменте 7, белки представляют полимерные молекулы длиной в 50-100-500 и более мономеров - аминокислот. Имеется 20 разновидностей аминокислот, различных по химическим свойствам их свободных концов - радикалов. Особо выделим аминокислоты со свободным электрическим зарядом. Так, аспарагиновая и глутаминовая кислоты имеют отрицательный заряд (лишняя –СОО- группа), аргинин, лизин, аспарагин и глутамин - положительный (лишняя –NH+ группа). Некоторые аминокислоты имеют свободную гидроксильную группу (–OH). В совокупности активные группы придают молекуле белка электрический заряд - положительный или отрицательный в зависимости от соотношения аминокислот с разными зарядами. Кроме того, такие аминокислоты как цистеин и метионин имеют на свободном конце серу (группа –SH или –SCH 3) и могут формировать между собой -S-S- мостики, стягивая участок полипептидной цепи в петлю. Эти и другие особенности белковой молекулы, которые целиком зависят от набора и порядка чередования аминокислот (то есть от ее первичной структуры), придают каждой молекуле в водном окружении неповторимую вторичную и третичную (трехмерную) структуру. В каждой белковой молекуле в строго определенных местах есть активные участки, нередко содержащие какой-нибудь металл (железо - Fe, магний - Mg, медь -Cu и др.) или другие специфические соединения. Эти участки обычно и отвечают за особые функции белков. Важнейшее свойство белковой молекулы, объясняющее механизм ее функционирования, это - способность обратимо изменять свою третичную структуру (трехмерную форму) в ответ на какое-либо раздражение. Раздражителем чаще всего выступает энергетический разряд от расщепления молекулы АТФ. Такая обратимая денатурация, или конформационная перестройка, и есть совершаемая молекулой работа. Конформационная перестройка молекулы подобна циклу сжатия и расслабления пружины: при внешнем давлении пружина сжимается и приобретает внутренний запас энергии, а на обратном ходу совершает работу. В зависимости от структуры белковой молекулы и ее местонахождения совершаемая работа, то есть функция, будет различна. Ниже будет показана роль белков в реализации основных жизненных функции: опорно-двигательной, транспортной, каталитической, защитной, сигнальной.
Обычно называют еще энергетическую функцию белков. Действительно, белки в своей химической структуре несут большой запас энергии. Они могут распадаться на отдельные аминокислоты, которые, в свою очередь, подобно глюкозе окисляются в митохондриях до углекислого газа и воды и отдают энергию на синтез АТФ. Однако этот путь в энергетическом обмене используется как резервный, в тех случаях, когда исчерпаны запасы углеводов и жиров - основных энергоемких субстратов. Использование белков в энергообмене расточительно для клетки, так как аминокислоты представляют дефицитный продукт, многие из них вообще не могут синтезироваться у животных, а получаются от растительных продуктов (незаменимые аминокислоты). Белки имеют уникальную структуру, которой дано более высокое предназначение. В этом смысле расщеплять белки для извлечения энергии - все равно, что топить печь ассигнациями. Кроме того, аминокислоты предварительно необходимо освободить от азота (дезаминировать), чтобы уровнять их с продуктами полураспада глюкозы, а это и дополнительная работа и потеря важнейшего элемента из организма (азот в составе простых соединений выводится с мочой). Таким образом, белки в энергетическом обмене используются в крайних случаях - при голодании, болезни, возрастных метаморфозах. Основные же функции белков, перечисленные выше и рассматриваемые ниже, значительно более важны и изящны, поскольку в их реализации используется уникальность структуры белка, его неповторимые индивидуальные формы и активные центры. СЕГМЕНТ 15. ОПОРА И ДВИЖЕНИЕ Опорно-двигательная функция - одна из важных в обеспечении жизнедеятельности клеток и всего организма. Движутся органоиды внутри клетки, сами клетки в воде или по твердой поверхности, организмы в их среде обитания. Движение невозможно без опоры, поэтому и в клетке и в организме формируются комплексные опорно-двигательные структуры. Например, у человека мышцы связаны со скелетом, и только в такой комбинации работа мышц становится эффективной. У позвоночных животных и человека опорные соединительные ткани имеют в межклеточной основе специальный волокнистый белок коллаген (при вываривании костей, сухожилий или связок он набухает и дает клей, отсюда и название белка - клей дающий). В костях межклеточная коллагеновая основа для большей твердости минерализована солями кальция. Имеются опорные белковые микронити и микротрубочки и в самих клетках, они придают клеткам определенную форму, поддерживают отростки (например, в нервных волокнах).
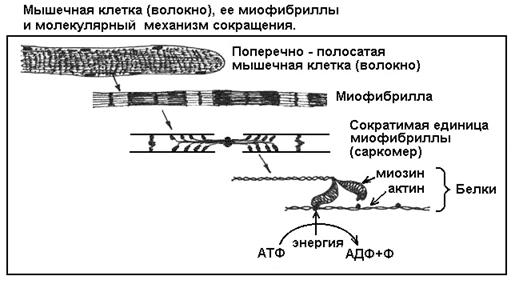
В клетках мышечной ткани имеются специальные сократительные нити - миофибриллы, которые обеспечивают сокращение клеток и всей мышцы. Каждая миофибрилла сложена из молекул белков двух основных видов - актина и миозина (рис. 7). Актин образует прочные микронити, по которым буквально шагают ножки миозина. Каждый шаг - это изменение третичной структуры молекулы миозина, его обратимая денатурация под действием энергии АТФ. Когда одна ножка, зацепившись за микронить, изгибается, другая ножка распрямляется и цепляется за новое место на микронити. Потом они меняются ролями - первая ножка отцепляется от микронити и распрямляется, а вторая изгибается и подтягивает нить. Каждый шаг требует энергии АТФ. Таким образом, при наличии АТФ ножки быстро бегут вдоль микронити, а точнее - тянут нить к себе, так как обращенные в разные стороны пучки миозина скреплены хвостиками, и ножки разных пучков тянут свои микронити в противоположных направлениях (см. рис. 7). Рис. 7
Главное, что следует вынести из описания мышечной функции, это понимание простой физико-химической сущности движения, которая сводится к изменению объемной формы молекулы белка миозина. Эта форма, или третичная структура, в свою очередь зависит от силы химических связей внутри молекулы. При энергетическом разряде от распада молекулы АТФ сила связей резко, но кратковременно изменяется - молекула «вздрагивает» (сгибается и тут же разгибается), совершая работу. Суть реакции миозина настолько проста, что воспроизводится in vitro («в стекле», в пробирке, то есть в искусственных условиях) на чистых белках, выделенных из клеток, или даже на мертвых клетках при добавлении АТФ. Добавим, что аналогичный механизм движения, но с другими белками, известен для ресничек и жгутиков, которыми снабжены многие одноклеточные организмы (например, инфузория), сперматозоиды, некоторые покровные (эпителиальные) ткани. Итак, движение - важное проявление жизни - имеет вполне материальную сущность.
|
||||||
|
Последнее изменение этой страницы: 2016-04-21; просмотров: 286; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.70.255 (0.006 с.) |