Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Термодинамические диаграммы i -lgP для хладагентов. М.: АВИСАНКО, 2003. – 50 с.Содержание книги
Поиск на нашем сайте
Термодинамические диаграммы i -lgP для хладагентов
ООО «АВИСАНКО»
Термодинамические диаграммы i -lgP для хладагентов. М.: АВИСАНКО, 2003. – 50 с.
В настоящей брошюре представлены термодинамические диаграммы i-lgP (удельная энтальпия-давление) и основные характеристики для всех известных хладагентов.
Рекомендуется для специалистов холодильной промышленности.
© AVISANCO, 2003 СОДЕРЖАНИЕ ВВЕДЕНИЕ…………………………………………………………………………………………………………………………………………………………………………... Графическое изображение цикла одноступенчатой холодильной машины……………………………………………………………………………………….………...….. R11, CCl3F, Trichlorofluoromethane……………………………………………………………………………………………………………………………………………….... R113, CCl2FCClF2, Trichlorotrifluoroethane………………………………………………………………………………………………………………………………………... R114, CClF2CClF2, Dichlorotetrafluoroethane……………………………………………………………………………………………………………………………………… R1150, CH2=CH2, Ethene (ethylene) ……………………………………………………………………………………………………………………………………………….. R12, CCl2F2, Dichlorodifluoromethane……………………………………………………………………………………………………………………………………………… R123, CHCl2CF3, Dichlorotrifluoroethane…………………………………………………………………………………………………………………………………………... R1270, CH3CH=CH2, Propene (propylene) ………………………………………………………………………………………………………………………………………… R13, CClF3, Chlorotrifluoromethane……………………………………………………………………………………………………………………………………………….... R134a, CH2FCF3, 1,1,1,2-tetrafluoroethane…………………………………………………………………………………………………………………………………………. R14, CF4, Tetrafluoromethane……………………………………………………………………………………………………………………………………………….............. R152a, CH3CHF2, 1,1-difluoroethane……………………………………………………………………………………………………………………………………………….. R170, CH3CH3, Ethane………………………………………………………………………………………………………………………………………………........................ R21, CHCl2F, Dichlorofluoromethane……………………………………………………………………………………………………………………………………………….. R22, CHClF2, Chlorodifluoromethane……………………………………………………………………………………………………………………………………………….. R23, CHF3, Trifluoromethane……………………………………………………………………………………………………………………………………………….............. R290, CH3CH2CH3, Propane……………………………………………………………………………………………………………………………………………….............. R401A, R22/152a/124 (53/13/34), R401A…………………………………………………………………………………………………………………………………………… R401B, R22/152a/124 (61/11/28), R401B…………………………………………………………………………………………………………………………………………… R401C, R22/152a/124 (33/15/52), R401C…………………………………………………………………………………………………………………………………………… R402A, R125/290/22 (60/2/38), R402A……………………………………………………………………………………………………………………………………………… R402B, R125/290/22 (38/2/60), R402B……………………………………………………………………………………………………………………………………………… R404A, R125/143a/134a (44/52/4), R404A………………………………………………………………………………………………………………………………………….. R406A, R22/142b/600a (55/41/4), R406A…………………………………………………………………………………………………………………………………………… R407A, R32/125/134a (20/40/40), R407A…………………………………………………………………………………………………………………………………………… R407B, R32/125/134a (10/70/20), R407B…………………………………………………………………………………………………………………………………………… R407C, R32/125/134a (23/25/52), R407C…………………………………………………………………………………………………………………………………………… R408A, R22/143a/125 (47/46/7), R408A…………………………………………………………………………………………………………………………………………….. R409A, R22/124/142b (60/25/15), R409A…………………………………………………………………………………………………………………………………………… R410A, R32/125 (50/50), R410A…………………………………………………………………………………………………………………………………………………….. R410B, R32/125 (45/55), R410B……………………………………………………………………………………………………………………………………………….......... R50, CH4, Methane………………………………………………………………………………………………………………………………………………............................... R500, R12/152a (73.8/26.2), R500………………………………………………………………………………………………………………………………………………........ R502, R22/115 (48.8/51.2), R502……………………………………………………………………………………………………………………………………………….......... R507, R125/143a (50/50), R507………………………………………………………………………………………………………………………………………………............ R508A, R23/116 (39/61), R508A……………………………………………………………………………………………………………………………………………….......... R600, CH3CH2CH2CH3, Butane………………………………………………………………………………………………………………………………………………......... R600a, CH(CH3)3, 2-methyl propane (isobutane) …………………………………………………………………………………………………………………………………... R717, NH3, Ammonia………………………………………………………………………………………………………………………………………………........................... R718, H2O, Water………………………………………………………………………………………………………………………………………………................................. R728, N2, Nitrogen………………………………………………………………………………………………………………………………………………................................ R729, N2/O2/A (76/23/1), Air………………………………………………………………………………………………………………………………………………............... R732, O2, Oxygen………………………………………………………………………………………………………………………………………………................................. R740, A, Argon………………………………………………………………………………………………………………………………………………...................................... R744, CO2, Carbon dioxide………………………………………………………………………………………………………………………………………………................... RC318, C4F8, Octafluorocyclobutane………………………………………………………………………………………………………………………………………………... ВВЕДЕНИЕ
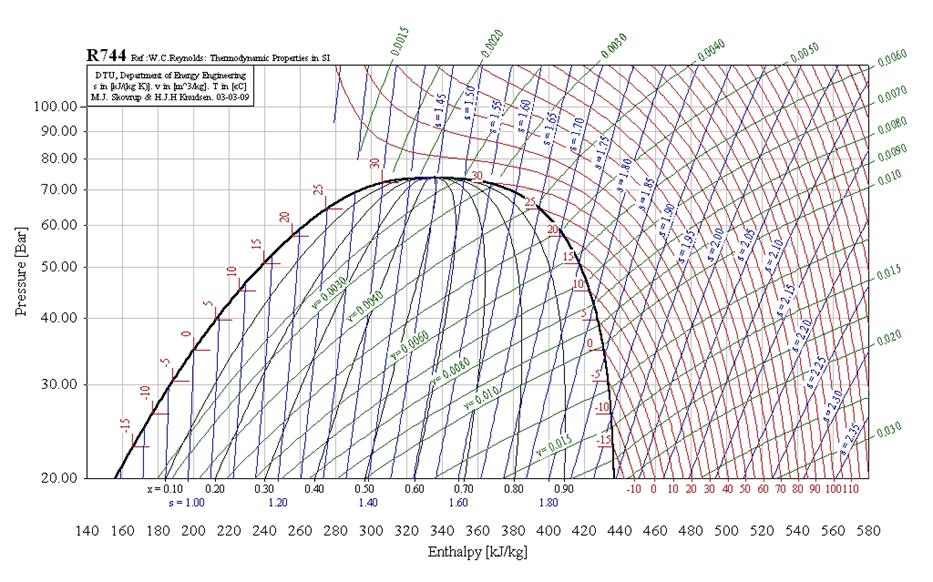
Для понимания цикла паровой компрессионной холодильной машины необходимо тщательно изучить отдельные процессы, входящие в него, а также связи, существующие между отдельными процессами, и влияние изменений в каком-либо процессе цикла на все другие процессы данного цикла. Это изучение в значительной степени можно упростить, используя диаграммы и схемы с графическим изображением цикла (см. рис. 1). Графическое изображение холодильного цикла позволяет рассматривать одновременно различные изменения в состоянии хладагента, происходящие в течение цикла, и влияние этих изменений на цикл без воспроизведения в памяти различных цифровых величин, связанных с циклом [1]. Наиболее распространенной в холодильной технике является диаграмма i –lgP* (удельная энтальпия - давление) как наиболее удобная для последующих тепловых расчетов. Состояние хладагента, находящегося в любом термодинамическом виде, может быть показано на диаграмме в виде точки, которая определяется двумя любыми параметрами, соответствующими данному состоянию. При этом могут быть использованы простые измеряемые параметры: температура (в °С или К); давление (в Па или в производных единицах: 1 кПа=103 Па, 1 МПа=106 Па=10 бар), а также удельный объем v (в м3/кг) или плотность ρ=1/v, кг/м3. Кроме простых измеряемых параметров, используют также сложные расчетные параметры. На диаграмме i –lgP таким (одним из основных) параметром является удельная энтальпия i, кДж/кг. Это полная энергия хладагента I, отнесенная к единице массы. В термодинамике удельную энтальпию i представляют в виде суммы внутренней энергии u, кДж/кг, и произведения абсолютного давления P, Па, на удельный объем v, м3/кг. i=u+Pv
В этом выражении произведение Pv представляет собой потенциальную энергию давления P, которая используется на совершение работы. Расчетным параметром является и энтропия S. В расчетах и на диаграммах используют удельное значение энтропии s, кДж/(кг·К). Так же, как и в случае энтальпии, для расчетов важно не значение энтропии «в точке», а ее изменение в каком-то процессе, то есть Δs=Δq/Tm, , где Δq – теплота, отнесенная к единице массы хладагента, а Tm , К – средняя абсолютная температура в течение процесса теплообмена между хладагента и внешней средой [2]. Для работы с диаграммой надо помнить, что она делится на три зоны: · переохлажденной жидкости – слева от кривой насыщенной жидкости (на диаграммах кривая черного цвета, имеющая максимальную толщину), где степень сухости пара x=0; · парожидкостной смеси – между кривыми x=0 и x=1 – насыщенный пар; · перегретого пара – справа от линии x=1. Линию, соответствующую насыщенной жидкости (x=0) называют левой, или нижней, пограничной кривой, а линию, соответствующую насыщенному пару (x=1), называют правой, или верхней, пограничной кривой. Линии постоянного давления – изобары – на диаграммах проходят горизонтально, а линии постоянной энтальпии – изоэнтальпы – вертикально (серые тонкие линии прямоугольной сетки). Процессы кипения и конденсации хладагента при постоянном давлении проходят между пограничными кривыми при неизменной (постоянной) температуре, соответствующей температуре насыщения при постоянном давлении.
--------------------------
* Логарифмическая ось давления принимается в целях уменьшения масштаба диаграммы [3].
|
||||
|
Последнее изменение этой страницы: 2024-06-17; просмотров: 5; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.158.246 (0.006 с.) |