
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Применение их соединений в медицине.⇐ ПредыдущаяСтр 12 из 12
Цинк Zn, кадмий Сd, ртуть Нg — микроэлементы. В организме взрослого человека содержится 1,8г (0,0024%) Zn, 50 мг (7-10-5%) Cd, 13мг (2-10-5%)Нg. Кадмий и ртуть — примесные элементы. Около 70% ртути сосредоточено в жировой и мышечной ткани. Кадмий локализуется на 30% в почках, остальное в печени, легких, поджелудочной железе. Цинк — необходимый элемент всех растений и животных. В организме взрослого человека больше всего цинка в мышцах (65%), костях (20%). Остальное количество приходится на плазму крови, печень, эритроциты. Наибольшая концентрация цинка в предстательной железе. Цинк не проявляет переменной валентности. Видимо поэтому его биокомплексы принимают участие во многих биохимических реакциях гидролиза, идущих без переноса электронов. Ион цинка входит в состав более 40 металлоферментов, катализирующих гидролиз эфиров и белков. Одним из наиболее изученных является бионеорганический комплекс цинка — фермент карбоангидраза (Мг = 30 000), состоящий, примерно, из 260 аминокислотных остатков. Ниже схематично представлено положение иона цинка в полости карбоангидразы (КА). Белковый лиганд, связанный с Zn2+, представляет активный центр фермента. Цинка в ферменте всего 0,22%. Тем не менее наличие цинка — необходимое условие каталитической активности карбоангидразы, которая обеспечивает гидратацию СО2: СО2 + Н2О → НСО3- + Н+ Протекание этой реакции обусловливает нормальное дыхание. В отсутствие карбоангидразы нормальный газообмен был бы затруднен, так как гидратация СО2 замедлилась бы в 10000000 (107) раз. Как видно из схемы, координационное число Zn2+ в карбоангидразе равно 4. Три связи заняты аминокислотными остатками (Нis — гистидил), а четвертая связывает гидроксил — ион ОН- или молекулу воды. Единого мнения о действии карбоангидразы нет. Одни исследователи считают, что цинк координирует молекулу воды, гидратирующую СО2. Другие полагают (механизм «цинк — гидроксид»), что цинк координирует гидроксильную группу при гидратации СО2: ОН- + СО2 ⇄ НСО3-
Прежде полагали, что карбоангидраза катализирует только обратимую гидратацию СО2. Однако имеются данные о каталическом действии карбоангидразы на превращение карбонильной группы (С=О) субстрата в карбоксильную (СООН). В этом случае механизм действия карбоангидразы подобен действию другого цинксодержащего фермента — карбоксипептидазы (КОП).
Механизм действия КОП окончательно не выяснен, и возможны два варианта. Механизм «цинк — карбоксил» предполагает, что субстрат вытесняет молекулу воды, координированную цинком. Затем карбонильная группа образует связь с ионом цинка. Другой механизм не предполагает образование связи через карбоксил фермента. Цинк не входит в состав дипептидаз — ферментов, катализирующих гидролиз дипептидов — веществ, состоящих из двух аминокислот. Цинк образует бионеорганический комплекс с инсулином — гормоном, регулирующим содержание сахара в крови. Потребность человека в цинке полностью удовлетворяется пищевыми продуктами: мясными, молочными, яйцами. При недостатке цинка в растениях нарушаются белковый и углеводный обмен, тормозится синтез хлорофилла и витаминов. Дефицит цинка устраняется при использовании цинксодержащих удобрений. Токсичность соединений IIБ-группы увеличивается от цинка к ртути. Водорастворимые соединения оказывают раздражающее действие на кожу. При попадании внутрь организма вызывают отравление. Токсичны и сами металлы. При вдыхании паров цинка (воздух цинковых производств) появляется «металлическая» лихорадка. Отравление парами ртути в средние века получило название «болезнь сумасшедшего шляпочника». Содержание ртути в пищевых продуктах (в морских, как в Японии) приводит к «болезни миномата». Токсичность ртути связана с агглютинацией (склеиванием, слипанием) эритроцитов, ингибированием ферментов. Например, сулема НgСl2 вызывает изменение размеров, осмотическую хрупкость и снижение деформируемости эритроцитов, которая необходима для их продвижения по капиллярам. Токсичность кадмия связана с его сродством к нуклеиновым кислотам. В результате его присоединения к ДНК нарушается ее функционирование.
Хроническая интоксикация кадмием и ртутью может нарушить минерализацию костей. Это связано с близостью ионных радиусов. Поэтому токсичные элементы могут замещать кальций. Это приводит к образованию апатита несовершенной структуры вследствие искажения параметров кристаллического компонента костной ткани. В результате снижается прочность костей. Соединения Zn, Сu, Нg могут вызывать нарушение белкового обмена, что проявляется в выделении белков плазмы через почки (протеинурия). Токсичное действие соединений группы IIБ на организм вызывается еще и тем, что ионы этих металлов вступают во взаимодействие с сульфгидрильными SН-группами белков, ферментов и аминокислот.
В реакциях подобного типа ионы металлов выступают акцептором, а сера — донором электронов. Наиболее выражено химическое сродство SН-группам у ртути. Очевидно, это связано с тем, что комплексообразующие свойства ртути выше и она образует более прочные связи с серой. SН-группы входят в состав более 100 ферментов, активность которых может быть подавлена из-за блокирования этих групп. Поэтому очевидно, насколько важно знать механизм блокирования и методы лечения при отравлении организма металлами. Известно, что токсические свойства элементов зависят от той химической формы, в какой они попадают в организм. Наиболее токсичны те формы, которые растворяются в липидах и легко проникают через мембрану в клетку. В литературе описан случай массового отравления ртутью в Японии. Неорганические соединения ртути под действием ферментов микроорганизмов превращались в метилртуть: Нg2+ + СН3- → СН3Нg+ Метилртуть накапливалась в рыбе, а затем с пищей попадала в организм человека. Из-за того, что СН3Нg+ растворяется в липидах, она накапливается в организме, в том числе и в мозге. Постепенно концентрируясь, метилртуть вызывает необратимые разрушения в организме и смерть. Использование соединений цинка и ртути в медицине основано на их вяжущем, прижигающем и антисептическом действии. В качестве глазных капель применяют 0,25%-ный водный раствор цинк сульфата ZnSО4. В стоматологии цинк хлорид ZnСl2 используют для прижигания папилом, для лечения воспаленных слизистых. Применяется также цинк оксид ZnО. Хлорид ртуть (II) Нg2Сl2 (сулема) очень ядовита и ее водные растворы при больших разбавлениях (1:1000) применяются для дезинфекции. Для лечения кожных и венерических заболеваний применяют мази, содержащие оксид ртути (II) НgО и сульфид ртути (II) НgS. Хлорид ртути (I) Нg2Сl2 (каломель) плохо растворяется в воде и поэтому мало ядовита. Эту соль применяют в ветеринарии как слабительное средство. Ртуть при обычных условиях — жидкий металл, который способен растворять другие металлы. При этом образуются твердые сплавы — амальгамы. В стоматологии для пломбирования зубов издавна применяли амальгамы серебра и кадмия. Они химически инертны, легко размягчаются при нагревании и поэтому легко формуются. Жидкая ртуть используется в ряде приборов, применяемых в медицине. Например, для измерения артериального давления, в медицинских термометрах.
Источники ультрафиолетового света — ртутно-кварцевые лампы медицинского назначения содержат газообразную ртуть (пары). При облучении светом этих ламп больничных помещений уничтожаются микроорганизмы, содержащиеся в воздухе. С помощью ультрафиолетовых лучей лечат различные кожные заболевания. Таким образом, по характеру функционирования и воздействия на организм металлы IIБ-группы можно разделить на жизненнонеобходимый элемент Zn и токсичные примесные элементы Сd и Нg.
Семейство платины.
В электрохимическом ряду все платиновые металлы стоят после водорода. По значениям электроотрицательности все элементы группы ближе к неметаллам, чем к металлам. Поэтому соединения этих металлов проявляют амфотерность, выраженную в разной степени. Гидроксиды не всех этих элементов растворяются и в кислоте и в щелочи. Тем не менее, элементы семейства платины образуют не только катионные, но и анионные комплексы. Устойчивые валентные состояния для элементов семейства платины следующие: Ru — IV, VI, VIII; Rh — III, IV; Рd — II, IV; Оs — IV, VI; Ir — III, IV; Рt — II, IV. Гидроксиды Ru, Rh, Рd, Оs, Ir и Рt в четырехвалентном состоянии существуют в форме МО2∙nН2О, где n = 2 (для платины n = 2, 3). Содержание воды зависит от температуры. Гидроксиды Rh, Рd и Рt растворяются в кислотах и щелочах: РtO2∙3Н2О + 2NаОН → Na2[Рt(ОН)6] + Н2О РtO2∙3Н2О + 6НСl → H2[РtСl6] + 5Н2О В обычных условиях платиновые металлы не взаимодействуют с такими сильными окислителями, как F2, Сl2 и О2. Низкая реакционная способность элементных веществ определяется большой энергией связи в кристаллической решетке. Та же причина определяет высокие температуры плавления и большие значения плотности. Только платина реагирует без нагревания с окисляющей смесью кислот 3Рt + 18НСl + 4НNО3 ⇄ 3H2[PtСl6] + 4NО + 8Н2О или с соляной кислотой в присутствии кислорода Рt + 6НСl + О2 ⇄ Н2[РtСl6] + 2Н2О Все металлы платинового семейства, кроме иридия, переходят в четырехвалентное состояние при сплавлении со щелочными окисляющими смесями. Например:
Ru + 2КОН + 3КNО3 → К2RuО4 + 3КNО2 + Н2О Иридий переходит в трехвалентную форму. При нагревании платиновые металлы реагируют с NаСl или НСl в токе хлора, что приводит к образованию комплекса. Например: Ir + 2NаСl + 2Сl2 → Na2[IrСl6] Платина при нагревании может образовывать цианидный комплекс: Рt + 6КСN + 4Н2О → К2[Рt(СN)6] + 4КОН + 2Н2 Элементы платинового семейства образуют комплексные соединения с координационными числами 4 и 6. Наиболее изучены цианидные, галогенидные и аммиачные комплексы. Комплексные соединения могут быть катионные, анионные и нейтральные. Катионный комплекс: [Рt(NН3)2Сl2] + 2NН3 → [Рt(NН3)4Сl2] Нейтральный комплекс: [Рt(NН3)4]Сl2 + 2НСl ⇄ [Рt(NН3)2Сl2] + 2NН4Сl Катионно-анионный комплекс: [Рt(NН3)4]Сl2 + К2[РtСl4] → [Рt(NН3)4] [РtСl4] + 2КСl Применение соединений платиновых элементов в медицине. Многочисленные исследования показали, что цис-изомер дихлородиамминплатины(II) [Рt(NН3)4]Сl2 оказывает лечебное действие при раковых заболеваниях. Действие этого комплекса основано на том, что в нем происходит постепенное замещение хлорид-ионов хелатирующими лигандами. Такими лигандами являются аминокислотные остатки в белках. Координация идет за счет взаимодействия металла с атомами азота лиганда. После замещения хлорид-ионов создаются условия для замещения и групп NН3. В результате платина образует четыре связи с новыми лигандами. Это свойство цис-дихлородиамминплатины приводит к образованию устойчивого комплекса с молекулой ДНК. Таким образом, это вещество ингибирует синтез ДНК. Интересно отметить, что транс-изомер дихлородиамминплатины (II) токсичен, но противоопухолевым действием не обладает.
Оксид осмия (VIII) ОsO4 применяется как фиксатор ткани (липидный стабилизатор) для гистологических исследований в виде 1%-ного раствора в ацетоне. ОsO4 можно использовать и для электронно-микроскопического выявления ферментов. Механизм действия ОsO4 может быть представлен в следующем виде:
Восстановление может идти глубже и будет образовываться Оs2О3 или ОsО. Все эти соединения имеют темно-коричневый или черный цвет, т.е. обеспечивается эффект контрастирования участка клетки или ткани (образуются эфиры холестерина и триглицеридов)
Комплекс [Ru(NН3)4(ОН)Сl]Сl — рутениевый красный также применят для анатомических и гистологических исследований. Его раствор (1:5000) окрашивает в розово-красные тона пектин.
|
|||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 22; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.71.146 (0.026 с.) |

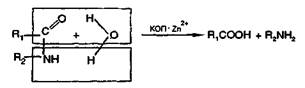 Одна из наиболее изученных форм КОП имеет 307 аминокислотных остатков (содержание цинка 0,19%). Схему реакции превращения карбонильной группы субстрата в карбоксильную, катализируемой КОП, можно представить следующим образом:
Одна из наиболее изученных форм КОП имеет 307 аминокислотных остатков (содержание цинка 0,19%). Схему реакции превращения карбонильной группы субстрата в карбоксильную, катализируемой КОП, можно представить следующим образом: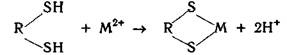 При взаимодействии ионов металлов с SН-группами образуются слабодиссоциирующие и, как правило, нерастворимые соединения. Поэтому блокирование сульфгидрильных групп приводит к подавлению активности ферментов и свертыванию белков. Ионы двухвалентных металлов блокируют одновременно две SН-группы.
При взаимодействии ионов металлов с SН-группами образуются слабодиссоциирующие и, как правило, нерастворимые соединения. Поэтому блокирование сульфгидрильных групп приводит к подавлению активности ферментов и свертыванию белков. Ионы двухвалентных металлов блокируют одновременно две SН-группы. В подгруппу платины входит шесть переходных металлов. По числу электронов на 4dЗs-орбиталях (Ru, Rh, Рd) и 5d6s-орбиталях (Оs, Ir, Рt) и по аналогии физико-химических свойств все элементы VI IIБ-группы делятся на три подгруппы: 1) Ru — Оs; 2) Rh — Ir; 3) Рd — Рt. Атомный радиус у всех шести элементов изменяется в небольшом интервале: 134 пм (Ru) — 139 пм (Рt).
В подгруппу платины входит шесть переходных металлов. По числу электронов на 4dЗs-орбиталях (Ru, Rh, Рd) и 5d6s-орбиталях (Оs, Ir, Рt) и по аналогии физико-химических свойств все элементы VI IIБ-группы делятся на три подгруппы: 1) Ru — Оs; 2) Rh — Ir; 3) Рd — Рt. Атомный радиус у всех шести элементов изменяется в небольшом интервале: 134 пм (Ru) — 139 пм (Рt).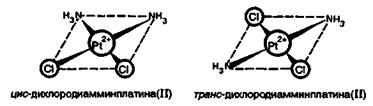 Наряду с цис-дихлор-диамминплатиной (II) противоопухолевой активностью обладают и другие комплексы, содержащие в качестве лигандов амины и хлорид-ионы. Например, цыс-диамминтетрахлорплатина (IV) [Рt(NН3)2Сl4] и цис-дианилиндихлороплатина (II) [Pt(NH2C6H5)2Cl2]:
Наряду с цис-дихлор-диамминплатиной (II) противоопухолевой активностью обладают и другие комплексы, содержащие в качестве лигандов амины и хлорид-ионы. Например, цыс-диамминтетрахлорплатина (IV) [Рt(NН3)2Сl4] и цис-дианилиндихлороплатина (II) [Pt(NH2C6H5)2Cl2]: Сплавы Рt — Ir и Рt — Аu применяются в ортопедической стоматологии, для изготовления шприцов; сплавы Рd—Аu, Рd—Аu—Рt, Рd—Рt—Ir — для изготовления хирургических инструментов, в ортопедической стоматологии используют сплавы Рd—Аu или Рd—Аg,Сu,Ir. Вживляемые в сердце электроды для стимуляции изготовлены из сплава Рt—Ir; Ir—Рt — эталон массы (а раньше и длины). Для дезинфекции питьевой воды применяют О3, его можно получить по реакции:
Сплавы Рt — Ir и Рt — Аu применяются в ортопедической стоматологии, для изготовления шприцов; сплавы Рd—Аu, Рd—Аu—Рt, Рd—Рt—Ir — для изготовления хирургических инструментов, в ортопедической стоматологии используют сплавы Рd—Аu или Рd—Аg,Сu,Ir. Вживляемые в сердце электроды для стимуляции изготовлены из сплава Рt—Ir; Ir—Рt — эталон массы (а раньше и длины). Для дезинфекции питьевой воды применяют О3, его можно получить по реакции: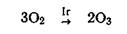 , где Ir — катализатор (порошкообразный иридий).
, где Ir — катализатор (порошкообразный иридий).



