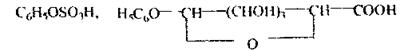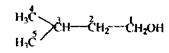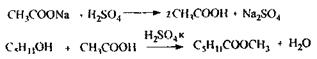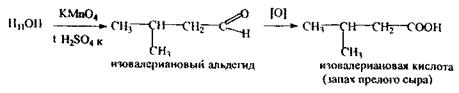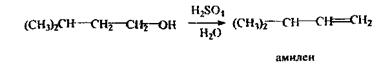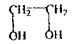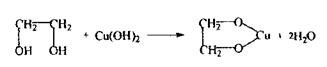Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Спостерігається червоне забарвлення розчину.Содержание книги
Поиск на нашем сайте
Реакціями, що підтверджують наявність ацетону, є реакції з альдегідами, наприклад, з фурфуролом - реакція неспецифічна. Спостерігається червоне забарвлення розчину. Залишок другого дистиляту змішують із третім дистилятом і знову проводять аналіз на галогенпохидні і формальдегід. З частиною третього дистиляту, що залишилася, виконують аналіз на фенол і ізоаміловий спирт. Летальні дози для фенолу - 8-15 г. Фенол добре всмоктується в організмі при попаданні через рот, дихальні органи. При токсичних дозах спостерігається печія, біль у шлунку, блювота, пронос, сеча чорного кольору. Відзначається жирове переродження печінки, нирок. Метаболізм фенолу:
З організму фенол виділяється із сечею у вигляді ефірів із сульфатною і глюкуроновою кислотами:
Темно-зелений колір сечі свідчить про окислювання фенолу за схемою:
Особливістю ізолювання фенолу є підлужнювання дистилляту розчином натрію гідрокарбонату до рН 8-9 для зв'язування слабких кислот (оцтової, саліцилової, молочної), що реагують з FеС13.Фенол екстрагують ефіром, ефірний витяг упарюють і реакції виконують із сухим залишком. При спрямованому аналізі на фенол, біологічний об'єкт підкислюють більш сильною СН3СООН, яку зв'язують потім лугом і фенол екстрагують ефіром.
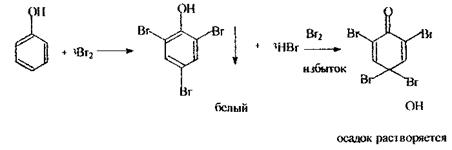
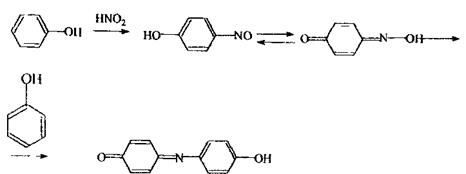
Аналіз фенолу починають проведенням реакції з бромною водою - найбільш чутливою, попередньою, але неспецифічною (анілін, саліцилова кислота, ароматичні аміни й ін.)
Даною реакцією виявляють фенол, який утворюється при гнитті білка. Судово-хімічне значення має негативний результат реакції.
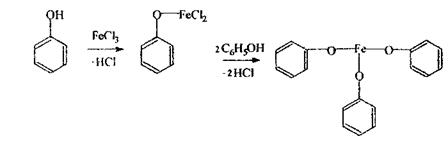
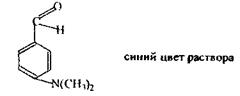
Реакція з хлоридом окісного заліза - специфічна для фенольного гідроксилу, спостерігається синє забарвлення розчину. Індофенольна реакція - неспецифічна, підтверджуюча.
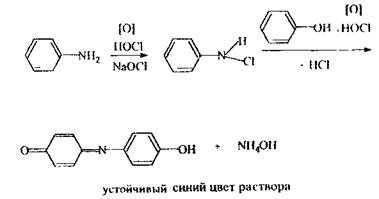
Реакція Лібермана - реакція утворення індофенолу, неспецифічна, підтверджуюча, спостерігається синє забарвлення, що переходить у червоне, а потім у зелене забарвлення.
Реакція з реактивом Міллона (суміш нітратів одно- і двовалентного меркурію, що містить азотисту кислоту), неспецифічна, підтверджуюча, спостерігається червоне або оранжеве забарвлення.
Ізоаміловий спирт
С5Н11ОН - головна складова частина сивушних олій і летальна доза складає 10-15 г. До складу сивушних олій також входять вищі спирти (бутиловий, аміловий), альдегіди, ефіри, кетони. Використовується ізоаміловий спирт в медицині, при виробництві бездимного пороху. Токсична дія ізоамілового спирту - наркотик; більш отрутний, ніж етанол, тому що повільно всмоктується, метаболізує і виводиться, викликаючи більш сильне і тривале сп'яніння з неврологічними і психічними порушеннями. Метаболізм: частина введеної дози метаболізує по шляху окислювання до ізовалер’янового альдегіду і ізовалер’янової кислоти, а частина - виводиться в незмінному вигляді нирками та легенями. Особливості ізолювання: спирт екстрагують ефіром (хлороформом) з дистиляту, а після того відганяють ефір і виконують аналіз. При аналізі вина, 40-50 мл його розводять водою до вмісту етанолу 10-15 % (спирт у такій кількості не ізолюється ефіром або хлороформом), а потім 15 мл СНС13 ізолюють ізоаміловий спирт. Аналіз ізоамілового спирту починають з реакції утворення ізоамілацетату, попередньої, специфічної:
Відчувається запах грушевої есенції, що підсилюється при розведенні водою.
Реакція окислення ізамілового спирту — підтверджувальна, специфічна. Реакція з альдегідами, підтверджуюча, неспецифічна:
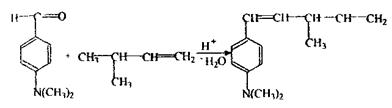
Реакція з п-диметилбензальдегідом
Реакція з саліциловим альдегідом.
Механізм реакції точно не описаний.
Один з можливих механізмів:
Ці реакції дають вищі спирти, не дають СН3 ОН і С2Н5ОН.
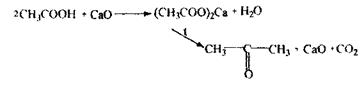
Оцтова кислота На оцтову кислоту виконують цілеспрямований аналіз, летальні дози 200 мл оцту, 10-20 г оцтової есенції. Токсична дія оцтової кислоти - опік стравоходу, уремія, гемолітична анемія. Метаболізм:
Особливості ізолювання: Аналіз спрямований, тому біологічний матеріал підкислюють розчином Н 2 SО4 або Н3 РО4. Оцтова кислота летка і її збирають у 0,1н NаОН. Аналіз на оцтову кислоту починають з реакції з хлоридом окісного заліза, неспецифічної, чутливої, попередньої.
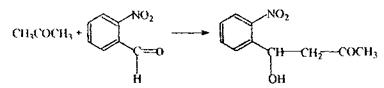
Реакція утворення складного ефіру, відчувається запах оцтово-етилового ефіру, реакція підтверджуюча, специфічна.
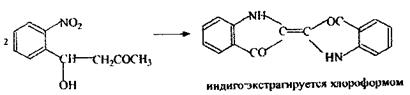
Реакція утворення індіго, підтверджуюча, неспецифічна.
Ацетон при взаємодії з о-нітробензальдегідом в лужному середовищі утворить індіго, що має синє забарвлення.
Етиленгліколь Двохатомний спирт, безбарвна масляниста рідина, змішується з водою у всіх співвідношеннях.
Етиленгліколь використовується в техніці як антифриз; у хімічній промисловості - як розчинник; для проведення органічного синтезу. Поводження в організмі - шляхи надходження через рот; шкіру; тому що спирт мало леткий, то його надходження через органи дихання обмежене. Метаболізм складний, який включає багатоетапне окислення:
Виведення етиленгліколю і його метаболітів - із сечею. Токсичність етиленгліколю полягає в тому, що він є судинною та протиплазматичною отрутою, яка викликає дегенерацію судин і пошкодження нирок за рахунок відкладення в них оксалатів.
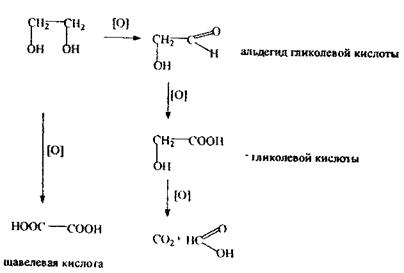
Особливість спрямованого ізолювання з біологічного матеріалу - використання бензолу як селективного переносника етиленгліколю при перегонці з водяною парою. Збирають дистилят об’ємом не менш 500 мл. Дистилят розділяється на 2 шари: верхній - бензол, нижній- етиленгліколь з водою. Аналіз етиленгліколю починається з попередньої реакції окислення етиленгліколю до формальдегіду, яка чутлива, неспецифічна.
Формальдегід виявляють при проведенні реакції з фуксинсульфатною кислотою по появі бузкового забарвлення розчину. Реакція із сульфатом купруму - підтверджуюча, неспецифічна Спостерігається синє забарвлення розчину.
Реакція окислювання етиленгліколю до щавлевої кислоти - підтверджуюча, специфічна Спостерігається утворення характерних за формою кристалів оксалату кальцію.
Тетраетилсвинець (ТЕС)
Тетраетилсвинець -(С2Н3)4РЬ - прозора безбарвна рідина, майже не розчиняється у воді, легко розчинна в бензині, ефірі, хлороформі, спирті, у жирах, маслах. Легко розкладається під впливом нагрівання, сонячних променів до неорганічних солей плюмбуму. Використовується як антидетонатор. Тетраетилсвинець дуже токсичний, надходить через рот, органи дихання, шкіру, поражає нервову систему, викликає головний біль, безсоння, розлад зору, судороги. Особливість спрямованого ізолювання - після перегонки з водяною парою тетраетилсвинець збирають у приймач зі спиртовим розчином йоду. (С2Н3)Рb + J2 →РbJ2 + 2С4Н10 Потім рідину випаровують до сухою залишку, який розчиняють в нітратній кислоті РbJ2+ 2НNО3 → Рb (NO3)2 + 2HJ Розчин знову випаровують і сухий залишок розчиняють у воді й аналізують на Рb2+ реакціями утворення дитизонату плюмбуму РbSО4, РbS, РbСгО4, РbJ2 . При аналізі харчових продуктів, одягу, рослинної сировини тетраетилсвинець екстрагують органічними розчинниками.
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 340; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.180.254 (0.007 с.) |