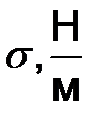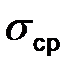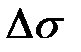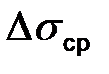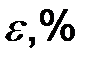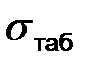Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Висновок: зробити самостійно.Содержание книги Поиск на нашем сайте
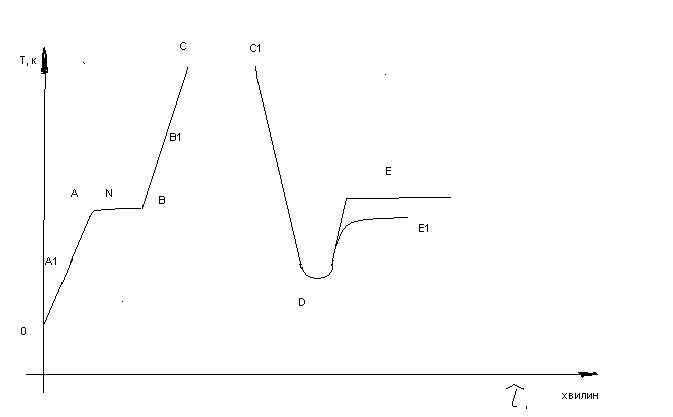
9 Домашнє завдання: підготуватись до наступної лабораторної роботи. ЛАБОРАТОРНА РОБОТА № 2 Спостереження процесів плавлення та кристалізації гіпосульфіта. 1 МЕТА. Дослідити процеси плавлення та кристалізації. ЗАВДАННЯ 2.1 За даними досліду побудувати на міліметровому папері графік плавлення та кристалізації гіпосульфіту. 2.2 За графіком визначити температуру плавлення гіпосульфіту (та кристалізації) ОБЛАДНАННЯ 3.1Колба з гіпосульфітом. 3.2Посудина з водою. 3.3Лабораторна плитка. 3.4Термометр. 3.5Секундомір. Вказівки на теоретичний матеріал 4.1 Фазові переходи 1 і 2 роду. (Л.1.,с.141) 4.2 Плавлення та кристалізація. (Л.1.,с139) Теоретичні положення. Графік, побудований у координатах „ температура – час”, відображує процеси, які відбуваються під час досліду при нагріванні і охолодженні з кристалізацією. Спочатку температура зростає пропорційно часу. Нахил прямої до осі абсцис залежить від потужності нагрівача. Під час плавлення температура речовини не змінюється, уся теплота іде на руйнування зв’язків у кришталевій решітці і збільшення кінетичної енергії молекул. Теоретично на цій ділянці графік уявляє собою пряму АВ, яка паралельна осі абсцис (рис 1). Але у зв’язку з тим, що температура у різних містах колби з гіпосульфітом внаслідок неідеальної теплопровідності неоднакова, а термометр вимірює температуру шару навколо головки, то у дійсності процес протікає по кривій. Після того як температура гіпосульфіту піднялась приблизно до 50...60 C, колбу починають охолоджувати у холодній воді по можливості до більш низької температурі (лінія С1D). Якщо охолодження проводити достатньо швидко і без дотиків, розплав можна довести до переохолодженого стану. Переохолоджений гіпосульфіт кристалізується з виділенням теплоти кристалізації при стряхуванні або попаданні у нього стороннього тіла і особливо при внесенні у розплав кристалика твердого тіла (центрів кристалізації). Теплота, яка при цьому виділяється, нагріває гіпосульфіт. Якщо при кристалізації не охолоджувати колбу з гіпосульфітом, то температура може піднятися до точки плавлення (лінія DE), або процес кристалізації може відбуватися при більш низькій температурі.
рисунок 1 ХІД РОБОТИ 6.1 Нагріваємо колбу з гіпосульфітом у водяній бані. 6.2 Як тільки температура почне підійматись, вмикаємо секундомір і записуємо значення температури через кожні 10-15 секунд. 6.3 При досягненні температури 50-60 С вимкнути плитку і опустити колбу з гіпосульфітом у холодну ванну. Продовжуємо спостерігати за зменшенням температури, записуючи значення через кожні 10-15 секунд. 6.4 Коли охолодження припиниться, убирають воду і у розплав вводять кристалики гіпосульфіта. При цьому продовжують записувати значення температур до того моменту, поки температура після підвищення не почне падати. 6.5Отримані результати занести до таблиці:
6.6 Побудувати графік на міліметровому папері. 6.7 Визначити температуру плавлення гіпосульфіту та кристалізації. КОНТРОЛЬНІ ПИТАННЯ 7.1Фізичний зміст понять: температура плавлення, теплота плавлення, кристалізація. Умови плавлення. 7.2Чому температура під час плавлення не змінюється? 7.3Дати пояснення за побудованим графіком змінення температури із зміненням часу. Література Трофимова Т.И. Курс физики: Учеб. пособие для вузов. 1999 9 ВИСНОВОК: зробити самостійно. 10 Домашнє завдання: підготуватись до наступної лабораторної роботи Лабораторна робота №3 Тема:Визначення коефіцієнту поверхневого натягу методом відриву кільця. 1 Мета. Визначити коефіцієнт поверхневого натягу води та порівняти з теоретичним значенням.
Завдання 2.1 Методом відриву кільця визначити коефіцієнт поверхневого натягу води. 2.2 Необхідні виміри зробити за допомогою штангенциркуля. 2.3 Обчислити за експериментальними даними коефіцієнт поверхневого натягу води.
3 Обладнання 3.1Спеціальна установка. 3.2 Штангенциркуль. 3.3 Технічні ваги. 3.3 Досліджувана рідина – вода. Вказівки на теоретичний матеріал 4.1 Властивості поверхні рідини. (Л.1., с.126) 4.2 Змочування. (Л.1., с.130) Теоретичні положення Поверхневий натяг можна визначити шляхом виміру сили, яку потрібно прикласти перпендикулярно до поверхні рідини для відриву різних твердих тіл від цієї поверхні. Так як тіло, яке відриваємо,змочується рідиною, то разом з ним підіймається деяка кількість рідини, т.б. вільна поверхня рідини буде збільшуватись. Внаслідок намагання цієї поверхні скоротитися з’являється сила поверхневого натягу. Якщо сила, яка діє на тіло, дорівнює за значенням силі поверхневого натягу, то тіло одірветься.
Роздивимось кільце із зовнішнім діаметром D товщею d, яке дотикається поверхні рідини. При підніманні кільця над поверхнею рідини між кільцем і поверхнею води утворюється викривлена плівка. Зовнішня поверхня цієї плівки тягне кільце вниз із силою: F=σ ∙ π ∙ D внутрішня поверхня — із силою: F= σ ∙ π ∙ (D – d) Рівнодіюча сила, яка утримує кільце: σ π D + σ π (D – d) ≈ 2 σ ∙ π (D – d). У момент відриву F = 2σ ∙ π (D – d), звідки
Так як діаметр і товща кільця можуть бути виміряні штангенциркулем, то визначення коефіцієнту поверхневого натягу зводиться до визначення сили відриву F.
Порядок виконання роботи 6.1 Воду налити у ємність і обережно підняти її до торкання рідини і кільця. 6.2 Помітити по шкалі покази рівню на якому знаходиться кільце. 6.3 Обережно опускаючи ємність з рідиною помітити покази рівню кільця по шкалі у момент відриву кільця (максимальне розтягнення пружини). 6.4 Загрузити площину гирьками, поки кільце не опуститься на раніше помічені покази. Користуючись законом Гука, знайти значення сили поверхневого натягу(у момент відриву кільця сила поверхневого натягу зрівноважена силою пружності; сила пружності буде чисельно дорівнювати силі тяжіння, значить сила натягу чисельно дорівнює модулю сили тяжіння) F=mg, де m-маса гирьок, якими ми загрузили кільце, g-прискорення вільного падіння. 6.5 За формулою (*) обчислити коефіцієнт поверхневого натягу води. 6.6 Дослід повторити 3 – 4 рази, результати занести до таблиці1.
Таблиця 1
6.7 Обчислити абсолютну і відносну похибки. 6.8 Порівняйте розраховане значення поверхневого натягу води із табличним.
7 Контрольні питання 7.1 Фізична сутність понять: поверхневий натяг, змочування, сила поверхневого натягу, енергія поверхневого шару. 7.2 У яких одиницях вимірюється поверхневий натяг? 7.3 Лапласівський тиск. Меніск. Умова підняття рідини у капілярі. 8 Література. Трофимова Т.И. Курс физики: Учеб. пособие для вузов. 2004.-560 с.
9 Висновок: зробити самостійно. 10 Домашнє завдання: вивчити конспект лекцій з даної теми.
Лабораторна робота №4
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 278; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.48.125 (0.011 с.) |




 мм
мм
 ,
мм
,
мм