
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Веществ, химических соединений, объема и состава продуктов их горения
А) Твердые вещества (расчет по массе) 1. Составляем уравнение реакции горения вещества в воздухе. 2. Рассчитываем объём, занимаемый 1 кмоль газа при заданных условиях.
где 22,4 м3/кмоль - объем, занимаемый 1 кмоль газа при нормальных условиях. Рну - атмосферное давление при нормальных условиях, равное 101325 Па. Тну – температура при нормальных условиях, равная 273К. Т - заданная температура, К. Р - заданное давление, Па. 3. Определяем молярную массу горючего вещества (М). 4. Рассчитываем объем воздуха, необходимый для сгорания горючего вещества.
где 4,76 - число кмоль воздуха (1 кмоль О2 + 3,76 кмоль N2); β - стехиометрический коэффициент, стоящий перед кислородом в уравнении реакции горения. m – масса горючего вещества, кг; Vt – объем, занимаемый 1 кмоль воздуха при заданных условиях, м3/кмоль; М - молярная масса горючего вещества, кг/кмоль; a - коэффициент избытка воздуха. 5. Определяем число кмоль кислорода и азота в избытке воздуха.
6. Рассчитываем общее количество вещества продуктов горения
7. Находим объем продуктов горения по формуле:
где Vt – объем, занимаемый 1 кмоль продуктов горения при заданных условиях, м3/кмоль; m - масса горючего вещества, кг; М - молярная масса горючего вещества, кг/кмоль; Snпг - количество вещества продуктов горения, кмоль.
8. Рассчитываем объёмы компонентов продуктов горения по формуле:
9. Рассчитываем мольный процентный состав продуктов горения, принимая общее число кмоль продуктов горения за 100 %.
Аналогично рассчитывается объемный процентный состав продуктов горения. Численное значение объемных процентов при этом будет совпадать с мольным процентным составом продуктов горения. Б) Газообразные вещества (расчет по объему): 1. Составляем уравнение реакции горения вещества в воздухе. 2. Рассчитываем объем воздуха, необходимого для сгорания вещества.
где Vв - теоретический объем воздуха необходимый для сгорания вещества, м3.
a - коэффициент избытка воздуха. Vгг - заданный объем горючего газа, м3.
3. Определяем число кмоль кислорода и азота в избытке воздуха.
4. Рассчитываем общее количество вещества продуктов горения
5. Находим общий объем продуктов горения по формуле: Vпг = Vгг × ånпг, м3 где Vгг - заданный объем горючего газа, м3; ånпг- общее количество вещества продуктов горения, кмоль.
6. Рассчитываем объём компонентов продуктов горения по формуле:
7. Рассчитываем мольный процентный состав продуктов горения, исходя из общего числа кмоль продуктов горения.
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 103; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.13.173 (0.006 с.) |
 , м3/кмоль;
, м3/кмоль;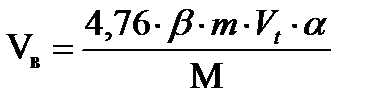 , м3;
, м3; = b(a - 1), кмоль;
= b(a - 1), кмоль;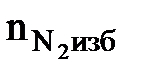 =3,76 × b(a - 1), кмоль.
=3,76 × b(a - 1), кмоль. , кмоль;
, кмоль;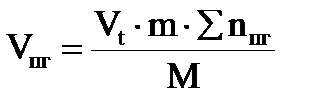 , м3
, м3



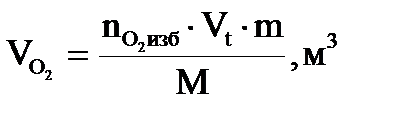 и т.д.
и т.д.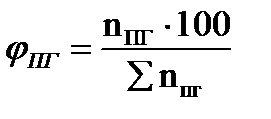 , мол. %;
, мол. %;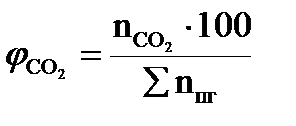 , мол. %;
, мол. %; 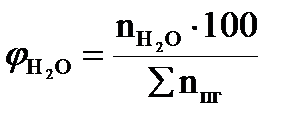 , мол. %;
, мол. %;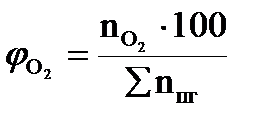 , мол. %;
, мол. %;  , мол. % и т.д.
, мол. % и т.д.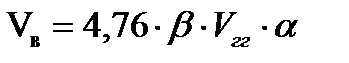 , м3,
, м3, - стехиометрический коэффициент при кислороде в уравнении реакции горения.
- стехиометрический коэффициент при кислороде в уравнении реакции горения.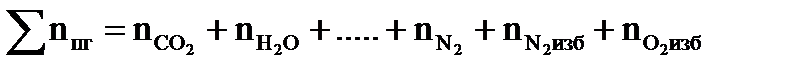 , кмоль.
, кмоль. = Vгг×
= Vгг×  , м3;
, м3;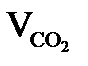 = Vгг×
= Vгг×  , м3;
, м3; 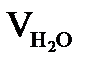 = Vгг×
= Vгг× 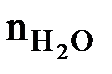 , м3;
, м3; = Vгг×
= Vгг× 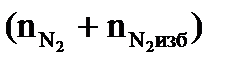 , м3
, м3 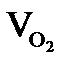 = Vгг×
= Vгг×  , м3 и т.д.
, м3 и т.д.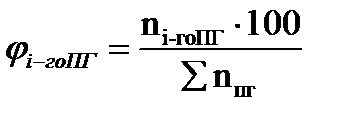 , мол. %;
, мол. %;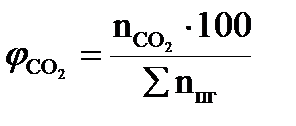 , мол. %;
, мол. %;  , мол. %;
, мол. %; , мол. %;
, мол. %; 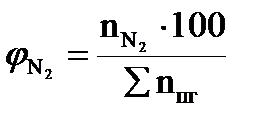 , мол. % и т.д.
, мол. % и т.д.


