
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные сведения об этаноле ⇐ ПредыдущаяСтр 3 из 3
Физические свойства Бесцветная легкоподвижная жидкость с характерным алкогольным запахом и жгучим вкусом, отлично растворимая в воде. Ядовита, но менее, чем метанол. * В продажу поступает спирт-ректификат, т.е. 95,5 % раствор этанола, т.е. содержит 4,5 % воды. Такая смесь этилового спирта и воды перегоняется без разделения на спирт и воду и называется азеотропной смесью. Чтобы получить 100 % этиловый спирт (безводный или абсолютный) его кипятят с водоотнимающими реагентами (безводным медным купоросом или негашёной известью). | |||||||||||||||
|
Химические свойства 1) 2C2H5ОН + 2Na → 2C2H5ОNa + H2↑ замещение 2) C2H5ОН + HBr 3) C2H5ОН + 3O2 * 4) C2H5ОН + СuO * 5) C2H5ОН ** 6) C2H5ОН + СН3СООН ** 7) 2C2H5ОН ** 8) 2C2H5ОН | ||||||||||||||||
|
Применение Является одним из наиболее важных органических веществ. Широко используется как растворитель (в технике) и антисептик (в медицине), для получения хлороформа, синтетического каучука, различных эфиров, красок и лаков, лекарственных препаратов, парфюмерных изделий (одеколонов, духов, лосьонов), а также в пищевой промышленности. | ||||||||||||||||
ОСНОВНЫЕ СВЕДЕНИЯ О ГЛИЦЕРИНЕ
| Общие сведения | ||
| Молекулярная формула С3Н8О3 или СН2OH–СНOH–СН2OH | Графическая формула
| Электронная формула
|
| Исторические сведения Впервые получен в 1779 году К.В. Шееле (Швеция) из продуктов гидролиза оливкового масла. | ||
Нахождение в природе
Входит в состав всех жиров и некоторых других веществ, образующих животные ткани.
*Получение
1) Образуется при брожении углеводов (например, глюкозы – С6Н12О6) и гидролизе жиров (как кислотном, так и щелочном) – уравнения не приводятся, вследствие их сложности.
2) СН2Cl–СНCl– СН2Cl +3NaOH 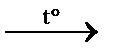 СН2OH–СНOH–СН2OH +3NaCl
СН2OH–СНOH–СН2OH +3NaCl
|
|
Физические свойства
Бесцветная, вязкая, гигроскопичная (см. стр.) жидкость без запаха и со сладковатым привкусом. Не ядовита. Смешивается с водой в любых отношениях. Имеет высокую температуру кипения (tº = 290 ºC).
Химические свойства
1) 2СН2OH–СНOH–СН2OH + 6Na → 2СН2ONa–СНONa–СН2ONa + 3H2↑ замещение
2) 2С3Н8О3 + 7О2 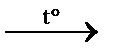 6CО2↑ + 8Н2О горение
6CО2↑ + 8Н2О горение
3) СН2OH–СНOH–СН2OH+ 3HNO3 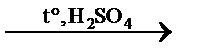 СН2ONO2–СНONO2–СН2ONO2 +
СН2ONO2–СНONO2–СН2ONO2 +
тринитрат глицерина («нитроглицерин»)
+ 3H2O нитрование
4) С3Н8О3 + Cu(OH)2 → глицерат меди (II) – ярко-синий комплекс. Полное уравнение не приводятся, вследствие его сложности.
Применение
Широко используется в кожевенной, текстильной, пищевой и кондитерской промышленностях, в парфюмерии и косметологии, как сырьё для получения лекарственных препаратов (например, 1 % раствор «нитроглицерина» используется, как сосудорасширяющее средство), взрывчатых веществ (например, динамита) и полимеров: лаков, красок, клеев.
ОСНОВНЫЕ СВЕДЕНИЯ
ОБ УКСУСНОЙ КИСЛОТЕ
| Общие сведения | |||
| Молекулярная формула СН3COOH | Графическая формула

| Электронная
формула

| |
|
Нахождение в природе Широко распространена в природе – содержится зелёных листьях растений, в выделениях животных (моче, желчи). Образуется при окислении многих органических веществ, а также при брожении, гниении, скисании вина и пива, содержится в кислом молоке и сыре. | |||
| *Получение 1) С4Н10 + 4[O] 2) С2H5OH + 2[O] 3) СH3CHO + [O] 4) CH3COONa + H2SO4(конц.) | |||
|
Физические свойства Безводная уксусная кислота представляет собой бесцветную кристаллическую массу, напоминающую лёд, поэтому ее называют «ледяной» (впервые получена в 1789 году Т.Е. Ловицем (Россия)). Обычная техническая кислота – представляет бесцветную легкоподвижную жидкость с резким специфическим запахом, отлично растворимую в воде. 70-80 % раствор называют уксусной эссенцией, а 3-9 % раствор пищевым уксусом.
| |||
|
Химические свойства 1) 2CH3COOH + Zn → (CH3COO)2Zn + H2↑ замещение 2) 2CH3COOH + ZnO → (CH3COO)2Zn + H2O обмен 3) CH3COOH + NaOH → CH3COONa + H2O обмен 4) 2CH3COOH + Na2CO3 → 2CH3COONa + CO2↑ + H2O обмен с разложением 5) CH3COOH + C2H5ОН | |||
|
Применение Широко используется в химической промышленности для получения солей – ацетатов, сложных эфиров (например, этилацетата), уксусного ангидрида, лекарственных препаратов, различных полимеров, ядохимикатов, а также в пищевой и консервной промышленностях. | |||
ОСНОВНЫЕ СВЕДЕНИЯ О ЖИРАХ
| ЖИР – это кислородсодержащее органическое веществ, состоящее из остатка глицерина и трёх остатков высших карбоновых кислот. | |
| Исторические сведения Впервые химический состав был установлен в 1817 году М.Э. Шеврелем совместно с А. Браконно (Франция), а первый синтез жира осуществлен в 1854 году П.Э.М. Бертло (Франция) при нагревании глицерина со стеариновой кислотой. | Графическая формула

|
Нахождение в природе
Широко распространены в природе, как в растительном, так и животном мире. В организмах они находятся либо в виде протоплазматического жира – выходят в состав протоплазмы клеток, либо в виде запасного (резервного) жира – входят в состав жировой ткани.
Жир человека содержит до 70 % олеиновой кислоты и 25 % стеариновой кислоты, а жир жвачных животных больше содержит стеариновой кислоты. Оливковое масло содержит до 80 %, а подсолнечное масло – до 40 % олеиновой кислоты.


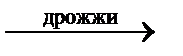 2C2Н5ОН + 2СО2↑ спиртовое брожение глюкозы
2C2Н5ОН + 2СО2↑ спиртовое брожение глюкозы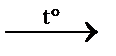 2CO2↑ + 3H2O горение
2CO2↑ + 3H2O горение C2H4↑ + H2O внутримолекулярная дегидратация
C2H4↑ + H2O внутримолекулярная дегидратация C2H5OC2H5 + H2O межмолекулярная дегидратация
C2H5OC2H5 + H2O межмолекулярная дегидратация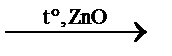 C4H6 + 2H2О + H2↑ реакция С.В. Лебедева
C4H6 + 2H2О + H2↑ реакция С.В. Лебедева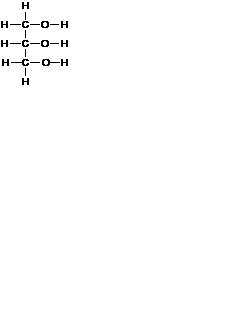

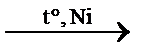 2CH3COOH окисление бутана
2CH3COOH окисление бутана


