Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теоретические основы процесса производства аммиака.
Синтез аммиака из элементов осуществляется по уравнению:
Реакция обратимая, экзотермическая, характеризуется большим тепловым эффектом
Реакция синтеза аммиака протекает с уменьшением объема. Основываясь на принципе Ле Шателье, можно сделать вывод о том, что в условиях равновесия содержание аммиака в смеси будет больше при высоком давлении, чем при низком. Использование константы равновесия позволяет количественно оценить степень предсказываемых изменений по уравнению:
Однако синтез аммиака протекает с заметной скоростью только в присутствии катализаторов в качестве которых обычно применяют Fe, Ru, Re и др. В промышленности нашли применение железные катализаторы, полученные сплавлением оксида железа с промоторами и последующим восстановлением оксида железа. В качестве промоторов применяют оксиды кислотного и аморфного характера – Al2O3, SiO2, TiO2 и др., а также K2O, Na2O, CaO и др. Исследование процесса синтеза аммиака позволило сделать вывод о том, что лимитирующей стадией процесса является хемосорбция азота на поверхности катализатора. Скорость обратимой реакции получения аммиака на большинстве известных катализаторов описывается уравнением Темкина-Пыжова:
где k 1 и k 2 – константы скоростей образования и разложения аммиака; При проведении процесса при атмосферном давлении величина α для промышленных катализаторов в интервале температур 400-500°С равна 0,5. Скорость реакции синтеза аммиака зависит от температуры, давления и состава реакционной смеси. Из уравнения Темкина-Пыжова видно, что скорость прямой реакции синтеза пропорциональна р1,5, а скорость обратной реакции пропорциональна р0,5. Отсюда очевидно, что с ростом давления наблюдаемая скорость процесса увеличивается. И термодинамические, и кинетические факторы свидетельствуют в пользу проведения процесса при высоких давлениях (увеличивается равновесный выход, повышается скорость синтеза). Вместе с тем, повышение давления увеличивает расход электроэнергии на компрессию, повышает требования к машинам и аппарата. При пониженном давлении упрощается аппаратурное оформление процесса, снижается расход энергии, но при этом растут габариты аппаратов, увеличиваются энергозатраты на циркуляцию газа и выделение аммиака, повышаются требования к чистоте синтез-газа.
Технологическое оформление процесса синтеза аммиака В мировой азотной промышленности наибольшее распространение получили установки среднего давления, в которых синтез аммиака ведут на плавленых железных катализаторах при температурах 420-500°С, давлении 25-32 МПа, объемной скорости 15-25 тыс.ч-1. Съем аммиака с 1 м3 катализатора составляет 20-40 тонн/сутки. На рис. 6.10 приведена технологическая схема синтеза аммиака в агрегате мощностью 1360 тонн/сутки на отечественном оборудовании. Свежая азотоводородная смесь, после очистки метанированием, сжимается в центробежном компрессоре до давления 32 МПа и после охлаждения в воздушном холодильнике (на схеме не показан) поступает в нижнюю часть конденсационной колонны 8 для очистки от остаточных примесей СО2, Н2О и следов масла. Свежий газ (СГ) барботируют через слой сконденсировавшегося жидкого аммиака, освобождается при этом от водяных паров и следов СО2 и масла, насыщается аммиаком до 3-5% и смешивается с циркуляционным газом (ЦГ). Полученная смесь проходит по трубам теплообменника конденсационной колонны и направляется в межтрубное пространство выносного теплообменника 4, где нагревается до 185-195°С за счет теплоты газа, выходящего из колонны синтеза. Затем циркуляционный газ поступает в колонну синтеза 2, которая представляет собой аксиальную четырехполочную колонну с предварительным теплообменником и трехполочным выносным теплообменником. В теплообменнике циркуляционный газ нагревается до температуры начала реакции 400-440°С за счет теплоты конвертированного газа и затем последовательно проходит четыре слоя катализатора, в результате чего концентрация NH3 в газе возрастает до 15%. Пройдя через центральную трубу, при температуре 500-515°С, азотоводородоамиачная смесь направляется во внутренний теплообменник, где охлаждается до 330°С. Дальнейшее охлаждение газовой смеси до 215°С осуществляется в трубном пространстве подогревателя питательной воды 3, в трубном пространстве выносного теплообменника 4 до 65°С за счет холодного циркулирующего газа, идущего по межтрубному пространству, а затем в аппаратах воздушного охлаждения 7 до 40°С, при этом часть NH3 конденсируется. Жидкий аммиак, сконденсировавшийся при охлаждении, отделяется в сепараторе 6, а затем смесь, содержащая 10-12% NH3, идет на циркуляционное колесо компрессора 5 азотоводородной смеси, где сжимается до 32 МПа.
Циркуляционный газ при температуре 50°С поступает в систему вторичной конденсации, включающую конденсационную колонну 8 и испарители жидкого аммиака 15. В конденсационной колонне газ охлаждается до 18°С и в испарителях за счет кипения аммиака в межтрубном пространстве до -5°С из трубного пространства испарителя смесь охлажденного циркуляционного газа и сконденсировавшегося NH3 поступает в сепарационную часть конденсационной колонны, где происходит отделение жидкого аммиака от газа и смешение свежий азотоводородной смеси с циркуляционным газом. Далее газовая смесь проходит корзину с фарфоровыми кольцами Рашига, где отделяется от капель жидкого NH3, поднимается по трубам
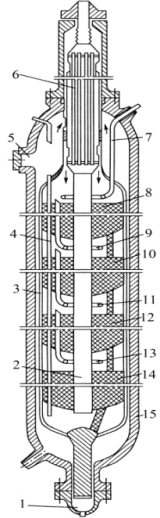
теплообменника и направляется в выносной теплообменник 4, а затем в колонну синтеза 2. Жидкий аммиак из первичного сепаратора проходит магнитный фильтр 16, где из него выделяется катализаторная пыль, и смешивается с жидким аммиаком из конденсационной колонны 8. Затем его дросселируют до давления 4 МПа и отводят в сборник жидкого аммиака 11. В результате дросселирования жидкого NH3 до 4 МПа происходит выделение растворенных в нем газов H2, N2, O2, CH4. Эти газы направляют в испаритель 12 с целью утилизации аммиака путем его конденсации при -25°С. Из испарителя танковые газы и сконденсировавшийся аммиак поступают в сепаратор 13 для отделения жидкого аммиака, направляемого в сборник 11. Для поддержания в циркуляционном газе постоянного содержания инертных газов, не превышающего 10%, производится продувка газа после первичной конденсации аммиака (после сепаратора 6). Продувочные газы содержат 8-9% NH3, который выделяется при температуре 20-30°С в конденсационной колонне 9 и испарителе 10 продувочных газов. Смесь танковых и продувочных газов, после выделения аммиака, используют как топливный газ. На рис. 6.11 показана четырехполочная колонна с аксиальными насадками. Основной поток газа поступает в колонну снизу, проходит по кольцевой щели между корпусом колонны 15 и корпусом катализаторной коробки 3 и поступает в межтрубное пространство теплообменника 6. Здесь синтез-газ нагревается конвертированным газом до 420-440°С и проходит последовательно четыре слоя катализатора 8,10,12,14, между которыми подается холодный байпасный газ. После четвертого слоя катализатора газовая смесь при 500-515°С поднимается по центральной трубе 2, проходит по трубкам теплообменника 6, охлаждаясь при этом до 300-350°С, и выходит из колонны.
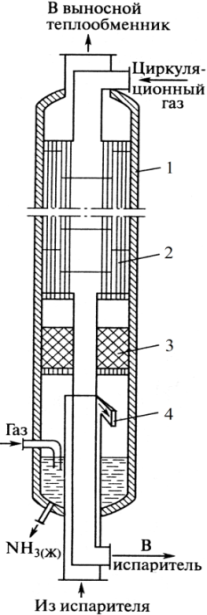
На рис. 6.12 изображена конденсационная колонна. Это вертикальный цилиндрический аппарат с внутренним диаметром 2 метра и высотой 18,9 метра и состоит из теплообменника и сепаратора, размещенного под теплообменником. В межтрубном пространстве размещены перегородки. Охлаждаемый раз идет по межтрубному пространству, а газ после сепарации NH3 – по трубкам. Газ, охлажденный в испарителе, через нижний штуцер поступает в сепарационное устройство 4, в котором создается вращательное движение; при этом частицы жидкости отделяются от газового потока, собираются в нижней части аппарата и непрерывно выводятся. Газ поднимается вверх, проходит отбойник 3, состоящий из слоя колец Рашига, и, проходя трубное пространство, отдает свой холод. Сжиженный газ, входящий через боковой штуцер в нижней части аппарата, барботирует через слой жидкого аммиака, освобождаясь от паров воды и СО2.
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 372; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.112.82 (0.01 с.) |
 .
.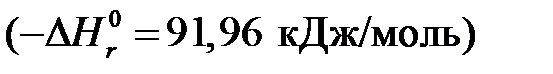 и при высоких температурах становится еще более экзотермической
и при высоких температурах становится еще более экзотермической  . Согласно принципу Ле Шателье при нагревании равновесие смещается влево, в сторону уменьшения выхода аммиака. Изменение энтропии в данном случае тоже отрицательно
. Согласно принципу Ле Шателье при нагревании равновесие смещается влево, в сторону уменьшения выхода аммиака. Изменение энтропии в данном случае тоже отрицательно  и не благоприятствует протеканию реакции. При отрицательном значении ∆ S повышение температуры уменьшает вероятность протекания реакции, так как ∆ S определяет характер зависимости ∆ G от температуры согласно уравнению:
и не благоприятствует протеканию реакции. При отрицательном значении ∆ S повышение температуры уменьшает вероятность протекания реакции, так как ∆ S определяет характер зависимости ∆ G от температуры согласно уравнению: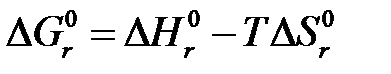 .
.
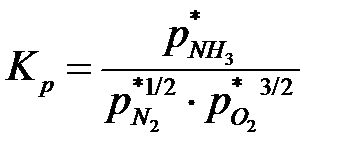 .
.
 ,
,
 - парциальные давления азота, водорода, аммиака; α – постоянная удовлетворяющая равенству 0<α<1.
- парциальные давления азота, водорода, аммиака; α – постоянная удовлетворяющая равенству 0<α<1.