Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Явления при которых из одних веществ получаются другие называются химическими реакциями.Содержание книги
Поиск на нашем сайте Признаки и условия течения химических реакций. По каким внешним признакам мы отличаем химические явления от физического? При химических реакциях из одних веществ образуются другие. По исчезновению признаков первых и появлению признаков вторых, а также по выделению или поглощению энергии мы и заключаем, что произошла химическая реакция. При прокаливании медной пластинки на ее поверхности появлялся черный налет; при продувании углекислого газа через известковую воду выпадал белый осадок; при горении древесины появлялись капли воды на холодных стенках сосуда, при горении магния получался порошок белого цвета. Изменение окраски, запаха, образование осадка, появление газа, выделение или поглощение энергии — все это признаки химических реакций. Рассматривая химические реакции, мы всякий раз обращали внимание не только на то, как они протекают, но и на условия, необходимые для начала и течения реакций. Что нужно сделать, чтобы началась химическая реакция? Для этого прежде всего необходимо реагирующие вещества привести в соприкосновение. Чем более измельчены вещества, чем больше поверхность соприкосновения их друг с другом, тем быстрее идет реакция между ними. Кусок сахара трудно зажечь, а тонко измельченный и распыленный в воздухе сахар сгорает мгновенно, со взрывом. Раздробить вещество на мельчайшие частицы можно растворением. Поэтому предварительное растворение исходных веществ облегчает проведение химических реакций между ними. В некоторых случаях соприкосновения веществ, например железа с влажным воздухом, достаточно, чтобы произошла реакция. Но часто одного соприкосновения веществ для этого недостаточно. Так, медь не вступает в реакцию с кислородом воздуха при невысокой температуре порядка 20-25 °С. Чтобы вызвать реакцию соединения меди с кислородом, надо нагреть вещества. На возникновение и течение химических реакций нагревание влияет по-разному. Для одних реакций требуется непрерывное нагревание. Прекращается нагревание — прекращается и химическая реакция. Это мы наблюдали на примере разложения сахара. В других случаях нагревание требуется лишь для возникновения реакции, оно дает ей как бы толчок, а дальше реакция течет сама собой. Так происходило при горении магния, дерева и других горючих веществ. Элементарное введение в строение электронной оболочки атома Электронная оболочка, окружающая ядро атома, имеет слоистое строение и формируется по определенным строгим правилам. Каждый электрон в атоме занимает определенное место, ему присваивается адрес, состоящий из четырех квантовых чисел: главного (n), орбитального (l), магнитного (ml) и спинового (ms). Будем проводить аналогию с домом, в котором есть этажи, квартиры и комнаты. На самом деле значения квантовых чисел имеют глубокий квантово-механический смысл, но обсуждать его в данном томе мы не будем. Квантовые числа Главное квантовое число (n) — определяет общую энергию электрона в слое, это номер слоя. На номер слоя налагаются такие же ограничения, как и на номер Вашей квартиры, номер может быть только целым и положительным числом от 1 до бесконечности. При n равном бесконечности электрон уже не принадлежит данному атому.
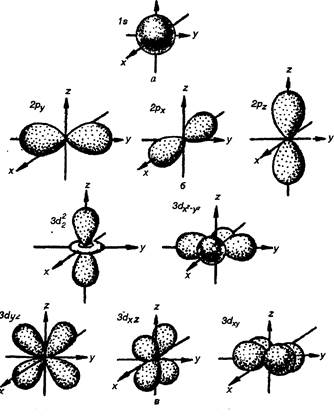
Рис. 1.5. Формы электронных облаков s-, p- и d-орбиталей. Каждый электронный слой в атоме имеет свою емкость, т. е. может содержать не больше определенного числа электронов, причем, чем дальше слой от ядра, тем электронов в нем может быть больше, максимальное число электронов в слое можно рассчитать по формуле: N = 2n2
Каждое значение главного квантового числа это как бы этаж в доме, а на каждом этаже есть квартиры, состоящие из разного числа комнат. Чисто квартир на этаже определяет орбитальное квантовое число l. Орбитальное квантовое число l. Оно может принимать целочисленные значения от 0 до n–1 (l = 0, 1,..., n–1). Обычно численные значения l принято обозначать следующими буквенными символами:
В этом случае говорят о s-, p-, d-, f-состояниях электронов, или о s-, p-, d-, f-орбиталях, квартиры в доме состоят из разного числа комнат (атомных орбиталей), на одной атомной орбитали могут располагаться не более двух электронов. Атомная орбиталь (АО) — область пространства в котором вероятность нахождение электрона максимальна и равна 90%. АО можно представить в виде электронных облаков различной формы. Форма электронного облака зависит от значения орбитального квантового числа l. При l = 0 (s-орбиталь) электронное облако имеет шаровидную форму (сферическая симметрия) и не обладает направленностью в пространстве (рис. 1.5). При l = 1 (p-орбиталь), электронное облако имеет форму гантели, т. е. форму тела вращения, полученного из «восьмерки» (рис. 1.5). Формы электронных облаков d- и f-электронов намного сложнее, они показаны на рис. 1.5 и 1.6. Магнитное квантовое число ml. Оно может принимать значения целых чисел, как положительных, так и отрицательных, от - l до + l, включая 0, т. е. всего (2 l + 1) значений. Каждое значение ml определяет атомную орбиталь, поэтому для s-электронов l = 0, ml = 0 одна орбиталь, для p-электронов l = 1, ml = 0, ±1 три орбитали, для d-электронов l = 2, ml = 0, ±1, ±2 пять орбиталей, для f-электронов l = 3, ml = 0, ±1, ±2, ±3 семь орбиталей. Спиновое квантовое число, является индивидуальной характеристикой электрона. При движении электрона (заряженной частицы) возникает магнитное поле, которое взаимодействует с магнитными полями других электронов, как полюса магнита ¾ одинаковые отталкиваются, разноименные притягиваются. Спиновое квантовое число имеет два значения +1/2 и -1/2.
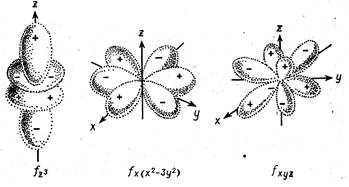
Рис. 1.6. Некоторые формы электронных облаков f-орбиталей.
|
||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 121; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.009 с.) |