
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Виды электрохимической коррозии
Разные фазовые составляющие, присутствующие в структуре сплава, находясь в электролите, приобретают разные по величине и знаку электродные потенциалы. Чем больше различие в электродных потенциалах отдельных фазовых составляющих, тем активнее будет протекать коррозионный процесс и коррозионное разрушение сплава. Электрохимическая гетерогенность поверхности металла является причиной коррозии (например, коррозионная пара перлит: феррит- анод, цементит - катод) Более коррозионностойкими являются сплавы со структурой однородного твердого раствора. Однако даже в случае однородной структуры коррозионные пары могут возникать за счет, различия остаточных напряжений в отдельных зернах, разли- чия в размерах зерен и других факторов. Особенно сильно электрохимическая коррозия развивается в случае контакта в конструкции разнородных материалов с разными потенциалами (например, коррозия стальных деталей в контакте с медными или магниевых сплавов в контакте со сталью). В пластинке железа покрытой цинком, при его разрушении, железо будет катодом. Цинк, разрушаясь, защищает железо от коррозии, чем и объясняется долговечность строительной жести, домашних ведер, оцинкованных кузовных листов и др. В случае однофазного материала, например чистого металла или однородного твердого раствора, коррозия распространяется равномерно по всей поверхности детали - происходит так называемая общая или равномерная коррозия. Обработка, ведущая к гомогенизации структуры, делает сплав более устойчивым против электрохимической коррозии. Примером таких обработок является закалка хромоникелевой коррозионностойкой стали или отжиг оловянистых бронз, имеющих после литья неоднородное строение вследствие ликвации. Наоборот, нагрев сплавов, приводящий к распаду пересыщенного твердого раствора и выделению частиц второй фазы, снижает коррозионную стойкость. Разность потенциалов отдельных составляющих микроструктуры способствует электрохимической коррозии. В неоднородных металлах коррозия носит местный характер, охватывая отдельные анодные участки их поверхности с низким значением электродного потенциала. К местной коррозии относятся питтинг, или точечная коррозия, пятнистая и язвенная ее разновидности. Очаги местной коррозии являются концентраторами напряжений. Анодными участками могут быть границы зерен и фаз, в то время как зерна сами по себе являются катодами. В этом случае развивается наиболее опасный вид коррозии - межкристаллитная коррозия (МКК).
Она почти незаметна с поверхности и распространяется в глубь металла по границам зерен. В результате межкристаллитной коррозии нарушается связь между зернами, при постукивании по металлу пропадает характерный металлический звук, и после приложения нагрузки металл легко разрушается. Межкристаллитная коррозия высокохромистой стали обусловлена выделением при повышенных температурах по границам зерен карбидов типа Сr23С6. Эти карбиды образуются в результате диффузии углерода из всего объема зерна, а хрома - только с приграничных областей. Углерод перемещается по межузельному механизму диффузии (по механизму внедрения), который по сравнению с перемещением атомов по механизму замещения характеризуется высокой подвижностью. Это приводит к снижению содержания хрома в приграничных областях ниже его критической концентрации 12-14 % и скачкообразному падению электродного потенциала с +0,2 до -0,6 В. Границы зерен становятся анодом по отношению к металлу внутри зерен. Эффективным средством, подавляющим межкристаллитную коррозию, является максимальное снижение содержания углерода и введение в сталь таких сильных карбидообразующих элементов, как титан или ниобий, обладающих большим сродством к углероду, чем хром. При одновременном действии коррозионной среды и нагрузки или остаточных напряжений возникает коррозия под напряжением, проявляющаяся в виде коррозионного растрескивания или сетки трещин. Места концентрации напряжений имеют более низкий электродный потенциал и приобретают характер анодных участков. Известно, что в поврежденных местах кузовов автомобилей, а также в местах деформаций продукты коррозии появляются чаще всего. Высокие остаточные напряжения являются причиной ускоренной коррозии сварных швов, околошовной зоны, болтовых, заклепочных и других соединений.
Большое влияние на процесс коррозии в водных средах оказывает растворенный в жидкости кислород. При достаточном содержании кислорода на поверхности образуется защитная оксидная пленка, повышающая электродный потенциал металла. Наиболее опасные анодные зоны создаются в местах плохой аэрации, где затруднен доступ кислорода из воздуха. Хорошо известно, что та часть стальной плиты, которая находилась под слоем песка, корродирует в большей степени по сравнению с той частью, которая оставалась под непосредственным влиянием атмосферы. Коррозионные явления усиливаются при наложении анодной напряженности на структурную. Состав атмосферы также оказывает влияние на коррозию сплавов. В городах, где воздух загрязнен промышленными газами, коррозия проявляется значительно сильнее, чем в сельской местности. Для стальных деталей особенно вредными являются сернистый газ SО2, сероводород H2S, хлор С12 и хлороводород HCI. Методы защиты от коррозии: нанесение защитных покрытий и пленок; изменение электрохимического потенциала защищаемого материала по отношению к среде на границе фаз; модификация коррозионной среды. В качестве защитных покрытий применяют металлические и неметаллические покрытия. Металлические покрытия делятся на две группы: катодные(электрохимический потенциал которых в данных условиях больше, чем у защищаемого металла) и анодные(электрохимический потенциал которых в данных условиях меньше, чем у защищаемого металла). Катодные покрытия.защищают металл благодаря его изоляции от внешней среды, следовательно выполняют свою роль только при наличии полной сплошности, поэтому их делают сравнительно большой толщины. Защитные свойства анодных покрытий состоят не только в изоляции от внешней среды, но и в электрохимическом воздействии (в случае нарушения покрытия и образовании коррозионного элемента, защищаемый металл, являющийся катодом не разрушается). Металлические покрытия наносят электроосаждением, погружением в расплавленные металлы, металлизацией напылением, химическим осаждением солей, диффузией и т.д. Неметаллические покрытия применяют в случае возникновения химических реакции металла в соответствующих средах. К ним относят оксидные алюминиевые покрытия, получаемые в ходе электролитического процесса, фосфатные покрытия, получаемые в ходе погружения изделия в разбавленный раствор фосфорной кислоты и кислых фосфатов цинка или магния, а также керамические покрытия и стекловидные эмали. Фосфатные покрытия применяются как правило с дополнительным нанесением красок и лаков. К органическим покрытиям относятся разнообразные лакокрасочные материалы. Коррзионностойкие стали Для защиты от коррозии широко применяется явление пассивации, которое возникает при образовании тонких прочных и непрерывных оксидных пленок, равномерно покрывающих поверхность материала. Переход от активного состояния к пассивному связан с ростом электродного потенциала. Устойчивость против коррозии повышается при введении в состав стали хрома, алюминия, кремния. Эти элементы образуют непрерывную прочную оксидную пленку и повышают электродный потенциал. Алюминий и кремний повышают хрупкость стали и применяются реже хрома. Из рис.14.1 следует, что при содержании хрома более 12 % сталь резко изменяет электродный потенциал с электроотрицательного (-0,6 В) на электроположительный (+0,2 В). На поверхности образуется защитная плотная пленка оксида Сr203.
Сталь, содержащая 12-14 % Сr, устойчива против коррозии в атмосфере, морской воде, ряде кислот, щелочей и солей. Кроме хрома, в состав коррозионностойких сталей вводят также другие элементы - чаще никель. С ростом содержания хрома коррозионная стойкость стали растет. Коррозионностойкие стали обычно делят на хромистые ферритные, содержащие 12-25 % Сr и 0,07-0,2 % С и хромистые мартенситные, содержащие 12-18 % Сr и 0,15-1,2 % С, а также аустенитные стали, содержащие 12-18 % Сr, 8-30 % Ni и 0,02-0,25 % С. 14.2.1 Хромистые нержавеющие стали Хромистые стали после охлаждения на воздухе имеют ферритную, мартенситно-ферритную (с содержанием феррита более 10%) и мартенситную структуру. Они коррозионностойки при температуре до 300 °С в водопроводной воде, влажной атмосфере, растворах азотной кислоты и многих органических кислотах. В морской воде хромистые стали подвержены коррозионному растрескиванию. Марки, химический состав и свойства хромистых сталей приведены в табл.14. 1. Хромистые стали при нагреве и охлаждении претерпевают фазовое ( Таблица14.1 Свойства хромистых коррозионностойких сталей (ГОСТ 5632—81)
Отпуск не приводит к существенному обеднению твердого раствора хромом, и коррозионная стойкость сохраняется на высоком уровне.
Термическая обработка мартенситных сталей, например 30Х13,40Х13 состоит из закалки от температуры 1000 °С в масле и низкого отпуска при температурах 200-300 °С. После такой обработки стали имеют структуру отпущенного мартенсита. Из них изготавливают режущий, формовочный, измерительный и хирургический инструмент, пружины, а также предметы домашнего обихода. Для изготовления подшипников, втулок, ножей и других деталей, работающих на износ в агрессивных средах, применяют сталь 95X18. После закалки с 1000-1050 °С в масло и отпуска при 200-300 °С сталь имеет высокую твердость - не менее 55 HRC. Мартенситно-ферритные стали закаливают с температуры 1000 °С и подвергают высокому отпуску (600-700 °С) для получения сорбитной структуры. В отожженном состоянии эти стали пластичны, имеют повышенную ударную вязкость и могут подвергаться не только горячей, но и холодной обработке давлением. Они применяются для изготовления деталей с повышенной пластичностью, подвергающихся ударным нагрузкам, работающих в слабоагрессивных средах. К таким деталям относятся клапаны гидравлических прессов, мешалки, валы и шнеки в пищевой промышленности. Ферритные стали подвергают отжигу при температуре 700-800 °С для получения однородного твердого раствора и увеличения коррозионной стойкости. Из сталей марок 08X13, 12X17, 15Х25Т, 15X28 изготавливают оборудование и оснастку предприятий пищевой и легкой промышленности, трубы теплообменной аппаратуры, работающие в агрессивных средах. Сварке ферритные стали подвергают редко, поскольку она приводит к росту зерна и снижению коррозионной стойкости. 14.2.2 Хромоникелевые коррозионностойкие стали Хромоникелевые коррозионностойкие стали после охлаждения на воздухе имеют аустенитную, аустенитно-мартенситную и аустенитно-ферритную (феррита более 10 %) структуру. Широко применяемые стали типа 12Х18Н10Т, 12Х18Н9, 04Х18Н10, ОЗХ18Н12,17Х18Н9 обычно содержат 18 % Сr и 9-12 % Ni (табл. 14.2.). Они имеют более высокую коррозионную стойкость по сравнению с хромистыми сталями. Термообработка этих сталей заключается в закалке от температуры около 1100 °С в воде без отпуска. Высокая температура при закалке необходима для растворения карбидов и получения структуры однородного аустенита. После закалки стали имеют следующие основные свойства: чисто аустенитную структуру, низкую твердость, высокую пластичность; они немагнитны, хорошо деформируются и свариваются. Высокая технологичность сталей позволяет широко использовать их в качестве конструкционного материала. При медленном охлаждении хромоникелевые стали приобретают многофазную структуру, в которой кроме аустенита присутствует небольшое количество феррита и карбидов. Такая структура отрицательно сказывается на коррозионной стойкости и пластичности. Состояние однофазного аустенита с сохранением всего хрома в твердом растворе обеспечивает сталям максимальную коррозионную стойкость. Пластичность на уровне δ= 35-40 % позволяет подвергать их холодной пластической деформации с наклепом и повышением прочности при сохранении коррозионной стойкости почти на прежнем уровне.(рис.14.2)
Содержание углерода в коррозионностойких аустенитных сталях ограничено, и желательно, чтобы оно было ниже предела растворимости углерода в легированном никелем аустените при 20 °С, составляющего 0,04 %. Присутствие в стали более высоких концентраций углерода может приводить к образованию карбидов хрома типа Сг Таблица 14.2 Состав и свойства закаленных коррозионностойких сталей аустенитного класса (ГОСТ 5632-81)
и создается двухфазная структура. При этом снижается коррозионная стойкость стали. Для предотвращения образования карбидов хрома, особенно при технологических нагревах, связанных с проведением операций сварки или пайки и опасностью возникновения межкристаллитной коррозии, в сталь вводят дополнительно титан, ниобий или тантал. Эти элементы связывают углерод в карбиды типа TiC, NbC, TaC, оставляя хром в твердом растворе. Необходимое количество титана для введения в сталь определяют по формуле, Ti = (С - 0,02) • 5, где С - содержание углерода в стали. Стали, не склонные к межкристаллитной коррозии, называют стабилизированными. Эффект стабилизации может быть достигнут, помимо введения сильных карбидообразующих элементов, снижением содержания углерода ниже 0,04 %. Пассивации Cr - Ni аустенитных сталей способствует введение 0,5-1,5 % Мо. Введение таких количеств молибдена в сталь 12Х18Н10Т уменьшает плотность критического тока пассивации в 10 раз. Аустенитные стали с молибденом не подвержены точечной коррозии в морской воде. В пищевой промышленности хромоникелевые коррозионно-стойкие стали применяют в изделиях, контактирующих с агрессивными пищевыми средами (емкости, трубопроводы и т. д.). Б холодильной и криогенной технике они используются для изготовления сосудов для хранения жидких газов, корпусов, адсорберов ацетилена, деталей центробежных машин. Хромоникелевые коррозионностойкие стали содержат дефицитный и дорогостоящий никель и поэтому имеют высокую стоимость. В ряде случаев применяют более дешевые стали, в которых весь никель или часть его заменены марганцем. До температур -196°С и в слабоагрессивных пищевых средах вместо стали 12Х18Н10Т может быть использована сталь 10Х14Г14Н4Т. Также в целях экономии никеля промышленность выпускает двухслойные стали, в которых в основном слое использованы низколегированные или углеродистые стали, а в плакирующем слое - хромоникелевые коррозионностойкие стали и цветные металлы. 14.2.3 Хромистые стали, легированные азотом С помощью атомов внедрения (углерода и азота), располагающихся в междоузлиях решетки, можно существенно увеличить прочностные свойства аустенитных сталей. Учитывая отрицательное влияние углерода на коррозионную стойкость, увеличение его содержания нецелесообразно. В отожженном и закаленном состояниях концентрация азота в хромоникелевых аустенитных сталях может быть доведена до 0,40 %, а при выплавке стали под давлением - до 1,0 %. При этом предел текучести при комнатной температуре может возрасти до 500 МПа, а временное сопротивление - до 1000 МПа. Азот повышает стабильность аусте-нита, поэтому для повышения коррозионной стойкости можно использовать более высокие концентрации хрома и молибдена, не увеличивая склонность стали к выделению интерметаллидных фаз. Примером может служить сталь ОЗХ20Н16АГ6, используемая в криогенной технике. Хромистые коррозионно-стойкие стали, легированные азотом. Азот, растворяясь в железе или в сложных композициях на его основе, придает им практически важные, а иногда даже уникальные свойства. Процесс азотирования поверхностного слоя стальных изделий в твердом состоянии для обеспечения высокой износостойкости деталей машин широко применяется в промышленности. Успешно использовать азот для объемного легирования сталей научились относительно недавно. Первые работы по легированию стали азотом относятся к тридцатым годам нашего века. Академик А.М. Самарин первый выдвинул идею замены в коррозионно-стойких сталях никеля азотом. Несмотря на доступность, азот не применяют столь же широко как углерод, поскольку технологические процессы насыщения железа азотом сложнее, чем углеродом, особенно при использовании традиционной слитковой технологии. Ниже перечислены основные методы введения азота в сплавы на основе железа, которые в настоящее время нашли применение в промышленных условиях. 1. Насыщение азотом расплавов а) плавка при нормальном давлении азота над расплавом (на воздухе) с использованием в качестве шихтовых материалов азотированных ферросплавов (Fe—Cr, Fe—Mn, Fe—V и др.) или металлов; б) плавка при повышенном давлении азота над расплавом. Ниже приведены основные способы насыщения жидкой стали азотом, табл.14. 3 (цифры ориентировочные): Т а б л и ц а 14.3. Способы насыщения жидкой стали азотом
*По сравнению со сталью, полученной при нормальном давлении азота. В индукционных печах можно создавать давление азота над расплавом до 100 атм, что по закону Сивертса дает "пересыщение" азотом в 10 раз. Так, например, в легированных коррозионно-стойких сталях растворимость азота после кристаллизации расплава при атмосферном давлении составляет 0,25%, а при давлении ЮС атм. -2,5%, 2. Насыщение азотом в твердом состоянии а) азотирование (объемное или поверхностное) компактного материала или порошков; б) горячее прессование в газостатах под давлением азота смеси порошков сплава заданного состава. Необходимо отметить, что азот, кроме придания стали особых свойств, стабилизирует γ-Fe. Поэтому при легировании сталей азотом возможна экономия не только элементов — γ -стабилизаторов (никель, марганец), но и дорогих и дефицитных- молибдена или вольфрама. В последнее десятилетие азот используют для легирования практически всех типов сталей, но в большей мере — высоколегированных коррозионно-стойких, в которые азот вводят в виде азотированного хрома или феррохрома. Для получения необходимой концентрации азота в сталях с малым содержанием хрома следует использовать рассмотренные выше специальные приемы азотирования. Азот широко применяют для легирования аустенитных и аустенитно-ферритных коррозионно-стойких сталей, так как он позволяет улучшить коррозионные и механические свойства сталей, уменьшить расход дефицитных легирующих элементов. Азот, так же как и углерод, образует с железом твердый раствор типа внедрения. Диаграммы состояния систем Fe-C и Fe-N имеют большое сходство. Эти диаграммы свидетельствуют о наличии эвтекто-идных превращений соответственно при 738 и 592°С. Указанные превращения обусловливают сходство в структурах, формирующихся в результате термической обработки в сплавах Fe—С и Fe—N. Более низкая температура эвтектоидного превращения у Fe—N сплавов обусловливает возможность получения более дисперсных фаз, составляющих металлографическую структуру. Нельзя не отметить, что предельная растворимость азота как в у-, так и в y-Fe выше, чем углерода. Самая большая сложность получения в затвердевшем железном сплаве большого количества азота заключается в том, что при температурах в интервале кристаллизации происходит резкое снижение растворимости азота в стали С помощью легирования растворимость азота можно повысить, выбрав составы стали, в которых кристаллизация из жидкой фазы будет происходить с образование γ-фазы, в которой растворимость азота весьма высока. В результате переохлаждения может происходить бездиффузионная перестройка г.ц.к. кристаллической решетки g-фазы в α-фазу, которая будет пересыщена азотом или 'углеродом. При зтом возникают тетрагональные искажения кристаллической решетки a-Fe. С повышением содержания азота тетрагональные искажения в a-Fe, образующемся по мартенситной реакции при охлаждении g-Fe, увеличиваются. Тетрагональные искажения a-фазы азот увеличивает несколько меньше, чем углерод (предполагают, что это связано с меньшими размерами атома азота). Азот при равном содержании с углеродом в высоколегированных железных сплавах обеспечивает повышенные технологическую пластичность и значение предела текучести. Он повышает способность к деформационному упрочнению и существенно увеличивает: способность металла сопротивляться распространению трещин в процессе разрушения, циклическую прочность, износо- и коррозионную стойкость. Стали, легированные азотом, подразделяют на два типа: с равновесным и "сверхравновесным" содержанием азота. Стали с равновесным содержанием азота получают в условиях кристаллизации на воздухе при обычном давлении азота. Стали со "сверхравновесным" содержанием азота — при использовании способа выплавки с повышенным давлением азота над расплавом или одного из способов твердофазного азотирования. Наибольшее распространение получили азотосодержащие стали, легированные хромом. При высоком содержании азота и хрома они могут иметь стабильную аустенитную структуру. При содержании 21% Сr достаточно добавки примерно 0,3% N для того, чтобы превратить структуру стали из мартенситной в аустенитную, т.е. сохранить до комнатной температуры высокотемпературную γ-модификацию железа. Для рассмотрения совместного влияния азота и хрома на аустенитизацию стали можно использовать эмпирическую зависимость: % γ =a+b(%Cr+18% N).При значениях (%Cr+18%N) вплоть до ~26% сталь имеет мартенситную структуру, а более 33% — аустенитную. Упрочнение таких сталей достигается при изменении концентрации азота в γ -твердом растворе. Растворение азота значительно увеличивает период кристаллической решетки аустенита, что способствует повышению прочности, но при этом снижается пластичность стали. Тем не менее даже при большом значении периода кристаллической решетки аустенита α=0,3620 нм (это соответствует содержанию в стали примерно 1.6% N) еще сохраняется достаточный запас пластичности, а прочность (s0.2 ) возрастает до 1150 МПа (что в 4 раза больше, чем у обычной аустенитной стали типа Х18Н9). Дополнительное повышение прочности азотосодержащих сталей может обеспечить процесс дисперсионного твердения с выделением нитридных (или карбонитридных) фаз из пересыщенного азотом γ -твердого раствора при термической обработке. Наибольшее упрочнение при одинаковом снижении пластичности обеспечивает нитрид ванадия. Стали, содержащие в структуре дисперсные частицы нитрида ванадия, могут иметь предел текучести в 4—5 раз более высокий, чем традиционные коррозионно-стойкие стали аустенитного класса и достигать 1400 МПа при достаточно высоком запасе пластичности. Предел текучести сварного соединения стали, полученного с использованием электрода, соответствующего по составу основному металлу, без специальных приемов сохранения азота (в наплавленном металле содержание азота составило 0.73%) составляет более 800 МПа. При равном суммарном содержании элементов внедрения (азота или углерода) прочность азотосодержащих сталей с мартенситной структурой выше, чем угеродосодержащих. Азотосодержащая сталь при всех температурах отпуска оказывается более прочной, чем сталь с эквивалентным содержанием углерода, в то время как пластичность у рассматриваемых сталей практически одинаковая. Важнейшей характеристикой работоспособности стали в конструкциях, испытывающих переменные нагрузки, является циклическая прочность (выносливость). Результаты испытания на выносливость мартенситной хромоазотистой стали, содержащей всего лишь 0,13% N, показали, что напряжение до разрушения образцов при числе циклов нагрузки 107 составляет около 770 МПа. При такой усталостной прочности сталь может конкурировать с легкими сплавами по высокой удельной прочности. У хромоазотистых мартенситных сталей очень высока способность к пластической деформации. Металл отлично деформируется в широком интервале температур (от 20 до 1200° С). После прокатки при 400° С твердость стали составляет HRC 52, что соответствует прочности -2000 МПа. Сталь сохраняет высокий уровень прочности вплоть до 400° С.. При более высоких температурах ее прочность снижается по двум причинам. Во-первых, происходит огрубление мельчайших частиц нитридов, которые образуются в стали при нагреве до 300—400° С; во-вторых, развивается обратное превращение мартенсита в аустенит (более пластичную и менее прочную модификацию железа). Удельные прочность и жесткость (отношение соответственно прочности и модулей упругости к плотности) — важные характеристики стихи эксплуатационных качеств конструкционных материалов. Для практического применения очень важно, что при равной удельной прочности хромистая сталь со структурой азотистого мартенсита заметно превосходит коррозионно-стойкие сплавы других типов по вязкости разрушения. Она сохраняет высокую удельную прочность вплоть до 400—450° С. Выше 500° С по удельной прочности некоторые преимущества перед рассматриваемой мартенситной сталью с 0,13% N имеет высокопрочный титановый сплав. Однако это не означает, что титановые сплавы являются полноценными конкурентами таких сталей в качестве конструкционного материала. Это подтверждает рис.14.3, на котором показана удельная усталостная прочность (прочность, которая сохраняется после 107 циклов нагрузки, отнесенная к плотности) и удельная жесткость (величина модуля упругости, отнесенная к плотности) для хромоазотистой стали (с содержанием не более 0,13% N) и некоторых сплавов алюминия (А16), магния (МА5) и титана (ВТ22). Видно, что по усталостной прочности титановый сплав несколько превосходит сталь, но по удельной жесткости этот сплав существенно уступает азотистой стали из-за низкого модуля упругости титана. Стали со сверхравновесным содержанием азота имеют большие перспективы практического применения. Низкоуглеродистые хромистые стали, содержащие азот в количествах, превышающих равновесное в несколько раз, могут претерпевать при охлаждении из области γ-фазы как "перлитоподобное" высокотемпературное превращение, так и низкотемпературное превращение мартенситного типа. Прочностные свойства низколегированной стали 0Х3А (0,19%N) со сверхравновесным содержанием азота, полученная методом литья с противодавлением азота (1,6 МПа), в сравнении со свойствами конструкционной стали 18Х2Н4ВА, при практически равном содержании элементов внедрения (соответственно 0,19%N или 0,18% С) существенно выше, при примерно одинаковой пластичности. Азотистые стали имеют более мелкое зерно, следовательно их хладостойкость выше, чем углеродистых сталей. Наибольшее применение получат высокоазотистые стали (сплавы) с аустенитной структурой. Для стабилизации аустенита в этих сплавах достаточно из числа элементов стабилизаторов аустенита использовать только азот. Сплавы, содержащие ~1%N и 18-24% Cr имеют предел текучести 850-900МПа, при δ= 25-50% (в зависимости от термической обработки). При прокатке прочность сплавов может быть доведена до 2500-2800МПа. Отличительной особенностью хромоазотистых аустенитных сплавов (Х18А1,3) является высокое сопротивление абразивному износу, обусловленное тем же механизмом, что и у стали Гатфильда, содержащей (1,1% С и 13% Мn). По абсолютному уровню износостойкости хромоазотистые аустенитные сплавы могут в 2-2,5 раза превосходить стали Гатфильда, и износостойкость их в несколько раз выше, чем у стали 95Х18 с мартенситной структурой. Недостатком сталей является распад пересышенного азотом γ- твердого раствора при тепловых выдержках в широком температурном интервале, т. е. идет процесс образования γ- твердого раствора с равновесным содержанием азота и нитрида хрома. Образующаяся при этом перлитоподобная структура вызывает снижение пластичности и вязкости. Однако разработанные способы обработки позволяют получить в структуре сплавов частицы нитридов хрома не пластинчатой, а зернистой формы. При наличии такой структуры уровень прочности и пластичности остаются удовлетворительными, что позволяет оценивать эти сплавы как конструкционные материалы нового поколения.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 154; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.212.145 (0.078 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
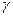
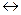
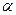 )-превращение, что позволяет их упрочнять, не теряя коррозионной стойкости. Прочность после закалки возрастает с увеличением содержания углерода.
)-превращение, что позволяет их упрочнять, не теряя коррозионной стойкости. Прочность после закалки возрастает с увеличением содержания углерода.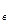 ,МПа
,МПа
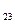 С
С 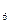 , вследствие чего твердый раствор обедняется хромом
, вследствие чего твердый раствор обедняется хромом


