Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема № 6: растворы. Массовая доля растворенного вещества
Растворы представляют собой однородную систему, состоящую из двух и более компонентов и продуктов их взаимодействия. Концентрация раствора это содержание растворенного вещества в определенной массе или объеме раствора (или растворителя). Массовая доля (ω) – это отношение массы растворенного вещества к общей массе раствора. Она выражается в долях от единицы или в процентах. Математическое выражение для расчета массовой доли:
Масса раствора складывается из массы растворенного вещества и растворителя, как правило воды: m (р-ра) = m (в-ва) + m (H 2 O) Растворы характеризуются важной величиной – плотностью. Плотность (ρ) –это масса одной единицы объема. Измеряется в г/см3 или г/мл. Зная плотность и объем раствора, можно вычислить массу раствора, преобразуя формулу: Задача 1. Вычислить массовую долю хлорида натрия в растворе, полученном при растворении 25 г соли в 475 г воды.
Задача 2. Вычислите массу гидроксида натрия, необходимого для приготовления 400 г 20 %-го раствора гидроксида натрия.
Контрольное задание № 6 «Растворы. Массовая доля растворенного вещества» Варианты заданий 1. Вычислить массовую долю раствора, полученного при растворении 30г вещества в 600 г воды. 2. Смешали 0,4 г соли и 200 мл воды. Какова массовая доля соли в полученном растворе? 3. Какую массу соли и объем воды необходимо взять для приготовления 70 г 2 % раствора? 4. Смешали 20 г сахара и 250 мл воды. Какова массовая доля сахара в полученном растворе? 5. Смешали 2 г соли и 140 мл воды. Какова массовая доля соли в полученном растворе?
6. Какую массу соли и объем воды необходимо взять для приготовления 60 г 1 % раствора? 7. Смешали 0,5 г соли и 300 мл воды. Какова массовая доля соли в полученном растворе? 8. Смешали гидроксид натрия NaOH в количестве 1 моль с 1 л воды. Какова массовая доля гидроксида натрия в полученном растворе? 9. Смешали нитрат натрия NaNO3 в количестве 0,1 моль с 0,5 л воды. Какова массовая доля нитрата натрия в полученном растворе? 10. При выпаривании раствора массой 500 г образовалось 25 г кристаллической соли хлорида натрия. Вычислите массовую долю соли в исходном растворе. 11. Какую массу соли и объем воды необходимо взять для приготовления 70 г 2 % раствора? 12. После выпаривания 200 г раствора соли получили 3 г кристаллической соли. Какова массовая доля растворенного вещества в растворе? 13. Для приготовления раствора сульфата меди (II) использовали 50г соли и 450г воды. Определите массовую долю сульфата меди(II) в полученном растворе. 14. Сколько хлорида магния содержится в 800 мл раствора с массовой долей MgCl2 10% (пл. 1,06 г/см3)? 15. Какую массу поваренной соли и воды необходимо взять для приготовления 300г раствора с массовой долей 15%? 16. Вычислить массовую долю раствора, полученного при растворении 30г вещества в 600 г воды. 17. Вычислите массовую долю (в %) хлороводорода в растворе соляной кислоты, содержащем 14,6 кислоты и 385,4 г воды. 18. Сколько граммов гидроксида калия содержится в растворе объемом 200 мл с массовой долей КОН 10%, плотность которого равна 1,09 г/см3. 19. Вычислить массовую долю раствора содержащего 2 моля соды Na2CO3 в 0,5 л воды? 20. Какую массу соли и объем воды необходимо взять для приготовления 50 г 0,5 % раствора? 21. К 200 г 40 %-ного раствора серной кислоты прилили 80 мл воды. Каково процентное содержание серной кислоты во вновь полученном растворе? 22. Какая масса азотной кислоты содержится в 178 г 30%-ого раствора? 23. К 150 г 20 %-ного раствора соляной кислоты прилили 200 мл воды. Каково процентное содержание соляной кислоты во вновь полученном растворе? 24. Какой объем аммиака потребуется для приготовления 20% раствора (p=0,926г/мл), объемом 2 литра? 25. Определите массовую долю растворенного вещества в растворе, полученном при растворение 10 г соли в 70 г воды.
26. К 80 г 30 %-ного раствора щелочи долили 420 мл воды. Каково процентное содержание щелочи во вновь полученном растворе? 27. Какая масса гидроксида натрия содержится в 200 г 5%-ого раствора? 28. Вычислите массу сульфата меди (II) необходимо для приготовления 60 г раствора медного купороса с массовой долей соли 5%. 29. Какая масса карбоната натрия потребуется для приготовления 0,5 л 13%-ного раствора плотностью 1,13 г/мл? 30. Какова массовая доля (%) хлорида бария в растворе (r = 1,08 г/мл), 200 мл которого содержат 0,4 моль соли? Ответы: 1. 5%; 2. 0,2%.; 3. 1,4 г; 68,6 мл; 4. 7,4%.; 5. 1,4%.; 6. 0,6 г, 59,4 мл; 7. 0, 166%.; 8. 3,8%; 9. 1,67%; 10. 5%; 11. 1,4 г; 68,6 мл; 12. 1,5%; 13. 10%; 14. 84,8 г; 15. 45 г, 255 г; 16. 4,76%; 17. 3,65 %; 18. 21,8 г; 19. 29,7 %. 20. 0,25 г; 49,75 мл; 21. 28,6 %; 22. 53,4 г. 23. 8,6 %.; 24. 488,32 л; 25. 12,5 %; 26. 4,8 %; 27. 10 г; 28. 3 г; 29. 73,45 г; 30. 38,5 г.
|
||||||||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 203; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.150.55 (0.008 с.) |
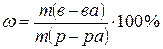
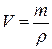 , m = V · ρ
, m = V · ρ 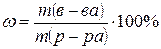
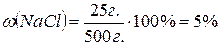
 · 100%
· 100%