Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Характеристика ацетилацетона
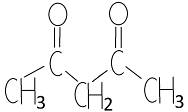
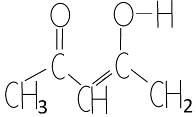
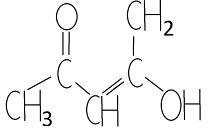
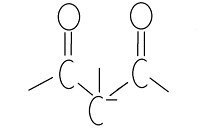
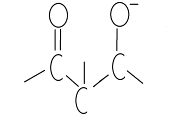
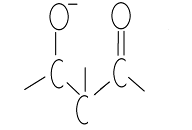
Ацетилацетон представляет собой бесцветную жидкость с приятным запахом, умеренно растворяется в воде (до 15%). Ацетилацетон, как в неразбавленном виде, так и в растворах является смесью таутомерных форм - дикарбонильная форма и енольная форма (одна или несколько), которые находятся в равновесии:
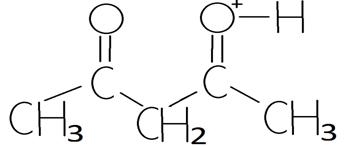
В таутомерной смеси всегда преобладает форма, имеющая меньшую кислотность. В случае ацетилацетона это дикетоформа. Химические свойства b-дикетонов в значительной степени определяются кето-енольной таутомерией. b-дикарбонильные соединения, в общем, являются высокореакционноспособными веществами. Для них характерны реакции как с нуклеофильными, так и с электрофильными реагентами. Особое место занимает кислотность, енолизация и образование солей (внутренних комплексов) этих соединений. Менее характерны реакции со свободнорадикальным механизмом. b-дикарбонильные соединения представляют собой кислоты. Константы кислотности в зависимости от строения соединения и растворителя меняются в широком интервале. Например, в водных растворах pKa»4….10. Дикарбонильная (кето-) форма является СН-кислотой, а енольная - ОН-кислотой, и каждая имеет свою константу ионизации. В кислой среде ацетилацетон, как и все b-дикетоны, протонируется с образованием катионов:
Подвижность атомов водорода при втором углеродном атоме обуславливает растворение ацетилацетона в щелочах с образованием карбанионов. Относительная легкость образования карбанионов у всех b-дикетонов объясняется стабилизацией карбанионов при помощи двух карбонильных групп вследствие резонанса:
Карбанионы b-дикетонатов являются полифункциональными лигандами. Они обладают высокой реакционной способностью и почти со всеми элементами периодической системы образуют хелаты, которые характеризуются высокой степенью делокализации p-электронной плотности в кольце, что приводит к эквивалентности связей С-О и С-С. Свойства хелатов b-дикетонатов сильно отличаются между собой [8]. Это позволило разработать методы определения, разделения и концентрирования многих элементов. С ионами металлов <http://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B> ацетилацетон дает прочные комплексные соединения <http://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BC%D0%BF%D0%BB%D0%B5%D0%BA%D1%81%D0%BD%D1%8B%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F>, которые используют в аналитической химии <http://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B0%D0%BB%D0%B8%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%85%D0%B8%D0%BC%D0%B8%D1%8F> для определения и разделения бериллия <http://ru.wikipedia.org/wiki/%D0%91%D0%B5%D1%80%D0%B8%D0%BB%D0%BB%D0%B8%D0%B9>, меди, хрома <http://ru.wikipedia.org/wiki/%D0%A5%D1%80%D0%BE%D0%BC>, железа <http://ru.wikipedia.org/wiki/%D0%96%D0%B5%D0%BB%D0%B5%D0%B7%D0%BE> и других металлов; в радиохимии <http://ru.wikipedia.org/wiki/%D0%A0%D0%B0%D0%B4%D0%B8%D0%BE%D1%85%D0%B8%D0%BC%D0%B8%D1%8F> - для выделения радиоактивных изотопов <http://ru.wikipedia.org/wiki/%D0%98%D0%B7%D0%BE%D1%82%D0%BE%D0%BF%D1%8B>.
Ацетилацетонат-анион образует комплексы со многими ионами переходных металлов <http://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B5%D1%85%D0%BE%D0%B4%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B>, где оба атома кислорода связаны с металлом, образуя шестичленные хелатные комплексы. Металл ацетилацетонаты, часто упоминаемые как хелаты металлов, хорошо известны в данной области. Металл ацетилацетонаты являются высокоэффективными катализаторами для широкого спектра органических преобразований, таких как олигомеризация, полимеризация, гидрогенизация, изомеризация, для связи и т.д. Они также используются в технологиях изготовления резины для вулканизации, для выделения и разделения металлов, в качестве реагентов ЯМР, в микроэлектронных устройствах, для синтеза высококачественных полупроводниковых материалов для оптоэлектронных устройств, для разделения энантиомеров, как источник металла или оксидов металлов для контролируемого осаждения, как фунгициды, в качестве стабилизатора цвета пигмента, как углеродные поглотители для дизельного топлива, для контроля сгорания катализаторов, для ракетных топлив и в лазерной технике.
|
|||||
|
Последнее изменение этой страницы: 2021-01-14; просмотров: 193; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.172.252 (0.005 с.) |