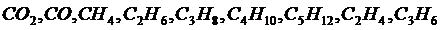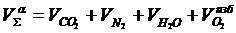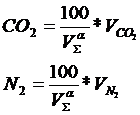Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
З. Расчет расхода окислителя и выхода продуктов полного сгорания газообразного топлива
Объем кислорода, необходимого для сгорания газообразного оксид углерода CO+0.5O2+1.88N2=CO2+1.88N2 водород H2+0.5O2+1.88N2=H2O+1.88N2 Предельные углеводороды: метан CH4+2O2+7.52N2=CO2+2H2O+7.52N2; этан С2H6+3.5O2+13.16N2=2CO2+3H2O+13.16N2; пропан С3H8+5O2+18.8N2=3CO2+4H2O+18.8N2; бутан C4H10+6.5O2+24.44N2=4CO2+5H2O+24.44N2; пентан C5H12+8O2+30.08N2=5CO2+6H2O+30.08N2. Непредельные углеводороды (с одной двойной связью): этилен C2H4+3O2+11.28N2=2CO2+2H2O+11.28N2; пропилен С3H6+4.5O2+16.92N2=3CO2+3H2O+16.92N2; сероводород H2S+1.5O2+5.64N2=SO2+H2O+5.64N2.
В соответствии с приведенными выше уравнениями горения компонентов газового топлива* объем кислорода, необходимый для сгорания 1 м3 газа, подсчитывают по формуле, м3/м3 газа
Объем воздуха топлива в стехиометрических условиях, подсчитывают, исходя из содержания в воздухе 21% кислорода по объему, м3/м3 газа:
Если в качестве окислителя используется воздух, искусственно обогащенный кислородом, то теоретический расход окислителя
где
При сжигании топлива с теоретическим количеством окислителя образуется соответственно и теоретическое количество продуктов полного сгорания
Объемы двуокиси углерода (II) и серы (II), образующиеся при сжигании топлива, не изменяются при различном расходе окислителя, а также объем образующегося водяного пара останется постоянным, если используется абсолютно сухой окислитель. Объем продуктов сгорания за вычетом объема водяных паров называется объемом сухих газов
VС.Г.=VΣ -VH2O
В практике теплотехнических расчетов объем сухих трехатомных продуктов сгорания VRO2 определяется совместно, м3/м3 газа VRO2=VCO2+VSO2 поскольку количество двуокиси серы SO2 в продуктах сгорания обычно невелико, а теплофизические свойства обоих газов близки. В этом случае теплоемкость, теплопроводность и другие характеристики сухих трехатомных продуктов сгорания принимаются как для двуокиси углерода СО2.
Выход сухих трехатомных газов, м3/м3 газа
Где, ит.д.-
содержание соответствующих углерод - и серосодержащих газов в газовом топливе. Теоретический выход азота складывается из азота воздуха и азота, Процентный состав продуктов горения определяют следующим образом, %: содержащегося в газовом топливе, м3/м3 газа:
Действительный выход азота, м^м3 газа
где α- коэффициент расхода воздуха.
Теоретический выход водяных паров определяется с учетом содержания водорода и влаги в топливе и водяных паров, содержащихся в воздухе, используемом в качестве окислителя. Содержание в воздухе водяных паров принимают около 1 мас. % (1,6 об. %), так как влагосодержание воздуха dв=10- 16 г/м3 сухого воздуха при относительной влажности φ=50-60% и температуре 20..30оС.
а с учетом содержания в 1 м3 газа d грамм влаги и содержания в воздухе 1мас. % влаги м3/м3 газа:
Для определения действительного выхода водяных паров в формулу вместо теоретического расхода воздуха действительный расход воздуха
м3/м3 газа
Общий объем продуктов сгорания при коэффициенте избытка воздуха, м3/м3
Перевод м3 в кг производят путем умножения на плотность (приложение 2). Материальный баланс процесса горения на 100 м3 газа составляется по форме табл. 1 Таблица 1
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 286; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.193.129 (0.009 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
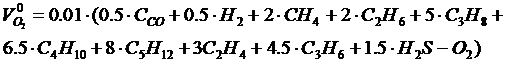
 , необходимый для сгорания 1 м3 газового
, необходимый для сгорания 1 м3 газового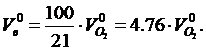
 определяется, исходя из концентрации кислорода в окислителе, м3/м3 газа:
определяется, исходя из концентрации кислорода в окислителе, м3/м3 газа: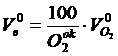
 - концентрация кислорода в окислителе, %.
- концентрация кислорода в окислителе, %.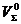 , состоящих из следующих компонентов, м3/м3 газа:
, состоящих из следующих компонентов, м3/м3 газа: