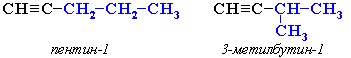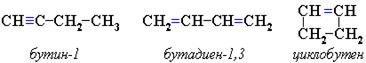Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
IV . Объяснение нового материалаСодержание книги Поиск на нашем сайте
Вопрос 1.Гомологи и изомеры алкенов и алкинов. Алкены – органические соединения, углеводороды алифатического (ациклического) непредельного характера, в молекуле которых между атомами углерода – одна двойная связь, и которые соответствуют общей формуле CnH 2 n. Для алкенов характерна sp2-гибридизация. Длина двойной связи 0,134нм, она более прочная, чем одинарная, так как ее энергия больше. Одновременно, наличие подвижной, легко поляризуемой π-связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения. В названии алкенов содержится суффикс –ен или –илен, обозначающий принадлежность соединения к данному классу. Простейший алкен: C2H4 или H – C = C – H этен или этилен, | | H H Его радикал: C2H3- или CH2=CH- винил. В определении названия алкена положение кратной связи имеет при нумерации преимущество перед остальными.
CH3 Cl CH3 7 6| 5| 4| 3 2 1 CH3 – CH – CH – C – CH = CH – CH3 | C2H5 4,6-диметил-4-этил-5-хлоргептен-2
Для алкенов характерны следующие виды изомерии: 1. Структурная изомерия: а) изомерия углеродного скелета 1 2 3 4 5 1 2 3 4 CH2=CH – CH2 – CH2 – CH3 CH2=CH – CH – CH3 | CH3 пентен-1 3-метилбутилен-1 б) изомерия положения кратной связи 1 2 3 4 5 1 2 3 4 5 CH2=CH – CH2 – CH2 – CH3 CH3–CH = CH – CH2 – CH3 пентен-1 пентен-2 в) изомерия положения заместителей (Hal, - NO2, SO2-OH и др.) 1 2 3 4 5 1 2 3 4 5 CH2=CH – CH – CH2 – CH3 CH2=CH – CH2 – CH – CH3
| | Cl Cl 3-хлорпентен-1 4-хлорпентен-1 2. Пространственная изомерия: а) геометрическая изомерия 1 2 3 4 CH3 – CH = CH – CH3 бутилен-2
CH3 CH3 CH3 H \ / \ / C=C C=C / \ / \ H H H CH3 цис-изомер транс-изомер 3. Межклассовая изомерия (с циклоалканами) 1 2 3 4 5 CH2=CH – CH2 – CH2 – CH3 CH2 – CH2 пентен-1 ! ! CH2 CH2 \ / CH2 циклопентан
Строение алкинов Орбитали атомов углерода, между которыми образована тройная связь (рис. 21), находятся в состоянии sp -гибридизации. Это означает, что в гибридизации участвует одна s- и одна р -орбиталь, а две р -орбитали остаются негибридизованными. Перекрывание гибридных орбиталей приводит к образованию σ -связи, а за счёт негибридизованных р -орбиталей соседних атомов
Тройная углерод-углеродная связь, длина которой 0,12 нм, короче двойной. Энергия тройной связи больше, т. е. она является более прочной. Гомологический ряд алкинов Неразветвлённые алкины составляют гомологический ряд этина (ацетилена): С2Н2 — этин, С3Н4 — пропин, С4Н6 — бутин, С5Н8 — пентин, С6Н10 — гексин и т. д. Номенклатура алкинов Наличие тройной связи в молекулах углеводородов этого класса отражается суффиксом - ин, а её положение в цепи — номером атома углерода. Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6):
2. Изомерия углеродного скелета (начиная с С5Н8):
3. Межклассовая изомерия с алкадиенами начиная с С4Н6:
|
||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 130; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.29.149 (0.009 с.) |

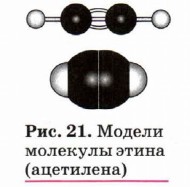 углерода образуются две π -связи. Таким образом, тройная связь состоит из одной σ - и двух тс-связей. Все гибридные орбитали атомов, между которыми образована тройная связь, а также заместители при них (в случае этина — атомы водорода) лежат на одной прямой, а плоскости π -связей перпендикулярны друг другу (см. рис. 6, б).
углерода образуются две π -связи. Таким образом, тройная связь состоит из одной σ - и двух тс-связей. Все гибридные орбитали атомов, между которыми образована тройная связь, а также заместители при них (в случае этина — атомы водорода) лежат на одной прямой, а плоскости π -связей перпендикулярны друг другу (см. рис. 6, б).