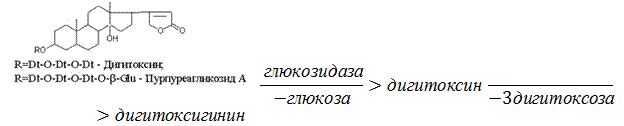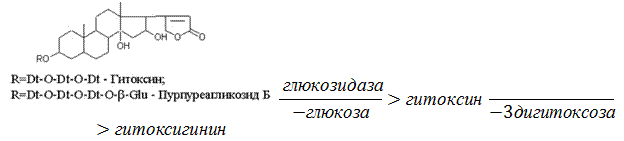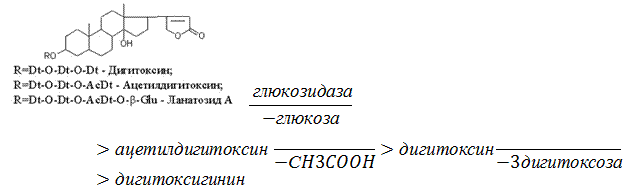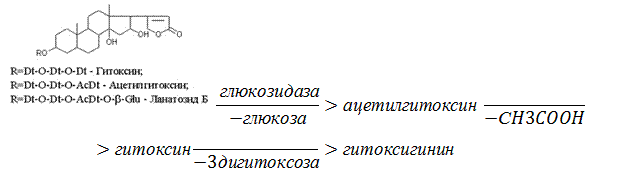Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физические и химические свойства СГ. ⇐ ПредыдущаяСтр 2 из 2
1. Сердечные гликозиды представляют собой кристаллические, реже аморфные вещества, бесцветные или беловатые, иногда с кремовым оттенком. 2. Без запаха, горького вкуса. Из-за ядовитости их вкус не определяют. 3. Имеют определенную температуру плавления. 4. Оптически активны, имеют определеннвый угол вращения 5. Способны флуоресцировать в УФ желтым, голубым и зеленым цветом. 6. СГ Хорошо растворимы в водных растворах метилового и этилового спиртов, в чистых спиртах при нагревании. Мало растворимы в воде и хлороформе. На растворимость в воде влияет длина сахарной цепочки. Чем она длинее, тем лучше растворяются сердечные гликозиды. Не растворимы в органических растворителях (диэтиловом и петролейном эфирах, в ССl4 и др.).
В зависимости от растворимости в воде и липидах СГ делятся на 2 группы: - Гидрофильные (полярные) СГ. Полярность обусловлена наличием альдегидной группы в С10 агликона, а также присутствием дополнительных -ОН групп в агликоне. -Липофильные (неполярные) СГ. Неполярность обусловлена метильными группами в С10 агликона. Подгруппа наперстянки. Наличие ОН групп и ацетилированных моносахаров позволяет увеличивать гидрофильные свойства.
Химические свойства. Все реакции на сердечные гликозиды можно разделить на 3 группы: 1. Реакции на углеводную часть молекулы. 2. Реакции на стероидное ядро. 3. Реакции на лактонное ненасыщенное кольцо. -Самые неустойчивое лактомное кольцо и гликозидная связь. -Лактамное кольцо изомеризуется под действием щелочей. -Гликозидная связь подвергается ферментативному гидролизу в присутствии воды – ступенчатый гидролиз СГ.
Начнем с сердечных гликозидов наперстянки пурпурной (Digitalis purpurea).
Гидролиз пурпуреагликозида А
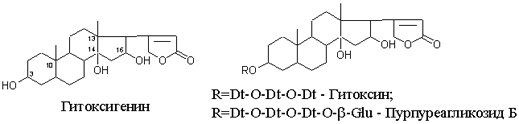
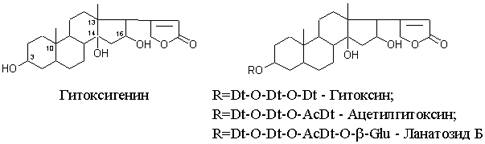
Пурпуреагликозид Б Теперь, если к молекуле дигитоксигенина присоединим еще одну –ОН группу (в положении при С16), получим гитоксигенин. Аналогично гликозидам дигитоксигенина строим гликозиды гитоксигенина – гитоксин и пурпуреагликозид Б.
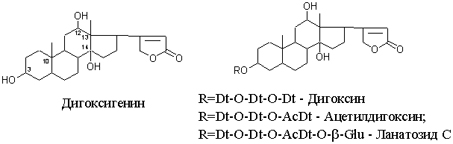
Гидролиз ланатозидов Карденолиды наперстянки шерстистой тоже строим на основе дигитоксигенина, гитоксигенина и дигоксигенина. Но при получении типичных гликозидов наперстянки шерстистой вместо трех молекул дигитоксозы добавляем к соответствующему агликону две молекулы дигитоксозы и одну – ацетилдигитоксозы.
Ланатозид А
Ланатозид Б
Ланатозид С
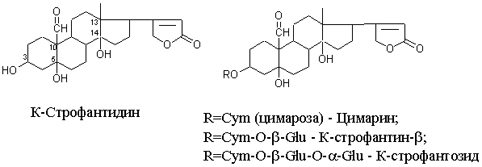
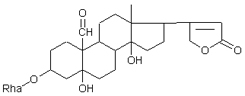
К-строфантазиды Сердечные гликозиды строфанта комбе (Strophanthus kombe) строятся на основе агликона, который называется К–строфантидин (К, то есть комбе). Он отличается от дигитоксигенина тем, что в его молекуле вместо –СН3 группы в положении С10 находится альдегидная группа –СОН и появляется еще одна –ОН группа – в положении С5 (на противоположном конце от альдегидной).
На основе К–строфантидина строим его гликозиды – цимарин (присоединяем в С3 положении вместо водорода одну молекулу цимарозы); К–строфантин–бета (к цимарозе добавляем одну молекулу бета–глюкозы) и К–строфантозид (к цимарозе и бета–глюкозе добавляем еще одну молекулу альфа–глюкозы). А если к молекуле К–строфантидина вместо цимарозы мы присоединим молекулу рамнозы, получим карденолид ландыша майского (Convallaria majalis) – конваллотоксин.
Конваллотоксин (Агликон – К–строфантидин (–ОН в С14, С5))
Эризимин (Агликон – К–строфантидин (–ОН в С14, С5))
Адонитоксин (Агликон – адонитоксигенин (–ОН в С14, С16))
Корельборин (Агликон – геллебригенин (–ОН в С14, С5), как К–строфантидин)
Химические свойства. Возможен кислотный и щелочной гидролиз (происходит расщепление до агликона и сахаров), некоторые при кипячении в воде.
Оценка качества сырья. Методы анализа Качественное определение Качественные реакции проводят или с индивидуальными веществами, или с очищенным извлечением из ЛРС. Все реакции на сердечные гликозиды можно разделить на 3 группы: 1. Реакции на углеводную часть молекулы. 2. Реакции на стероидное ядро. 3. Реакции на лактонное ненасыщенное кольцо. 1. Реакции на сахарный компонент. В начале проводится кислотный гидролиз. Свободный сахар определяется Феллинговой жидкостью (идет образование красной закиси меди) или реакцией образования "серебряного зеркала". На дезоксисахара проводят: Реакцию Келлер-Килиани - к извлечению (сухому остатку) прибавляют: концентрированную СН3СООН со следами трехвалентного железа, осторожно наслаивают концентрированную Н2SO4 со следами трехвалентного железа. На границе двух слоев образуется коричневое или бурое кольцо, верхний слой окрашивается в сине-зеленый цвет. Реакция положительная в том случае, если дезоксисахар находится в свободном состоянии или занимает крайнее положение в молекуле гликозида. Если дезоксисахар связан с одной стороны с агликоном, а с другой - с другим сахаром (например, глюкозой), то реакция Келлер-Килиани не дает положительных результатов. Для обнаружения дезоксисахаров в таких случаях проводят гидролиз трихлоруксусной кислотой. Свободный дезоксисахар с нитрофенилгидразином и щелочью дает голубую окраску. Известна на дезоксисахара и ксантгидрольная реакция. К извлечению прибавляют ксантгидрол и ледяную уксусную кислоту, при нагревании и добавлении небольшого колическтва серной (или фосфорной) кислоты образуется красное окрашивание.
Реакции на стероидное ядро. Реакция Либермана-Бурхарда: сухой остаток растворяют в ледяной уксусной кислоте, прибавляют смесь уксусного ангидрида с концентрированной серной кислотой (50:1) - развивается окраска от красной до розовой, переходящей в зеленую или сине-зеленую. Реакция Розенгейма: сухой остаток растворяют в хлороформе, прибавляют 90%-ный водный раствор трихлоруксусной кислоты. Возникает розовая окраска, переходящая в лиловую. Реакция с SbCl 3: в среде уксусного ангидрида – лиловое окрашивание. 3. Реакции на пятичленное лактонное кольцо. Все реакции проводятся со спиртовым очищенным извлечением из ЛРС в щелочной среде: реакция Легаля: с нитропруссидом натрия появляется быстро исчезающее красное окрашивание; реакция Раймонда: с м-динитробензолом - красно-фиолетовое окрашивание; реакция Кедде: с 3,5-динитробензойной кислотой - фиолетовое окрашивание; реакция Балье: с пикриновой кислотой - оранжевое окрашивание. 4. Реакции на шестичленный лактонный цикл: к спиртовому извлечению прибавляют насыщенный раствор треххлористой сурьмы в хлороформе - при нагревании возникает лиловая окраска; 20% раствор треххлористой сурьмы в хлороформе используется для обнаружения буфадиенолидов на хроматограммах. Кроме того сердечные гликозиды образуют нерастворимые комплексы с растворами ДВ, что используется при отравлениях сердечными гликозидами.
|
|||||||
|
Последнее изменение этой страницы: 2020-12-17; просмотров: 211; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.79.60 (0.021 с.) |