
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Экономика и управление на предприятии,Содержание книги Поиск на нашем сайте
Экономика и управление на предприятии, Промышленное и гражданское строительство», 210104 «Микроэлектроника и твердотельная электроника».
Автор – Шаврак Е.И.
Волгодонск 2007 г.
Тесты первого промежуточного контроля знаний по общей химии Контролируемые темы:
А. Основные понятия и законы химии. Закон эквивалентов.
a) ν Na2S =1 моль б) νNa2S=0,5моль в)νNa2S=νэкв. г)νNa2S=39 ν экв=0,5 νэкв=1 моль νэкв=0,5 моль νэкв=19,5
а) 52,6 г б) 31,6 в) 158 г г) 48,6
а) 21 г б) 63 г в) 0,031 г г) 3,1 г
а) 21 г б) 32,6 в) 31 г г) 27 г
Б. Состав и строение атома.
a) Zn2+ б) Са2+ в) As3+ г) Se
а) 1S22S22P4 б) 1S22S22P6 в) 1S22S22P3 г) 1S22S22P5
а) As5+ б) Са2+ в) Fe2+ г) Br-
а) 3 d54S1 б) 3 d 64S0 в) 3d44S2 г) 3 d 7
а) 2s22p6 б) 2s02p0 в) 2s22p3 г)2s22p5
а) 2s22p2 б) 2s22p4 в) 2s12p3 г) 2s22p4
а) 2s б) 2p6 в) 3d г) 4P
Г. Химическая связь
а) LiF б) LiCI в) LiBr г) LiI
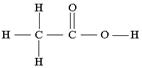
а)H3PO4, BF3, CH3COONH4 б) H2SO4, F2, P2O5 в) PF5, Cl2O7, NH4Cl г)NO2, SOCl2, CH3COOH 4.В каком веществе нет химических связей между атомами серы? 5.Определите, каким кислотам принадлежат приведённые ниже графические формулы: 1. 6.Определите, графическая формула какой соли приведена ниже, напишите ее химическую формулу:
Какие элементы, химические знаки которых приведены ниже, способны к образованию межмолекулярных водородных связей:а) Sе,б) C,в) O,г) Te,
ВСЕГО 50 тестов
А. Химическая термодинамика 20. ΔНореакции: CaO(к) + CO2(г) = CaCO3(к) составляет, кДж 21. При сгорании 1 г магния выделилось 25 кДж теплоты. На основании этих данных молярная теплота образования оксида магния (кДж/моль) равна: а) 600 б) 1000 в) 1200 г) 2000 22. Стандартная энтальпия образования SO2 равна -297 кДж/моль. Чему равно количество тепла, выделившееся при сгорании 16 г серы: а) 74,25 кДж б) 148,5 кДж в) 297 кДж г) 594 кДж 23. Поприведенным стандартным значениям изменения энтальпии и энтропии для химической реакции а) 0,98К б)9,8К в) 98К г) 980К 24. В изолированной системе реакция может протекать самопроизвольно, если: а) изменение энтропии системы положительно б) изменение энтропии системы отрицательно в) изменение энтальпии системы положительно г) изменение энергии Гиббса системы отрицательно 25. В открытой системе реакция может протекать самопроизвольно, если: а) изменение энтропии системы положительно б) изменение энтропии системы отрицательно в) изменение энтальпии системы положительно г) изменение энергии Гиббса системы отрицательно ВСЕГО 70 тестов
Экономика и управление на предприятии,
|
||||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 146; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.137.244 (0.006 с.) |

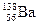
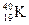

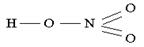 2.
2. 

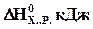 =+ 173,
=+ 173, 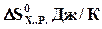 = +176 рассчитайте температуру, при которой равновероятны прямое и обратное направления данной реакции:
= +176 рассчитайте температуру, при которой равновероятны прямое и обратное направления данной реакции:


