
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Проведение импульса по системе Гиса-Пуркинье.Содержание книги Поиск на нашем сайте
Проводящая система желудочков представлена общим пучком Гиса, ножками пучка Гиса с их разветвлениями и волокнами Пуркинье. Ветвление ножек пучка Гиса очень вариабельно (рис. 14). Из рисунка видно, что разделение левой ножки на переднюю и заднюю ветви является большим упрощением. Электрофизиологически проводящая система желудочков проявляет быстрый электрический ответ, причем скорость проведения в ней наибольшая в миокарде, что обусловлено несколькими причинами. Во-первых, за счет относительно гиперполяризованного максимального диастолического потенциала и реактивации вследствие этого быстрых натриевых каналов, что, в свою очередь, приводит к увеличению амплитуды потенциала действия и скорости деполяризации ( В отличие от типичных клеток с быстрым электрическим ответом, клетки системы Гиса-Пуркинье демонстрируют незначительную медленную диастолическую деполяризацию, обусловленную пейсмейкерным током (I f). Эта особенность ответственна за пейсмейкерную активность проводящей системы, которая, хотя и не проявляется в нормальном миокарде, но в случае подавления суправентрикулярных пейсмейкеров или атриовентрикулярной блокады обуславливает редкий желудочковый ритм (до 40 ударов в минуту). Кроме того, в некоторых случаях, например, при адренергической стимуляции, пейсмейкерная активность проводящей системы желудочков может усиливаться (аномальный автоматизм), что приводит к формированию желудочковых тахиаритмий. Потенциалы действия и, как следствие, рефрактерные периоды волокон Пуркинье имеют самую большую в миокарде длительность. Считается, что эта особенность защищает проводящую систему от возврата волны возбуждения из рабочего миокарда и связанной с этим дезорганизацией возбуждения желудочков. Деполяризация желудочков Последовательность и скорость распространения волны деполяризации в миокарде желудочков определяется, в основном, расположением терминалей проводящей системы, архитектоникой волокон рабочего миокарда и особенностями потенциалов действия кардиомиоцитов. В зависимости от степени развития системы Гиса-Пуркинье у позвоночных животных выделяется несколько типов активации миокарда (рис. 16,17). У земноводных и пресмыкающихся, развитие проводящей системы у которых крайне слабое, если таковая вообще присутствует, волна деполяризации движется последовательно от основания к верхушке и от эндокарда к эпикарду (последовательный тип активации миокарда). У копытных животных и птиц вероятно с целью быстрого охвата возбуждением большого объема миокарда проводящая система развита исключительно высоко – волокна Пуркинье прорастают не только в субэндокард, но и в интрамуральные и даже субэпикардиальные слои. Вследствие этого в толще стенок желудочков формируются множественные первичные очаги возбуждения, от которых волна возбуждения распространяется и к эпикарду, и к эндокарду. Такой способ активации миокарда получил название вспышечного. У хищных животных, а также у человека тип активации промежуточный: за счет системы Гиса-Пуркинье происходит очень быстрое возбуждение субэндокардиальных слоев, после чего волна деполяризации движется последовательно от эндокарда к эпикарду. В общих чертах, для человека характерна следующая последовательность активации желудочков сердца: левый субэндокард межжелудочковой перегородки, субэндокард свободной стенки левого желудочка, свободные стенки правого и левого желудочка, основания обоих желудочков и межжелудочковой перегородки.
Вторым важным фактором, определяющим ход деполяризации миокарда, является направление волокон рабочего миокарда. Вдоль волокна возбуждение распространяется примерно в три раза быстрее, чем поперек (анизотропия миокарда). Главную роль в анизотропном распространении деполяризации играет распределение щелевых контактов (gap junctions), которые содержат ионные каналы, образованные белковыми комплексами – коннексонами. Плотность щелевых контактов на полюсах кардиомиоцитов больше, чем на их боковых поверхностях. Типичным примером формирования анизотропии является развитие гипертрофии, в том числе, физиологической гипертрофии левого желудочка после рождения. В этих условиях происходит перераспределение щелевых контактов: они смещаются с боковых поверхностей на полюса. Кроме этого между волокнами развивается соединительная ткань. За счет своего высокого электрического сопротивления соединительная ткань усиливает анизотропию, а также способствует электрическому разобщению (uncoupling) кардиомиоцитов.
Сопротивление ионных каналов щелевых контактов непостоянно, - оно увеличивается при повышении внутриклеточной концентрации кальция и катионов водорода и при снижении внутриклеточной концентрации цАМФ, что создает предпосылки для изменения межклеточного взаимодействия при нарушениях кальциевого гомеостаза, ишемии, сердечной недостаточности, а также для нейрогуморальной регуляции этого взаимодействия. Изменение межклеточного взаимодействия в миокарде важно с теоретической и практической точки зрения. Во-первых, это явление уточняет понятие функционального синцития, согласно которому в ответ на пороговый стимул миокард реагирует как единое целое. В связи с изменением электрического межклеточного взаимодействия, степень этой «целостности» может быть неодинаковой в разных условиях. Во-вторых, электрическое разобщение кардиомиоцитов, является одним из мощных факторов, поддерживающих фибрилляцию желудочков, поэтому щелевые контакты можно использовать как мишени для антиаритмических препаратов. Еще одним фактором, влияющим на скорость проведения волны деполяризации в миокарде является совокупность особенностей потенциалов действия кардиомиоцитов (рис.18). Наиболее важными из этих электрофизиологических характеристик являются амплитуда потенциала действия и максимальная скорость нарастания потенциала в фазу деполяризации ( Перечисленные выше факторы, влияющие на скорость распространения волны деполяризации, в целом справедливы не только для желудочков, но и для других областей миокарда. Реполяризация желудочков Реполяризация миокарда изучена намного меньше, чем деполяризация, в частности, последовательность реполяризации желудочков, которая определяет формирование зубца Т электрокардиограммы, на сегодняшний день не установлена. Чаще всего рассматривается трансмуральная последовательность реполяризации. Считается, что раньше всего реполяризуются субэпикардиальные участки, затем субэндокардиальные, а в последнюю очередь – кардиомиоциты в интрамуральных слоях, так называемые М-клетки. В то же время практически неизвестно каким образом соотносится реполяризация на верхушке и в основании, в правом и левом желудочке, на передней и задней поверхности.
Можно выделить два основных фактора, которые влияют на последовательность реполяризации желудочков сердца. Во-первых, это длительности потенциалов действия в разных участках миокарда, а, во-вторых, последовательность активации желудочков. В целом, при нормальном проведении импульса, главным фактором является распределение длительностей потенциалов действия, а при замедлении активации желудочков, например, при блокадах ножек пучка Гиса или при эктопическом возбуждении желудочков, определяющей становится последовательность деполяризации (рис. 19). На этом основании выделяются, соответственно, первичные и вторичные изменения реполяризации. Важно, что при вторичных нарушениях последовательность реполяризации повторяет последовательность деполяризации, но потенциал каждой клетки меняется в противоположном направлении: деполяризованные клетки снаружи заряжены отрицательно, а реполяризованные – положительно, - совокупность этих двух особенностей (повторение последовательностей и противоположность изменения зарядов) приводят к тому, что при вторичных нарушениях реполяризации формируются дискордантные, то есть, разнонаправленные комплексы QRS и Т. В последнее время сформулировано понятие «памяти сердца». Память сердца - изменения волны ST-T при желудочковых аритмиях, которые остаются длительное время после восстановления нормальной последовательности возбуждения миокарда. Суть изменений, происходящих при таком «запоминании», заключается в том, что измененная последовательность активации приводит к изменению длительностей потенциалов действия, то есть, происходит комбинирование первичных и вторичных изменений реполяризации (рис. 20).
Аритмогенез
Механизмы аритмий делятся на механизмы, основанные на нарушениях образования импульса, нарушениях проведения импульса и комбинированных нарушениях. Нарушения образования импульса 1. Изменения нормального автоматизма за счет нейрогуморальной регуляции (синусовая тахи- и брадикардия). 2. Аномальный автоматизм. Существенное повышение нормального автоматизма. Пример такого изменение – формирование желудочковых тахикардий за счет усиления пейсмейкерной активности волокон Пуркинье под влиянием адреналина. Второй механизм аномального автоматизма – превращение клеток с быстрым ответом в клетки с медленным ответом в ишемизированном миокарде за счет деполяризации потенциала покоя и инактивации натриевых каналов.
3. Триггерная активность. В основе триггерной активности лежат ранние и поздние постдеполяризации (рис. 21), которые возникают после нормального потенциала действия, который рассматривается в этом случае как пусковой фактор, или триггер. Постдеполяризации могут под- и надпороговыми, надпороговые вызывают формирование новых потенциалов действия. Механизм постдеполяризаций до конца не ясен. По наиболее распространенной точке зрения, они возникают при кальциевых перегрузках. В этих условиях один внутриклеточный ион кальция начинает обмениваться на три внеклеточных иона натрия через натрий-кальциевый обменник, что обуславливает входящий (деполяризующий) ток. 4. Деполяризация за счет электротонического взаимодействия, которое проявляется при наличии в миокарде электрических неоднородностей, связанных либо с локальной деполяризацией потенциала покоя, либо с большими различиями во времени реполяризации (рис. 22). Оба случая характерны для ишемизированных областей миокарда.
|
||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 99; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.223.30 (0.011 с.) |

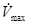 ). Во-вторых, в клетках проводящей системы внутреннее сопротивление ниже, чем в рабочем миокарде. В-третьих, волокна системы Гиса-Пуркинье полностью или частично изолированы от окружающих тканей, что ограничивает утечку токов в соседние области. Все причины способствуют более эффективной передачи возбуждения между проводящими кардиомиоцитами.
). Во-вторых, в клетках проводящей системы внутреннее сопротивление ниже, чем в рабочем миокарде. В-третьих, волокна системы Гиса-Пуркинье полностью или частично изолированы от окружающих тканей, что ограничивает утечку токов в соседние области. Все причины способствуют более эффективной передачи возбуждения между проводящими кардиомиоцитами.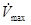 ). Эти параметры определяют «силу влияния» возбужденного кардиомиоцита на соседние клетки: чем больше амплитуда и
). Эти параметры определяют «силу влияния» возбужденного кардиомиоцита на соседние клетки: чем больше амплитуда и 


