
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ионные каналы кардиомиоцитовСодержание книги Поиск на нашем сайте
Ионные каналы кардиомиоцитов
Электрофизиологические особенности клеток миокарда
В соответствии с распределением ионных каналов в разных областях миокарда формы потенциалов действия кардиомиоцитов из этих участков отличаются друг от друга. Для описания различий между потенциалами действия в данном разделе мы используем следующие параметры: уровень потенциала покоя (ПП), или максимального диастолического потенциала (МДП); наличие или отсутствие фазы медленной диастолической деполяризации (МДД); крутизна нарастания потенциала в фазу МДД; Максимальная скорость нарастания потенциала в фазу 0 Ниже приведены основные особенности кардиомиоцитов из разных областей миокарда.
Клетки с медленным ответом (рис. 1, 3) 1. Деполяризованный МДП; 2. Фаза МДД – токи I f, I Ca-T; 3. В клетках СА-узла МДД круче, чем в клетках АВ-узла; 4. Максимальная скорость нарастания потенциала в фазу 0
Клетки с быстрым ответом Общие особенности (рис. 2, 4): 1. Относительно гиперполяризованный и стабильный МДП; 2. Отсутствие или малая выраженность МДД; 3. Высокая 4. Выраженная фаза плато ПД; 5. Большая длительность ПД и рефрактерного периода. Клетки рабочего миокарда предсердий (рис. 2, 4): 1. 2. Мало выражена фаза плато ПД из-за мощного I to и присутствия I Kur. Клетки рабочего миокарда желудочков (рис.2, 5). Приведены наиболее распространенные в литературе точки зрения. Кроме перечисленных трансмуральных различий клеток, имеются особенности в зависимости от положения клеток в правом или левом желудочке, на верхушке или в основании, на передней или задней поверхности и т.п. Клетки субэпикарда желудочков: 1. Выраженная фаза 1 – форма ПД "пик и купол" – большая величина транзиторного выходящего калиевого тока (I to); 2. Малая длительность ПД – большая плотность калиевых токов задержанного выпрямления (I K). Клетки субэндокарда желудочков:
1. Невыраженная фаза 1 – малая величина транзиторного выходящего калиевого тока (I to); 2. Большая, по сравнению с субэпикардом, длительность ПД – меньшая плотность калиевых токов задержанного выпрямления (I K). М-клетки интрамуральных слоев желудочков: 1. 2. Выраженная фаза 1 – форма ПД "пик и купол" – большая величина транзиторного выходящего калиевого тока (I to); 3. Большая длительность ПД – меньшая, по сравнению с субэпи- и субэндокардом, плотность калиевых токов задержанного выпрямления, особенно I Ks. 4. При уменьшении ЧСС – большее, по сравнению с субэпи- и субэндокардом, увеличение длительности ПД – малая плотность I Ks. Клетки проводящей системы Гиса-Пуркинье (рис. 2, 6): 1. Гиперполяризованный МДП; 2. Небольшая МДД– ток I f; 3. 4. Наибольшая длительность ПД в миокарде – сниженная плотность реполяризующих токов.
Генерация импульса В миокарде импульс генерируется в пейсмейкерной системе, основу которой составляют клетки с медленным электрическим ответом (рис.1). Важнейшей особенностью этих клеток является фаза медленной диастолической деполяризации, обусловленная пейсмейкерным током (I f) и током через кальциевые каналы Т-типа (I Ca-T). Начало данной фазы связано с активацией пейсмейкерного тока за счет реполяризации (гиперполяризации). При этом одновременно увеличивается калиевая и натриевая проводимости. Поскольку в гиперполяризованной клетке электродвижущие силы для движения ионов натрия больше, чем для ионов калия, результирующий ток является входящим, который приводит к постепенной деполяризации, которая далее активирует кальциевые каналы Т-типа. Ток через эти каналы поддерживает конечную часть медленной диастолической деполяризации и активирует кальциевые каналы L-типа, пороговый потенциал которых выше, чем для каналов Т-типа. I Ca-L ток ответственен за формирование фазы быстрой деполяризации потенциала действия. В клетках с медленным ответом скорость быстрой деполяризации существенно ниже, чем в клетках с быстрым ответом (отсюда названия). Причина этих различий заключается в том, что быстрая деполяризация в клетках с быстрым ответом формируется за счет натриевого тока, а в клетках с медленным ответом – кальциевым, поскольку имеющиеся там натриевые каналы инактивированы за счет деполяризации диастолического потенциала.
В нормальном сердце водителем ритма является пейсмейкерный комплекс, связанный с СА-узлом, поскольку в нем скорость медленной диастолической деполяризации наибольшая. На эпикарде предсердий можно обнаружить несколько точек первичной активности. Локализация этих точек зависит от частоты ритма сердца, что, в свою очередь, определяется регуляторными влияниями со стороны автономной нервной системы (рис. 10). Важно, что область, где может быть зарегистрирована первичная активность почти в два раза больше СА-узла. На этом основании была сформулирована концепция предсердного пейсмейкерного комплекса (мультицентровой генерации импульса), в который помимо СА-узла входят кардиомиоциты окружающего предсердного миокарда, клетки в основании створок клапанов. Исходя из мультицентрового происхождения импульса объясняются такие явления, как выскальзывающие комплексы и синусовая аритмия (рис. 11). Согласно этой концепции, изменение длины цикла сердца связано с тем, что изменяется иерархия между одновременно существующими очагами возбуждения в пейсмейкерном комплексе. Деполяризация предсердий В силу функционирования предсердного пейсмейкерного комплекса последовательность активации предсердий вариабельна (рис.10,11). Она зависит от местоположения очага возбуждения, который в данный момент доминирует. Особенно это касается правого предсердия, поскольку СА-узел расположен в его ткани. Другим фактором, который обуславливает вариабельность последовательности активации предсердий является относительно слабое развитие трактов проводящей системы предсердий несоизмеримое с системой Гиса-Пуркинье желудочков. В миокарде предсердий описаны следующие тракты предпочтительного проведения: передний тракт с левопредсердной ветвью, которая иногда называется пучком Бахманна, средний тракт (Венкебаха) и задний (Торела). Все эти тракты, кроме пучка Бахманна направляются от СА- к АВ-узлу (рис.12). Деполяризация желудочков Последовательность и скорость распространения волны деполяризации в миокарде желудочков определяется, в основном, расположением терминалей проводящей системы, архитектоникой волокон рабочего миокарда и особенностями потенциалов действия кардиомиоцитов. В зависимости от степени развития системы Гиса-Пуркинье у позвоночных животных выделяется несколько типов активации миокарда (рис. 16,17). У земноводных и пресмыкающихся, развитие проводящей системы у которых крайне слабое, если таковая вообще присутствует, волна деполяризации движется последовательно от основания к верхушке и от эндокарда к эпикарду (последовательный тип активации миокарда). У копытных животных и птиц вероятно с целью быстрого охвата возбуждением большого объема миокарда проводящая система развита исключительно высоко – волокна Пуркинье прорастают не только в субэндокард, но и в интрамуральные и даже субэпикардиальные слои. Вследствие этого в толще стенок желудочков формируются множественные первичные очаги возбуждения, от которых волна возбуждения распространяется и к эпикарду, и к эндокарду. Такой способ активации миокарда получил название вспышечного. У хищных животных, а также у человека тип активации промежуточный: за счет системы Гиса-Пуркинье происходит очень быстрое возбуждение субэндокардиальных слоев, после чего волна деполяризации движется последовательно от эндокарда к эпикарду. В общих чертах, для человека характерна следующая последовательность активации желудочков сердца: левый субэндокард межжелудочковой перегородки, субэндокард свободной стенки левого желудочка, свободные стенки правого и левого желудочка, основания обоих желудочков и межжелудочковой перегородки.
Вторым важным фактором, определяющим ход деполяризации миокарда, является направление волокон рабочего миокарда. Вдоль волокна возбуждение распространяется примерно в три раза быстрее, чем поперек (анизотропия миокарда). Главную роль в анизотропном распространении деполяризации играет распределение щелевых контактов (gap junctions), которые содержат ионные каналы, образованные белковыми комплексами – коннексонами. Плотность щелевых контактов на полюсах кардиомиоцитов больше, чем на их боковых поверхностях. Типичным примером формирования анизотропии является развитие гипертрофии, в том числе, физиологической гипертрофии левого желудочка после рождения. В этих условиях происходит перераспределение щелевых контактов: они смещаются с боковых поверхностей на полюса. Кроме этого между волокнами развивается соединительная ткань. За счет своего высокого электрического сопротивления соединительная ткань усиливает анизотропию, а также способствует электрическому разобщению (uncoupling) кардиомиоцитов. Сопротивление ионных каналов щелевых контактов непостоянно, - оно увеличивается при повышении внутриклеточной концентрации кальция и катионов водорода и при снижении внутриклеточной концентрации цАМФ, что создает предпосылки для изменения межклеточного взаимодействия при нарушениях кальциевого гомеостаза, ишемии, сердечной недостаточности, а также для нейрогуморальной регуляции этого взаимодействия. Изменение межклеточного взаимодействия в миокарде важно с теоретической и практической точки зрения. Во-первых, это явление уточняет понятие функционального синцития, согласно которому в ответ на пороговый стимул миокард реагирует как единое целое. В связи с изменением электрического межклеточного взаимодействия, степень этой «целостности» может быть неодинаковой в разных условиях. Во-вторых, электрическое разобщение кардиомиоцитов, является одним из мощных факторов, поддерживающих фибрилляцию желудочков, поэтому щелевые контакты можно использовать как мишени для антиаритмических препаратов.
Еще одним фактором, влияющим на скорость проведения волны деполяризации в миокарде является совокупность особенностей потенциалов действия кардиомиоцитов (рис.18). Наиболее важными из этих электрофизиологических характеристик являются амплитуда потенциала действия и максимальная скорость нарастания потенциала в фазу деполяризации ( Перечисленные выше факторы, влияющие на скорость распространения волны деполяризации, в целом справедливы не только для желудочков, но и для других областей миокарда. Реполяризация желудочков Реполяризация миокарда изучена намного меньше, чем деполяризация, в частности, последовательность реполяризации желудочков, которая определяет формирование зубца Т электрокардиограммы, на сегодняшний день не установлена. Чаще всего рассматривается трансмуральная последовательность реполяризации. Считается, что раньше всего реполяризуются субэпикардиальные участки, затем субэндокардиальные, а в последнюю очередь – кардиомиоциты в интрамуральных слоях, так называемые М-клетки. В то же время практически неизвестно каким образом соотносится реполяризация на верхушке и в основании, в правом и левом желудочке, на передней и задней поверхности. Можно выделить два основных фактора, которые влияют на последовательность реполяризации желудочков сердца. Во-первых, это длительности потенциалов действия в разных участках миокарда, а, во-вторых, последовательность активации желудочков. В целом, при нормальном проведении импульса, главным фактором является распределение длительностей потенциалов действия, а при замедлении активации желудочков, например, при блокадах ножек пучка Гиса или при эктопическом возбуждении желудочков, определяющей становится последовательность деполяризации (рис. 19). На этом основании выделяются, соответственно, первичные и вторичные изменения реполяризации. Важно, что при вторичных нарушениях последовательность реполяризации повторяет последовательность деполяризации, но потенциал каждой клетки меняется в противоположном направлении: деполяризованные клетки снаружи заряжены отрицательно, а реполяризованные – положительно, - совокупность этих двух особенностей (повторение последовательностей и противоположность изменения зарядов) приводят к тому, что при вторичных нарушениях реполяризации формируются дискордантные, то есть, разнонаправленные комплексы QRS и Т.
В последнее время сформулировано понятие «памяти сердца». Память сердца - изменения волны ST-T при желудочковых аритмиях, которые остаются длительное время после восстановления нормальной последовательности возбуждения миокарда. Суть изменений, происходящих при таком «запоминании», заключается в том, что измененная последовательность активации приводит к изменению длительностей потенциалов действия, то есть, происходит комбинирование первичных и вторичных изменений реполяризации (рис. 20).
Аритмогенез
Механизмы аритмий делятся на механизмы, основанные на нарушениях образования импульса, нарушениях проведения импульса и комбинированных нарушениях. Нарушения образования импульса 1. Изменения нормального автоматизма за счет нейрогуморальной регуляции (синусовая тахи- и брадикардия). 2. Аномальный автоматизм. Существенное повышение нормального автоматизма. Пример такого изменение – формирование желудочковых тахикардий за счет усиления пейсмейкерной активности волокон Пуркинье под влиянием адреналина. Второй механизм аномального автоматизма – превращение клеток с быстрым ответом в клетки с медленным ответом в ишемизированном миокарде за счет деполяризации потенциала покоя и инактивации натриевых каналов. 3. Триггерная активность. В основе триггерной активности лежат ранние и поздние постдеполяризации (рис. 21), которые возникают после нормального потенциала действия, который рассматривается в этом случае как пусковой фактор, или триггер. Постдеполяризации могут под- и надпороговыми, надпороговые вызывают формирование новых потенциалов действия. Механизм постдеполяризаций до конца не ясен. По наиболее распространенной точке зрения, они возникают при кальциевых перегрузках. В этих условиях один внутриклеточный ион кальция начинает обмениваться на три внеклеточных иона натрия через натрий-кальциевый обменник, что обуславливает входящий (деполяризующий) ток. 4. Деполяризация за счет электротонического взаимодействия, которое проявляется при наличии в миокарде электрических неоднородностей, связанных либо с локальной деполяризацией потенциала покоя, либо с большими различиями во времени реполяризации (рис. 22). Оба случая характерны для ишемизированных областей миокарда.
Реентри Особым аритмогенным механизмом является так называемый повторный вход волны возбуждения, или реентри (reentry). При данных аритмиях волна возбуждения длительно циркулирует в миокарде, возвращаясь к тому участку, откуда она вышла (рис. 23). Для существования реентри необходимо три условия. 1. Однонаправленный блок проведения, который чаще всего возникает в случае большой дисперсии рефрактерности. Такая ситуация может возникать при ранних экстрасистолах или при укорочении сердечного цикла, когда разные потенциалы действия укорачиваются неодинаково. Во всех этих случаях часть миокарда пребывает в рефрактерности, а другая часть уже вышла из этого состояния. 2. Возможность кругового движения волны возбуждения, которая, как правило, основывается на наличии анатомического или функционального препятствия, вокруг которого волна деполяризации циркулирует. Анатомическое препятствие, как правило, предполагает наличие двух путей проведения (см., например, рис. 13), а функциональное представляет собой зону невозбудимости. 3. Замедление проведения возбуждения, которое возможно в случае миогенного проведения (без участия проводящей системы), проведения через зону с медленным ответом или через ишемизированный участок миокарда. Реентри может возникать в дополнительных путях АВ-проведения, месте ветвления рабочих волокон или волокон Пуркинье, между ножками пучка Гиса, в АВ-узле. Реентри характеризуется несколькими параметрами. Во-первых, наличием морфологического субстрата. Во-вторых, величиной «окна возбудимости», то есть зоны миокарда, готового к возбуждению (вышедшего из рефрактерного периода), находящегося перед фронтом волны возбуждения. Чем больше окно возбудимости, тем устойчивее реентри, поэтому гипертрофированные и дилатированные сердца более уязвимы к аритмиям, основанным на реентри. От величины окна возбудимости зависит и принцип лечения. Если окно достаточно велико, в него можно «попасть» электрическим стимулом, привести эту зону в состояние рефрактерности и, таким образом, прервать движение волны возбуждения. Если окно мало, приходится использовать дефибрилляцию. В-третьих, степенью фрагментации волн возбуждения и количеством колец реентри. В-четвертых, стабильностью реентри. На основании этих характеристик, выделяются два основных типа реентри: микрореентри, или случайное, или функциональное реентри, или фибрилляция (функциональный субстрат, небольшое окно возбудимости, фрагментация волн возбуждения, несколько колец реентри, нестабильность); и макро-реентри, или упорядоченное, или анатомическое реентри, или трепетание, или тахикардия (анатомический субстрат, большое окно возбудимости, одно стабильное нефрагментирующееся кольцо реентри). Ионные каналы кардиомиоцитов
|
|||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 163; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.76.111 (0.013 с.) |

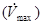 ; наличие и выраженность фаз плато и начальной быстрой реполяризации; длительность потенциала действия и рефрактерного периода.
; наличие и выраженность фаз плато и начальной быстрой реполяризации; длительность потенциала действия и рефрактерного периода.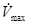 , обусловленная быстрым натриевым током (I Na);
, обусловленная быстрым натриевым током (I Na);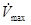 ). Эти параметры определяют «силу влияния» возбужденного кардиомиоцита на соседние клетки: чем больше амплитуда и
). Эти параметры определяют «силу влияния» возбужденного кардиомиоцита на соседние клетки: чем больше амплитуда и 


