Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Раздел I. Специфический клеточный иммунитетСтр 1 из 14Следующая ⇒
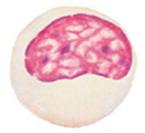
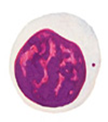
Глава II. ОСНОВЫ ИММУНИТЕТА Раздел I. Специфический клеточный иммунитет I. 1. Разновидности лейкоцитов. Лейкоцитарная формула Лейкоциты – это клетки белой крови. В норме содержание лейкоцитов варьирует в пределах от 4 до 9 тысяч в мкл крови или от 4 до 9 х 10 9 в литре крови. Количество лейкоцитов в объеме крови определяется с помощью счетной камеры Горяева или пикоскела. Среди лейкоцитов различают - эозинофилы, - базофилы, - нейтрофилы, - моноциты, - лимфоциты. Разновидности лейкоцитов идентифицируются в процессе исследования мазка крови в соответствии с - диаметром клетки, - размером и формой ядра, - цветом окрашивания ядра и цитоплазмы, - наличием гранул в цитоплазме. Те клетки, в цитоплазме которых содержатся гранулы, называются гранулоцитами, те, укоторых гранулы отсутствуют– агранулоцитами. Гранулоцитами являются эозинофилы, базофилы и нейтрофилы, агранулоцитами – моноциты и лимфоциты. Нейтрофилы в мазке крови здорового человека могут быть представлены тремя разновидностями – юными, палочкоядерными и сегментоядерными. Структурные особенности нейтрофилов зависят от стадии их развития. У самых молодых клеток (юных или метамиелоцитов), имеет округлую форму. По мере взросления нейтрофилов их ядро приобретает форму двух соединенных палочек. Взрослые клетки характеризуются ядром, состоящим из двух-трех фрагментов (сегментов), соединенных ядерным веществом (рис. I-1).
А Б В Г Д
Рис. I-1. Разновидности лейкоцитов: А – эозинофил, Б – базофил, В – сегментоядерный нейтрофил, Г – моноцит, Д - лимфоцит
Фрагмент антигена, непосредственно взаимодействующий I. 3. Функции Т-лимфоцитов
Рассмотрим роль Т-лимфоцитов в защите организма человека от чужеродных бактерий и вирусов. В популяции Т-лимфоцитов различают две основные субпопуляции
цитотоксические Т-хелперы Т-лимфоциты (Тцтл) (Тh)
В мембране клеток обеих субпопуляций имеется сложная белковая структура, состоящая из двух типов полипептидных цепей, – антигенраспознающий рецептор, формирующийся в процессе антигеннезависимой дифференцировки лимфоцитов. Антигенраспознающие рецепторы – TCR (от T-cell receptor)соединены в мембране лимфоцита с функциональнозначимыми гликопротеинами – корецепторами, обозначаемыми литерами CD (от claster definition/differentiation) с определенной арабской цифрой. Корецепторы содержат несколько полипептидных цепей и участвуют в связывании лимфоцитов с антигеном микроба и передаче информации об этом ядру лимфоцита и другим клеточным включениям.
О Т-хелперах (CD 4) Т-хелперы (от англ. helper – помощник) – это Т-лимфоциты, организующие иммунный процесс. В отличие от Тцтл, Т-хелперы сами не уничтожают чужеродные микроогранизмы, но без их активного участия цитотоксические лимфоциты (и Т-, и В-) осуществлять свою функцию не могут. Среди Т-хелперов различают нулевые Т-хелперы (Th0), Т-хелперы 1-го, 2-го и 3-го типа (Th1, Th2 и Th3 соответственно). В мембране Т-хелперов, как и у цитотаксических Т-лимфоцитов, имеются высокоспецифические антигенраспознающие рецепторы (TCR). И так же, как в субпопуляции Тцтл, в организме человека содержится громадное число небольших по численности разновидностей Т-хелперов (рис. I-4). Корецепторами Т-хелперов являются молекулы CD 4. Функции различных типов Т-хелперов будут обсуждаться в контексте иммунных реакций.
Рис. I-4. Разновидности Т-хелперов
Итак, в борьбу с внедрившимся в организм микробом, маркированным определенным антигеном, включаются предназначенные для распознавания и разрушения этого объекта пулы Т-лимфоцитов – Тцтл и Т- хелперы. Обе субпопуляции лимфоцитов имеют в мембране абсолютно одинаковые антигенраспознающие рецепторы (TCR), комплементарные эпитопу данного антигена, и разные корецепторы.
I. 3. 2. Клонирование Если микробы, впервые атаковавшие организм, способны запустить иммунный ответ, их количество оценивается иммунной системой как опасное. В сравнении с количеством вторгшихся микробов число цитотоксических Т-лимфоцитов, предназначенных для уничтожения этого агрессора, является небольшим.
Напомним, в норме в крови насчитывается от 4 до 9 х 10 9/л всех лейкоцитов. Среди них находятся и Т-лимфоциты, предназначенные для борьбы со всеми природными чужеродными бактериями, вирусами и пр. Очевидно, что пул Т-лимфоцитов с определенным антигенраспознающим рецептором (TCR) весьма ограничен. Исходя из неблагоприятного соотношения «враг – разрушитель врага» в начале иммунного ответа, необходимо пропорционально увеличить (с некоторым преобладанием) пул соответствующих цитотоксических Т-лимфоцитов посредством их клонирования.
II. 1. Функции В-лимфоцитов
В-лимфоциты осуществляют специфический гуморальный иммунитет. Так же, как и Т-лимфоциты, В-лимфоциты располагают антигенраспознающими рецепторами (ВСR – от англ. B-cell receptor) и сложным комплексом корецепторов, обозначаемым CD 5. Кроме этих структур в мембране В-лимфоцитов имеется ряд других костимулирующих молекул, участвующих в передаче сигнала с поверхности мембраны внутрь В-лимфоцита – к ядру клетки и другим органеллам. Антигенраспознающий рецептор В-лимфоцита (ВС R) состоит из мономерной молекулы антитела – иммуноглобулина М или D, связанной с двумя костимулирующими белками.
II. 1. 1. Антитело - ключевое слово в описании функций В-лимфоцитов В-лимфоциты производят антитела и делегируют их для реализации своей функции разрушителей чужеродных микроагентов. Антитело представляет собой белковую молекулу иммуноглобулиновой фракции (Ig), имеющую характерную конформацию латинской буквы Y. Антитело состоит из двух пар полипептидных цепей – двух одинаковых тяжелых цепей (Н-цепи) и двух идентичных легких (L-цепи). Тяжелые цепи друг с другом и легкие цепи с тяжелыми соединены дисульфидными мостиками. В любом антителе имеются центры связывания двух типов
специфические и неспецифические
с антигеном с белками комплемента и фагоцитами
Антигенсвязывающие центры антитела располагаются в области гипервариабельных фрагментов тяжелых и легких цепей (Fab – fragment antigen binding). Специфичность антител определяется аминокислотной последовательностью гипервариабельных областей. Любое антитело может связываться только с комплементарными этим участкам эпитопами антигена по принципу «ключ-замок». Во фрагменте тяжелых цепей, образующих «ножку» буквы Y, имеется неспецифический центр связывания с белками комплемента и с фагоцитирующими клетками крови (Fc – fragment cristallizable) (рис. II-1).
Рис. II-1. Структура антитела
Как и среди Т-лимфоцитов, в субпопуляции В-лимфоцитов еще в процессе антигеннезависимой дифференцировки образуется множество небольших по численности высокоспецифичных пулов В-лимфоцитов. В совокупности эти лимфоциты готовы к встрече со всеми микроорганизмами, представляющими потенциальную угрозу организму человека. Борцы с разными микробами отличаются друг от друга структурой гипервариабельных фрагментов антител, фиксированных в мембране В-лимфоцитов в качестве антигенраспознающих рецепторов (ВС R). На рис. II-2 схематично изображены В-лимфоциты, предназначенные для распознавания и уничтожения различных микроорганизмов.
Рис II-2. В-лимфоциты, предназначенные для распознавания различных антигенов
Классы иммуноглобулинов
Различают пять классов антител-иммуноглобулинов: Ig G, Ig M, Ig A, Ig D и Ig E. Их структура (рис. II-3 А – В) и осуществляемые ими функции в иммунных реакциях различны. Иммуноглобулины G (Ig G) – антитела-мономеры с низкой молекулярной массой, имеют два центра связывания с антигеном (рис. II-3 А). Более всего образуются во вторичном иммунном ответе. Способны легко перемещаться в ткани и эффективно блокировать там антигены. Проникают через плацентарный барьер. Участвуют в активации комплемента по альтернативному пути, стимулируют фагоцитоз.
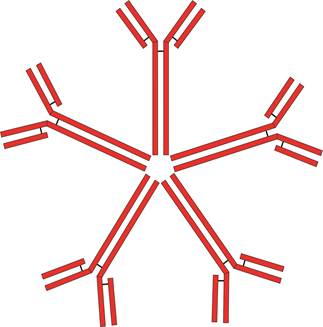
Рис. II-3 А Иммуноглобулины М (Ig M) – антитела-пентамеры. Состоят из пяти соединенных в виде колеса телеги антител-мономеров. Содержат десять центров связывания с антигеном (рис. II-3 Б). Образуются в первичном иммунном ответе. Связываются с белками комплемента, активируя его по классическому пути. Лабораторное выявление Ig M указывает на острый воспалительный процесс.
Рис. II-3 Б Иммуноглобулины А (Ig A) – секреторные иммуноглобулины. Димеры (рис. II-3 В). Содержатся в слюне, желудочном соке, слезной жидкости, в молозиве и грудном молоке, во всех секретах, выделяемых кожей, – в поте, ушной сере, сальном секрете. Блокируют микроорганизмы, проникшие в эти среды. В плазме крови циркулирует другой тип иммуноглобулинов А – мономеров – сывороточные иммуноглобулины.
Рис. II-3 В Иммуноглобулины D (Ig D) – антитела-мономеры. Наряду с мономерами иммуноглобулинов М являются ключевой структурой антигенраспознающего рецептора В-лимфоцитов (ВСR). Иммуноглобулины Е (Ig E) – антитела-мономеры. Реализуют аллергические и противогельминтные иммунные реакции. Фрагмент Fc антител этого типа обладает высокой способностью связываться с гистаминоцитами – тучными клетками и базофилами, вызывая их дегрануляцию, и с эозинофилами. Активированные В-лимфоциты (плазмоциты) обладают уникальной способностью к переключению классов антител: в начале иммуного ответа синтезируются антитела Ig M, через некоторое время вследствие рекомбинации ДНК – Ig G. При первичном иммунном ответе антитела Ig M обнаруживаются в плазме крови примерно через 6 дней со времени внедрения антигена. Титр антител этого класса достигает максимума на 9-10 день. Антитела Ig G выявляются в крови через 10 дней от начала агрессии, а наибольшей концентрации достигают на 21-22 день.
Образование МАК
С белком С7 контактирует белок комплемента С8.
На этом последовательное взаимодействие белков комплемента С5b – С9 завершается (рис. III-2).
Рис. III-2. Формирование мембраноатакующего комплекса на поверхности микроорганизма
12-14 молекул С9 соединяются друг с другом, образуя белковый цилиндр, формирующий пору в клеточной стенке микрообъекта. Сборка мембраноатакующего комплекса завершается (рис. III-3).
Рис. III-3. Мембраноатакующий комплекс
Активация всего каскада классического пути происходит в течение двух-трех минут. Последствия нарушения целостности микрообъекта очевидны. В поврежденную клетку через множество образовавшихся пор (каналов) диаметром около 10 нм диффундируют ионы натрия, осмолярность внутриклеточной жидкости возрастает, и в клетку по осмосу начинает поступать вода. Наступает осмотический лизис микроба. Итак, комплемент является механизмом неспецифического гуморального иммунитета. Неспецифического – потому что белки комплемента связываются с неспецифическим центром связывания антител. Гуморального – в связи с тем, что микрообъекты лизируются посредством белков плазмы крови, циркулирующих в жидких (humor) средах организма.
IV. 1. 1. О нейтрофилах
Нейтрофилы как и все гранулоциты проходят следующие стадии развития: стволовая кроветворная клетка – миелобласт – промиелоцит – миелоцит – метамиелоцит (юный) – палочкоядерный – сегментоядерный. Зрелые нейтрофилы несколько суток находятся в костном мозге, образуя костномозговой резерв. Затем они перемещаются в кровеносные сосуды. В сосудах часть нейтрофилов циркулирует в кровотоке, образуя циркулирующий пул. Другая часть обратимо прикрепляется к эндотелию мелких сосудов, формируя пристеночный пул. Под влиянием ряда факторов – при остром стрессе, физической нагрузке, гипоксии, после еды – происходит мобилизация пристеночного пула. Нейтрофилы покидают эндотелий и поступают в кровоток, увеличивая циркулирующий пул. При повреждении тканей, бактериальной агрессии, накоплении продуктов воспаления нейтрофилы первыми из лейкоцитов начинают перемещаться из кровотока в ткани к очагу воспаления.
IV. 1. 2. О макрофагах Моноциты являются самыми крупными клетками крови. Они образуются в красном костном мозге из стволовой кроветворной клетки и проходят следующий цикл развития: стволовая клетка – монобласт костного мозга – промоноцит – моноцит. Моноциты циркулируют в крови 10-14 часов, а затем мигрируют в ткани. Отметим, что в отличие от нейтрофилов, моноциты перемещаются в ткани трансцеллюлярно, вледствие их захвата эндотелием и выделения экзоцитозом. В тканях клетки продолжают дифференцироваться, в них существенно увеличивается количество лизосом и митохондрий. Теперь эти клетки называются тканевыми макрофагами. Макрофаги присутствуют во всех тканях – в коже, печени, легких, нервной ткани, в костях, селезенке и лимфоузлах. Макрофаги так же, как и нейтрофилы, являются профессиональными фагоцитами. Однако основное войско макрофагов выдвигается на поле боя несколько позже нейтрофилов, в процессе вторичного или иммунного фагоцитоза. Это связано с тем, что ключевыми активаторами макрофагов, усиливающими фагоцитоз, являются молекулы, образующиеся в процессе развития иммунного ответа и связывающиеся с поверхностью микроорганизма – опсонизирующими его.
Опсонизация (от лат. оpsono – приправа, способность делать вкусным) – это связывание поверхности микрообъектов с антителами, белками комплемента и рядом других белков, направленное на усиление фагоцитоза. Иммунные активаторы (молекулярные усилители) фагоцитоза называются опсонинами. Ключевыми опсонинами являются - антитела, секретируемые плазмоцитами; - гамма-интерферон – цитокин, синтезируемый Т-хелперами 1 типа; - некоторые белки комплемента, в основном С3b.
Фагоциты захватывают и разрушают опсонизированные объекты в 5000 раз быстрей, чем неопсонизированные. Эффективность фагоцитоза существенно усиливается в связи с наличием на поверхности макрофагов рецепторов к опсонинам – Fc-фрагментам антител, компоненту комплемента С3b, гамма-интерферону и др.
Макрофаги рецепторами своей мембраны связываются с опсонизированными объектами, заключают в фагосому и переваривают (рис. IV-1 А – В).
А Б В
Рис. IV-1. Начальные стадии фагоцитоза
Тканевые макрофаги очищают поврежденную ткань от погибших в бою нейтрофилов, продуктов распада, не добитых микробов, простейших и пр. В отличие от нейтрофилов, у которых фагосома сливается с гранулами цитоплазмы, в макрофагах происходит соединение фагосомы с лизосомами. Разрушение же поглощенных частиц происходит посредством ферментов лизосом, образования токсичных для оболочки микробов форм кислорода и монооксида азота (NO). После переваривания поглощенных структур макрофаг экзоцитозом выбрасывает продукты деградации, которые затем удаляются из организма почками и желудочно-кишечным трактом.
Фагоцитоз – это ключевой механизм неспецифического клеточного иммунитета. Неспецифического – потому что нейтрофилам и макрофагам глубоко безразлично, кого поедать. Они подвергают деструкции все микроорганизмы, нарушившие целостность барьерных тканей, не взирая на лица агрессоров. Клеточного – поскольку разрушение вторгшихся объектов происходит в результате непосредственного контакта двух структур – фагоцита и микроба. Эозинофилы и базофилы также участвуют в поглощении и лизисе микробов, хотя этот вид защиты организма для данных гранулоцитов не является основным. Эозинофилы и базофилы специализируются на разрушении достаточно крупных структур, каковыми, например, являются личинки некоторых гельминтов, посредством выделения литических веществ в окружающую среду. После опсонизирования личинки гельминта антителами Ig E и Ig G эозинофилы связываются с опсонинами и секретируют на поверхность гельминта два высокотоксичных белка – большой основной протеин и катионный протеин эозинофилов, разрушающие оболочку антигенсодержащего объекта. Базофилы, имеющие, как и эозинофилы, высокое сродство к Ig E и Ig G (Ig G4), также соединяются с антителами, дегранулируются и выделяют на опсонизированный объект провоспалительное вещество гистамин.
Задача № 1 Вторая беременность D-отрицательной женщины протекает неблагоприятно. D-положительный ребенок, родившийся в первой, неотягощенной, беременности, уже подрос и посещает Детский сад. Какие иммунные реакции стали причиной осложнения второй беременности?
Задача № 2 У больного, перенесшего вирусную инфекцию, в плазме крови обнаружены антитела иммунноглобулины М. О чем свидетельствует этот факт? Задача № 3 Вирус иммунодефицита человека преимущественно разрушает Т-хелперы. Каковы возможные последствия инфицирования этим вирусом?
Задача № 4 Продуктами генов системы Резус являются два белка: белок Резус D и белок Резус CE. Белок Резус D является носителем одного резус-антигена – D, а белок Резус CE – двух антигенов (С и Е). Каким образом ученым удалось установить этот факт?
Задача № 5 Мальчик принес домой бродячего кота,искупал и вычесал его. Кот и мальчик стали неразлучными друзьями. Через некоторое время в процессе планового медицинского обследования у ребенка обнаружили эозинофилию и высокий титр иммуноглобулинов Е. В чем возможные причины изменения иммунного статуса мальчика? Задача № 6 Пациенту неправильно определили группу крови. В связи с иногруппной гемотрансфузией эритроциты реципиента подверглись агглютинации. Вследствие чего разрушились агглютинированные эритроциты?
Задача № 7 Что может быть причиной несовместимости матери и плода по системе АВ0, если у матери группа крови 0(I), а у плода – В(III)?
Задача № 8
Цитотоксические Т-лимфоциты уничтожают клетки-мишени, инициируя их апоптоз. Белки системы комплемента разрушают опсонизированный объект посредством осмотического лизиса. Объясните, почему Т-лимфоциты и комплемент применяют разную тактику иммунной защиты.
Ответы на ситуационные задачи Ответ на задачу № 1 В процессе родов, завершивших первую беременность, в кровь матери поступил некоторый объем крови плода. Эритроциты плода запустили специфический гуморальный ответ, уничтоживший D-положительные эритроциты плода и оставивший в крови матери В-лимфоциты памяти. Во время второй беременности попадание в кровь матери небольшого числа эритроцитов D-положительного плода запускает вторичный иммунный ответ. В крови матери интенсивно образуются антитела Ig G, которые преодолевают плацентарный барьер и связываются с эритроцитами плода, опсонизируя их со всеми вытекающими отсюда последствиями.
Ответ на задачу № 2 Антитела Ig M в плазме крови указывают на первичный иммунный ответ.
Ответ на задачу № 3 Уменьшение содержания Т-хелперов – ключевых организаторов иммунного процесса – лишает больного СПИДом возможности противостоять инфекциям. Снижение иммунной защиты делает больного подверженным тем инфекциям, с которыми при сохранных Т-хелперах иммунная система смогла бы успешно бороться. Ответ на задачу № 4 Белок Резус D инициирует иммунную реакцию в виде выработки антител одного типа – анти-D, в то время как белок Резус CE запускает образование антител двух типов – анти-C и анти-E. Ответ на задачу № 5 Эозинофилия и высокое содержание Ig E могут свидетельствовать - о возникновении крапивницы на какие-либо факторы, связанные с присутствием кота в доме, и/или - о гельминтной инвазии (которая тоже, кстати, может сопровождаться крапивницей).
Ответ на задачу № 6 Агглютинация – это связывание эритроцитов одной группы крови антителами, соответствующими их антигенам. С неспецифическими центрами связывания антител соединяется белок системы комплемента С1, активируется, приобретает свойства протеолитического фермента и запускает активацию прочих белков комплемента. Активация комплемента завершается формированием множества мембраноатакующих комплексов на поверхности агглютинированных эритроцитов. Поврежденные эритроциты подвергаются осмотическому лизису.
Ответ на задачу № 7
Естественные антитела анти-А и анти-В являются иммуноглобулинами М и поэтому не проникают через плаценту в кровь плода. У небольшого числа женщин значительное число естественных антител принадлежат к иммуноглобулинам G, которые поступают в кровь плода и агглютинируют его эритроциты.
Ответ на задачу № 8
Тцтл специализируются на борьбе с внутриклеточными микрообъектами, следовательно, с теми клетками организма, в которых происходит репродукция микробов. Перфорация мембраны инфицированной клетки без одновременного запуска апоптоза вызвала бы осмотический лизис клетки, в которой стремительно размножаются патогенные микробы. Эволюция выбрала единственный разумный способ уничтожения внедрившихся агентов – апоптоз. Клетка, в которой запущен механизм апоптоза, разрушается обреченно, но без драматизма, вместе со всем своим содержимым. Лизис инфицированной клетки не сопровождается распространением микробов и развитием воспаления. Мембраноатакующий комплекс уничтожает объекты, репродукция которых происходит во внеклеточной среде, поэтому осмотический лизис или фагоцитоз подобных мишеней – простое и верное решение.
Содержание Стр.
Введение…………………………………………………………………………………………..
Глава I. Состав и свойства крови. Эритроциты. ………………………………… Раздел I. Состав и свойства крови………………………………………………………… I. 1. Гематокрит…………………………………………………………………………………….. I. 2. Функции крови………………………………………………………….. I. 3. Функции минеральных веществ плазмы крови………………………. I. 4. Функции белков плазмы крови………………………………………….. I. 5. Тесты для контроля знаний раздела I…………………………………… Раздел II. Структурно-функциональные особенности эритроцитов. Гемоглобин. СОЭ……………………………………………………………….. II. 1. Эритроциты………………………………………………………………… II. 2. Гемоглобин……………………………………………………………… II. 3. Индексы эритроцитов…………………………………………………… II. 4. Скорость оседания эритроцитов (СОЭ)…………………………………. II. 5. Тесты для контроля знаний раздела II………………………………………………. II. 5. 1. Правильные ответы на тестовые задания разделов I и II……………. II. 5. 2. Ситуационные задачи по главе I с ответами…………………………
Глава II. Основы иммунитета …………………………………………………. Раздел I. Специфический клеточный иммунитет………………………………. I. 1. Разновидности лейкоцитов. Лейкоцитарная формула…………………. I. 2. Роль лимфоцитов в иммунной защите………………………………….. I. 2. 1. Функции Т-лимфоцитов……………………………………………….. I. 2. 1. 1. Представление антигена Т-лимфоцитам…………………………… I. 2. 1. 2. Клонирование……………………………………………………….. I. 2. 1. 3. Где сейчас находятся микрообъекты, внедрившиеся в барьерные ткани, и что с ними происходит……………………………………………… I. 2. 1. 4. Каковы дальнейшие действия Тцтл……………………….............. I. 2. 1. 5. Как Тцтл уничтожает инфицированную клетку…………………. Раздел II. Специфический гуморальный иммунитет………………………… II. 1. Функции В-лимфоцитов…………………………………………………. II. 1. 1. Антитело - ключевое слово в описании функций В-лимфоцитов…. II. 1. 2. Как происходит презентация антигена В-лимфоцитам…………….. II. 1. 3. Как В-лимфоциты осуществляют цитотоксическую функцию……. Раздел III. Неспецифический гуморальный иммунитет……………………. III. 1. Система комплемента…………………………………………………… III. 1. 1. Классический путь активации комплемента……………………….. III. 1. 2. Альтернативный путь активации комплемента…………………….. Раздел IV. Неспецифический клеточный иммунитет………………………. IV. 1. Фагоцитоз……………………………………………………………….. IV. 1. 1. О нейтрофилах……………………………………………………….. IV. 1. 1. 1. Как нейтрофилы узнают, где находится очаг повреждения…… IV. 1. 1. 2. Каков механизм лизиса микроорганизмов нейтрофилами……… IV. 1. 2. О макрофагах…………………………………………………………. IV. 2. О естественных киллерах……………………………………………….. V. Тесты для контроля знаний главы II…………………………………………………… V. 1. Правильные ответы на тестовые задания главы II…………………………… V. 2. Ситуационные задачи по главе II с ответами…………………………… Заключение…………………………………………………………………….110
В пособии представлены современные данные о функциях эритроцитов и лейкоцитов, успешно восполняющие актуальный учебный материал, не получивший достаточного освещения в существующих учебниках по физиологии человека. Пособие отличает необычная структура текста, лаконичный и ясный стиль изложения. Все ключевые элементы, рассматриваемые в учебной работе, прекрасно иллюстрированы, что делает увлекательным и доступным изучение сложных вопросов функционирования иммунной системы организма. Содержание пособия способствует формированию функционального мышления, являющегося базой профессиональной деятельности врача. Пособие предназначено для студентов медицинских и биологических специальностей, изучающих физиологию человека.
УДК 612.1 ББК 54.11 Ш30 Кабардино-Балкарский государственный университет, 2013
Л.З. Шауцукова
Физиология эритроцитов и лейкоцитов. Основы иммунитета Глава II. ОСНОВЫ ИММУНИТЕТА Раздел I. Специфический клеточный иммунитет
|
||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 116; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.218.184 (0.148 с.) |
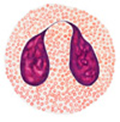









 На поверхности чужеродного объекта рядом с фрагментом С5b адсорбируется белок комплемента С6.
На поверхности чужеродного объекта рядом с фрагментом С5b адсорбируется белок комплемента С6. С белком С6 связывается белок комплемента С7, который заякоревает комплекс белков: встраивает его в мембрану.
С белком С6 связывается белок комплемента С7, который заякоревает комплекс белков: встраивает его в мембрану. Белок С8 связывается с белком С9.
Белок С8 связывается с белком С9.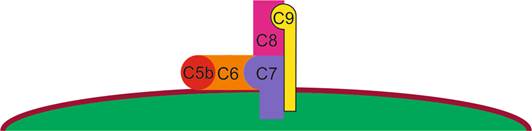
 Затем происходит полимеризация белка С9 – многократное присоединение друг к другу одинаковых молекул С9.
Затем происходит полимеризация белка С9 – многократное присоединение друг к другу одинаковых молекул С9.