
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
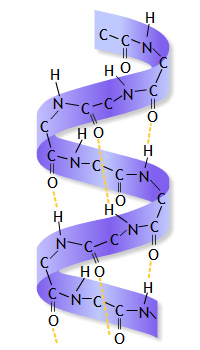
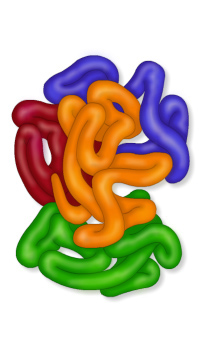
Первичная, вторичная, третичная и четвертичная структура белка ⇐ ПредыдущаяСтр 3 из 3
Химические свойства белков В зависимости от молекулярной массы и функциональных групп белки могут как хорошо растворяться в воде, так и не растворяться в ней. Под действием температуры, растворов солей тяжёлых металлов, кислот и щелочей происходит разрушение вторичной, третичной и четвертичной структуры белка, называемое денатурацией. При нагревании в присутствии кислоты или щёлочи белки подвергаются гидролизу, распадаясь на исходные аминокислоты. Белки в щелочной среде в присутствии сульфата меди (II) окрашивают раствор в красно-фиолетовый цвет. Это реакция на пептидную группу (биуретовая реакция). Концентрированная азотная кислота при нагревании окрашивает белки в жёлтый цвет, если в состав белка входят остатки ароматических аминокислот, например, фенилаланина (ксантопротеиновая реакция). Для обнаружения в составе белка атомов серы проводят реакцию с ацетатом свинца в щелочной среде при нагревании. В результате образуется чёрный осадок (цистеиновая реакция).
Превращения белков в организме Белки являются обязательными компонентами в пищевом рационе человека. В организме человека белки, поступившие с пищей, под действием ферментов подвергаются гидролизу и разлагаются на отдельные аминокислоты. Эти аминокислоты – строительный материал для образования новых белков, необходимых человеку. Для синтеза белков необходима энергия, которую поставляет в организме АТФ. Также энергия выделяется при распаде жиров и углеводов. Кроме синтеза белков происходит их распад с образованием углекислого газа, аммиака, мочевины и воды. Успехи в изучении и синтезе белков В 1954 г. британский биолог Фредерик Сенгер впервые расшифровал строение белка инсулина. Каждая молекула инсулина состоит из двух полипептидов, в одном из которых 21 остаток аминокислоты, а в другом – 30 аминокислотных остатков. В 1967 г. был создан прибор – секвенатор, позволяющий определять последовательность остатков аминокислот в макромолекуле белка. Первый белок, синтезированный в лаборатории в 1953 г. был окситоцин. В настоящее время развивается наука, которая занимается синтезом искусственных белков, – генная инженерия. ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ
1. Решение задачи на вычисление массовой доли элемента в молекуле аминокислоты. Условие задачи: вычислите массовую долю азота в молекуле аспаргина
Шаг первый: вычислить относительную молекулярную массу молекулы аспаргина: М = 4·12 + 8·1 + 2·14 + 3·16 = 132 а.е.м. Шаг второй: определить количество атомов азота в молекуле аспаргина и определить их относительную атомную массу: 2·14 = 28 а.е.м. Шаг третий: определить массовую долю азота как отношение относительной атомной массы азота к относительной молекулярной массе аспаргина: (28: 132)·100 = 21,2 %. Ответ: 21,2. 2. Решение задачи на определение количества различных олигопептидов, которые можно получить из определённого набора аминокислот. Условие задачи: Сколько ди- и трипептидов можно составить из двух молекул аланина и одной молекулы цистеина? Шаг первый: определить количество возможных дипептидов. Из двух молекул аланина и одной молекулы цистеина можно составить три дипептида: Ala-Ala, Ala-Cys и Cys-Ala (два последних дипептида – разные соединения, так как в молекуле Ala-Cys карбоксильная группа аланина соединяется с аминогруппой цистеина, а в молекуле Cys-Ala карбоксильная группа цистеина соединяется с аминогруппой аланина). Шаг второй: определить количество возможных трипептидов. Ala-Ala-Cys, Ala-Cys-Ala, Cys-Ala-Ala – возможно составить 3 трипептида. Ответ: 3 дипептида и 3 трипептида. Основные источники Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Домашнее задание. Ответить письменно на задания. 1.В чем причина несовместимости при пересадке органов от одного организма к другому? (Для тканей каждого организма характерен свой индивидуальный набор белков). 2.Научное название белков. (протеины). 3.Из чего построены молекулы белков? (из остатков аминокислот). 4.Сколько структур белка существует? (4). 5.Структура белка, свернутая в спираль? (вторичная). 6.Как называется четвертичная структура белка? (глобула). 7.Как называется связь - NH – CO -? (пептидная). 8.Разрушение структуры белка. (денатурация).
9.Реакции, определяющие наличие белка? (ксантопротеиновая, биуретовая). 19.Пищевые продукты с большим содержанием белка. 20.Самая неустойчивая структура белка? (четвертичная). Критерии оценивания знаний. 5 баллов – за развернутый, точный и уникальный ответ в пределах оговоренного задания; 4 балла – за неточный, неуникальный или излишне длинный ответ; 3 балла – за попытку ответить хотя бы что-то на поставленный вопрос; 2 балла – за несоответствие ответа заданию; 1 балл – за невнятные символы вместо ответа; 0 баллов – за полное отсутствие ответа.
|
|||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 235; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.134.90.44 (0.007 с.) |





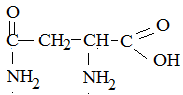 . Ответ запишите с точностью до десятых долей.
. Ответ запишите с точностью до десятых долей.


