
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Преподаватель: Ларионова Н.К.Содержание книги
Поиск на нашем сайте
Дисциплина: ОДБ.09 Химия Группа: ТЭЭО-20 1/9 Дата: 20.10.2020 Преподаватель: Ларионова Н.К. Задание: Документ или фото выполненной работы прислать по адресу: kitdistergo@mail.ua (Название файла с ответами: № занятия, дисциплина, группа, Фамилия, имя, студента). Например: 14-Химия, ТЭЭО-20, Сидоров М. Сроки выполнения:20.10.2020 Задания для дистанционного обучения будут выдаваться в день проведения занятия, согласно расписанию и подмен по адресу: https://s3320.nubex.ru/5989/ или https://vk.com/id314054111 Занятие № 14 Тема: Амины. Аминокислоты и белки. Цель: Дидактическая Изучить строение, изомерию, номенклатуру аминокислот, их химические свойства и биологическое значение; узнать о строении пептидов; познакомиться со структурой белков, их химическими свойствами, с успехами в их изучении и синтезе. Развивающая Развитие внимательности, наблюдательности и умений выделять главное при оценке различных процессов, явлений и факторов; развитие умений грамотно, четко и точно выражать мысли. Воспитательная Воспитание творческого отношения к учебной деятельности. Воспитание бережливого отношения к окружающей среде. Воспитание сознательной дисциплины и норм поведения обучающихся. Способствовать овладению необходимыми навыками самостоятельной учебной деятельности.
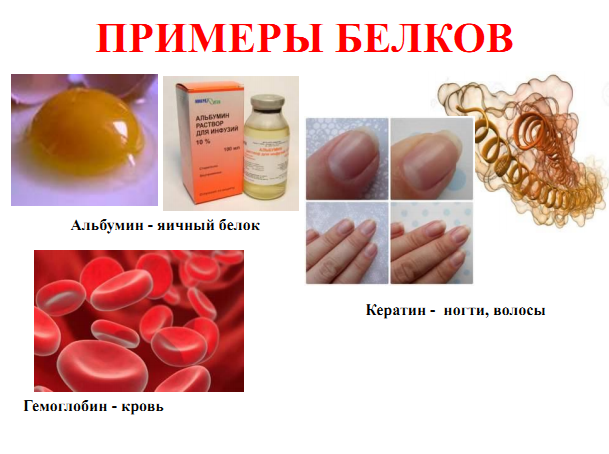
План: 1. Амины. 2.Аминокислоты. 3.Белки. Мотивация А знаете ли Вы: 1. Белок никогда не переходит в жир – совет врача-диетолога. 2. Образование морщин связано с уменьшением натурального белка коллагена. Впрыскиванием его в верхний слой кожи коллаген возмещается. Почти все мелкие и крупные морщины можно корректировать этой терапией – совет врача-косметолога. 3. Современное название белков-ферментов – энзимы. 4. Выработка иммунитета – это важная защитная функция белка. Диета снижает иммунитет. 5. Изучение белков позволило ответить на вопросы, почему одни люди высокого роста, а другие низкого, одни полные, другие худые, одни медлительные, другие проворные, одни сильные, другие слабые. Лекция №14
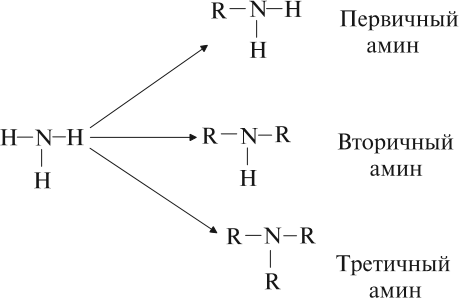
1.Амины. Амины — органические соединения, которые можно рассматривать как производные аммиака, в котором атомы водорода (один или несколько) замещены на углеводородные радикалы.
Названия первичных аминов обычно производят от названий соответствующих углеводородов, добавляя к ним приставку амино- или окончание -амин. Названия вторичных и третичных аминов чаще всего образуют по принципам рациональной номенклатуры, перечисляя имеющиеся в соединении радикалы:
Физические свойства. Простейшие алифатические амины при нормальных условиях представляют собой газы или жидкости с низкой температурой кипения, обладающие резким запахом. Все амины являются полярными соединениями, что приводит к образованию водородных связей в жидких аминах, и следовательно, температурыих кипения превышают температуры кипения соответствующих алканов. Первые представители ряда аминов растворяются в воде, по мере роста углеродного скелета их растворимость в воде уменьшается. Амины растворимы также в органических растворителях. Анилин C6H5NH2 — важнейший из ароматических аминов. Он представляет собой бесцветную маслянистую жидкость, мало растворимую в воде. Анилин применяется для получения красителей, лекарственных препаратов, пластмасс и т. д
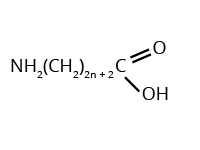
2. Аминокислоты – это азотсодержащие органические соединения, в состав которых входят как аминогруппа, так и карбоксильная группа. Аминокислоты – кристаллические вещества без цвета и запаха, сладковатые на вкус. Хорошо растворяются в воде. Аминокислоты могут реагировать друг с другом. Соединения, образованные более чем 50 остатками аминокислот с помощью пептидной связи, называются белками. Это природные полимеры, которые образуют клетки всех живых организмов. Белки образованы атомами углерода, водорода, кислорода и азота. Кроме этого, белки могут содержать атомы других элементов. В зависимости от молекулярной массы и функциональных групп белки могут, как хорошо растворяться в воде, так и не растворяться в ней. Генная инженерия занимается синтезом белков. Аминокислоты – это азотсодержащие органические соединения, в состав которых входят как аминогруппа, так и карбоксильная группа Простейшим представителем аминокислот является глицин – аминоуксусная (аминоэтановая) кислота По международной номенклатуре нумерация углеродных атомов начинается от углерода карбоксильной группы. Достаточно часто в литературе можно встретить обозначения углеродных атомов в аминокислотах с помощью букв греческого алфавита. При этом атом углерода карбонильной группы не имеет обозначения.
Для некоторых аминокислот существуют тривиальные названия. Изомеры аминокислот различаются строением углеводородного радикала и положением аминогруппы. Все α-аминокислоты, кроме глицина, имеют в своем составе асимметрический атом, который следует сразу за карбоксильной группой. У этого атома углерода все заместители разные. В природе распространены только L-α-аминокислоты. Получение аминокислот В промышленности α-аминокислоты получают гидролизом белков. Можно синтезировать аминокислоты из хлорпроизводных карбоновых кислот и аммиака. Cl-CH2-COOH + 2NH3 → NH2-CH2-COOH + NH4Cl Пептиды Аминокислоты могут реагировать друг с другом, аминогруппа одной кислоты соединяется с карбоксильной группой другой кислоты, при этом происходит выделение воды. Группа атомов СО-NH называется пептидной (или амидной) группой, а связь между атомами углерода и азота – пептидной (амидной) связью. Белки Полипептиды, содержащие в своём составе более 50 остатков аминокислот, называются белками. Это природные полимеры, которые образуют клетки всех живых организмов. Без белков невозможно обмен веществ, размножение и рост живых организмов. Белки образованы атомами углерода, водорода, кислорода и азота. Кроме этих атомов, макромолекулы белков могут содержать атомы фосфора, серы, железа и других элементов. Относительная молекулярная масса белковых молекул может быть от нескольких десятков до сотен атомных единиц массы.
Структура белков Последовательность остатков аминокислот в молекуле белка образует первичную структуру белка. Между атомом кислорода в группе С=О и атомом водорода в амидной группе – NH – образуется водородная связь, в результате чего макромолекула белка закручивается в спираль. Образуется вторичная структура белка.
В результате образуется третичная структура белка, которая определяет специфическую биологическую активность белков. Именно благодаря уникальной третичной структуре биологические катализаторы – ферменты обладают уникальной избирательностью. Благодаря различным функциональным группам белковые молекулы могут соединяться друг с другом, в результате формируется четвертичная структура белка. Химические свойства белков В зависимости от молекулярной массы и функциональных групп белки могут как хорошо растворяться в воде, так и не растворяться в ней. Под действием температуры, растворов солей тяжёлых металлов, кислот и щелочей происходит разрушение вторичной, третичной и четвертичной структуры белка, называемое денатурацией. При нагревании в присутствии кислоты или щёлочи белки подвергаются гидролизу, распадаясь на исходные аминокислоты. Белки в щелочной среде в присутствии сульфата меди (II) окрашивают раствор в красно-фиолетовый цвет. Это реакция на пептидную группу (биуретовая реакция). Концентрированная азотная кислота при нагревании окрашивает белки в жёлтый цвет, если в состав белка входят остатки ароматических аминокислот, например, фенилаланина (ксантопротеиновая реакция). Для обнаружения в составе белка атомов серы проводят реакцию с ацетатом свинца в щелочной среде при нагревании. В результате образуется чёрный осадок (цистеиновая реакция).
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ 1. Решение задачи на вычисление массовой доли элемента в молекуле аминокислоты. Условие задачи: вычислите массовую долю азота в молекуле аспаргина
Шаг первый: вычислить относительную молекулярную массу молекулы аспаргина: М = 4·12 + 8·1 + 2·14 + 3·16 = 132 а.е.м. Шаг второй: определить количество атомов азота в молекуле аспаргина и определить их относительную атомную массу: 2·14 = 28 а.е.м. Шаг третий: определить массовую долю азота как отношение относительной атомной массы азота к относительной молекулярной массе аспаргина: (28: 132)·100 = 21,2 %. Ответ: 21,2. 2. Решение задачи на определение количества различных олигопептидов, которые можно получить из определённого набора аминокислот. Условие задачи: Сколько ди- и трипептидов можно составить из двух молекул аланина и одной молекулы цистеина? Шаг первый: определить количество возможных дипептидов. Из двух молекул аланина и одной молекулы цистеина можно составить три дипептида: Ala-Ala, Ala-Cys и Cys-Ala (два последних дипептида – разные соединения, так как в молекуле Ala-Cys карбоксильная группа аланина соединяется с аминогруппой цистеина, а в молекуле Cys-Ala карбоксильная группа цистеина соединяется с аминогруппой аланина). Шаг второй: определить количество возможных трипептидов. Ala-Ala-Cys, Ala-Cys-Ala, Cys-Ala-Ala – возможно составить 3 трипептида. Ответ: 3 дипептида и 3 трипептида. Основные источники Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Домашнее задание. Ответить письменно на задания. 1.В чем причина несовместимости при пересадке органов от одного организма к другому? (Для тканей каждого организма характерен свой индивидуальный набор белков). 2.Научное название белков. (протеины). 3.Из чего построены молекулы белков? (из остатков аминокислот). 4.Сколько структур белка существует? (4). 5.Структура белка, свернутая в спираль? (вторичная). 6.Как называется четвертичная структура белка? (глобула). 7.Как называется связь - NH – CO -? (пептидная). 8.Разрушение структуры белка. (денатурация). 9.Реакции, определяющие наличие белка? (ксантопротеиновая, биуретовая). 19.Пищевые продукты с большим содержанием белка. 20.Самая неустойчивая структура белка? (четвертичная). Критерии оценивания знаний. 5 баллов – за развернутый, точный и уникальный ответ в пределах оговоренного задания;
4 балла – за неточный, неуникальный или излишне длинный ответ; 3 балла – за попытку ответить хотя бы что-то на поставленный вопрос; 2 балла – за несоответствие ответа заданию; 1 балл – за невнятные символы вместо ответа; 0 баллов – за полное отсутствие ответа.
Дисциплина: ОДБ.09 Химия Группа: ТЭЭО-20 1/9 Дата: 20.10.2020 Преподаватель: Ларионова Н.К. Задание: Документ или фото выполненной работы прислать по адресу: kitdistergo@mail.ua (Название файла с ответами: № занятия, дисциплина, группа, Фамилия, имя, студента). Например: 14-Химия, ТЭЭО-20, Сидоров М. Сроки выполнения:20.10.2020 Задания для дистанционного обучения будут выдаваться в день проведения занятия, согласно расписанию и подмен по адресу: https://s3320.nubex.ru/5989/ или https://vk.com/id314054111 Занятие № 14 Тема: Амины. Аминокислоты и белки. Цель: Дидактическая Изучить строение, изомерию, номенклатуру аминокислот, их химические свойства и биологическое значение; узнать о строении пептидов; познакомиться со структурой белков, их химическими свойствами, с успехами в их изучении и синтезе. Развивающая Развитие внимательности, наблюдательности и умений выделять главное при оценке различных процессов, явлений и факторов; развитие умений грамотно, четко и точно выражать мысли. Воспитательная Воспитание творческого отношения к учебной деятельности. Воспитание бережливого отношения к окружающей среде. Воспитание сознательной дисциплины и норм поведения обучающихся. Способствовать овладению необходимыми навыками самостоятельной учебной деятельности.
План: 1. Амины. 2.Аминокислоты. 3.Белки. Мотивация А знаете ли Вы: 1. Белок никогда не переходит в жир – совет врача-диетолога. 2. Образование морщин связано с уменьшением натурального белка коллагена. Впрыскиванием его в верхний слой кожи коллаген возмещается. Почти все мелкие и крупные морщины можно корректировать этой терапией – совет врача-косметолога. 3. Современное название белков-ферментов – энзимы. 4. Выработка иммунитета – это важная защитная функция белка. Диета снижает иммунитет. 5. Изучение белков позволило ответить на вопросы, почему одни люди высокого роста, а другие низкого, одни полные, другие худые, одни медлительные, другие проворные, одни сильные, другие слабые. Лекция №14
1.Амины. Амины — органические соединения, которые можно рассматривать как производные аммиака, в котором атомы водорода (один или несколько) замещены на углеводородные радикалы. Названия первичных аминов обычно производят от названий соответствующих углеводородов, добавляя к ним приставку амино- или окончание -амин. Названия вторичных и третичных аминов чаще всего образуют по принципам рациональной номенклатуры, перечисляя имеющиеся в соединении радикалы:
Физические свойства. Простейшие алифатические амины при нормальных условиях представляют собой газы или жидкости с низкой температурой кипения, обладающие резким запахом. Все амины являются полярными соединениями, что приводит к образованию водородных связей в жидких аминах, и следовательно, температурыих кипения превышают температуры кипения соответствующих алканов. Первые представители ряда аминов растворяются в воде, по мере роста углеродного скелета их растворимость в воде уменьшается. Амины растворимы также в органических растворителях.
Анилин C6H5NH2 — важнейший из ароматических аминов. Он представляет собой бесцветную маслянистую жидкость, мало растворимую в воде. Анилин применяется для получения красителей, лекарственных препаратов, пластмасс и т. д
2. Аминокислоты – это азотсодержащие органические соединения, в состав которых входят как аминогруппа, так и карбоксильная группа. Аминокислоты – кристаллические вещества без цвета и запаха, сладковатые на вкус. Хорошо растворяются в воде. Аминокислоты могут реагировать друг с другом. Соединения, образованные более чем 50 остатками аминокислот с помощью пептидной связи, называются белками. Это природные полимеры, которые образуют клетки всех живых организмов. Белки образованы атомами углерода, водорода, кислорода и азота. Кроме этого, белки могут содержать атомы других элементов. В зависимости от молекулярной массы и функциональных групп белки могут, как хорошо растворяться в воде, так и не растворяться в ней. Генная инженерия занимается синтезом белков. Аминокислоты – это азотсодержащие органические соединения, в состав которых входят как аминогруппа, так и карбоксильная группа Простейшим представителем аминокислот является глицин – аминоуксусная (аминоэтановая) кислота По международной номенклатуре нумерация углеродных атомов начинается от углерода карбоксильной группы. Достаточно часто в литературе можно встретить обозначения углеродных атомов в аминокислотах с помощью букв греческого алфавита. При этом атом углерода карбонильной группы не имеет обозначения. Для некоторых аминокислот существуют тривиальные названия. Изомеры аминокислот различаются строением углеводородного радикала и положением аминогруппы. Все α-аминокислоты, кроме глицина, имеют в своем составе асимметрический атом, который следует сразу за карбоксильной группой. У этого атома углерода все заместители разные. В природе распространены только L-α-аминокислоты.
|
||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.60.214 (0.011 с.) |




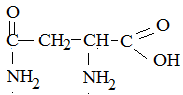 . Ответ запишите с точностью до десятых долей.
. Ответ запишите с точностью до десятых долей.


