
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Использование тепловых диаграмм и таблиц для нахождения основных характеристик паровой турбины. ⇐ ПредыдущаяСтр 5 из 5
Цель работы: определение кпд и мощности по диаграмме i-s для водяного пара. Приборы и оборудование: i - s -диаграмма для водяного пара, справочникам по теплофизическим свойствам жидкостей и газов, карандаш, резинка стиральная, линейка, инженерный калькулятор. Краткие теоретические сведения.
В паровой турбине рабочим телом является пар. Получают его из воды, Поступая на рабочие лопатки турбины пар совершает работу. Часть энергии пара переходит в механическую энергию турбины, на валу которой находится генератор электрической энергии. Паровая турбина-тепловой двигатель. Превращение воды в пар, перегрев пара и его расширение на лопатках турбины, а затем охлаждение в конденсаторе можно представить в виде термодинамических процессов. Если рассматривать идеальную паровую турбину, то термодинамические процессы, связанные с превращениями рабочего тела-водяного пара, это хорошо известные нам 4 термодинамических процесса: изохорный, изобарный, изотермический, адиабатный. Основным законом, используемым для анализа тепловых процессов в паровой турбине, является первое начало термодинамики. Уравнение первого закона термодинамики имеет следующий вид: Q = (U2 – U1) + L, (6-1) где Q - количество теплоты, подведенной (отведенной) к системе; L - работа, совершенная системой (над системой); (U2 – U1) =∆U - изменение внутренней энергии в данном процессе. Если подводится бесконечно малое количество теплоты, то δQ= dU +δL (6-2). Внимание: э то запись первого начала в дифференциальной форме, в то время как формулу (6-1) называют записью первого начала в интегральной форм е. В таком виде первое начало используется при анализе так называемых равновесных процессов, когда давление внутри термодинамической системы и во внешней среде одинаковы. Единственным видом работы в таком процессе является механическая работа (работа изменения объёма) δ L = P· dV. L=
Если давление внешней среды не равно давлению внутри термодинамической системы, то работа, совершаемая термодинамической системой (её называют по разному- техническая, полезная внешняя, работа по изменению давлении) определяется, как L*= - Удельные значения величин, входящих в приведенные выше уравнения, находятся делением их значений на массу рабочего вещества: u= U / m; i = I / m. v = V / m и т. д. Все процессы рассматриваются как обратимые. Это означает, что при совершении подобных процессов, как в прямом, так и в обратном направлении, термодинамическая система возвращается в исходное состояние без каких- либо изменений в окружающей среде. При необратимых процессах система уже не может вернуться в исходное состояние без изменений в окружающей среде. Саади Карно ещё в начале 19 века показал в своих работах, что тепловой двигатель может совершать полезную работу, если совершает замкнутый процесс или цикл. В результате такого процесса рабочее тело должно возвратиться в первоначальное состояние. Совершаемый рабочим телом цикл можно представить состоящим из нескольких простых процессов. Изучая каждый процесс в отдельности, можно определить все необходимые параметры и функции состояния, а затем рассчитать полезную работу и коэффициент полезного действия конкретного теплового двигателя. Полезная работа за цикл определяется сложением работ всех процессов, из которых состоит цикл, с учётом их знака: (+) или (-) В этом и заключается основная задача технической термодинамики в применении к тепловым агрегатам: умение проводить теплотехнические расчёты и находить нужные параметры.
Д ля термодинамических расчётов используют таблицы и термические диаграммы. Расчёты по данным таблиц более точны, по диаграммам - более просты. Для водяного пара удобной диаграммой является диаграмма i - s. Она строится на основе табличных данных и каждая её точка позволяет определить пять параметров и функций состояния как влажного, так и перегретого пара: давление, удельный объём, температуру, удельные энтальпию и энтропию. Удельную внутреннюю энергию можно найти, используя ф-лу (6-9). Если указан процесс, который совершает пар, и заданы начальные и конечные его параметры, то можно рассчитать работу процесса (ф-ла6- 4) и определить теплоту (ф-ла 6- 5). Используя ф-лы (6-5), (6-9), можно рассчитать техническую работу пара, поступающего на лопатки турбины. Идеальная паровая турбина работает по циклу Ренкина. Применение основных уравнений технической термодинамики к циклу Ренкина для паровой турбины, позволяет получить следующие выражения для расчёта её термической мощности и к.п.д.: Nт = (i1 – i2)· М, (Вт) (6-10); ηt = (i1 – i2)/(i1 – i3) (6-11), i3 – энтальпия воды при давлении Р2. Прямая 2’ -3 изображает изохорный процесс сжатия воды до конечного давления пара Р1. Вода практически несжимаема, поэтому процесс сжатия является изохорным. Эту работу сжатия совершает насос. Теплота, в которую превращается работа по сжатию, гораздо меньше теплоты q1, которая идёт на превращение воды в пар и его перегрев, поэтому ею можно пренебречь, а процесс считать одновременно и адиабатным. . Теплота q1 подводится в результате 3-х процессов: 3-4 изобарный процесс подвода теплоты, в результате которого вода доводится до кипения и превращается в пар при постоянном давлении и постоянной температуре; 4-1 изобарный перегрев пара. Из пароперегревателя пар поступает в турбину. Этот быстро протекающий процесс можно считать адиабатным (без подвода и отвода теплоты): 1-2 адиабатное расширение пара в турбине, в результате которого совершается полезная работа. Пар становится влажным и поступает в конденсатор. Здесь он охлаждается проточной водой (изобарно-изотермический процесс 2-2’) и превращается в воду, при этом от него отводится тепло q2; цикл завершается.
Выполнение работы. Процесс расширения пара в турбине - адиабатный. Проведём полный термодинамический расчёт адиабатного процесса, используя i - s диаграмму. Задание 1. Изучить диаграмму i - s, т.е. определить изображение на ней основных термодинамических процессов (расположение изобар, изохор, изотерм, адиабат), а так же расположение кривых степени сухости (х=1 и др.) для влажного пара. Изобары (сплошные линии) идут из правого верхнего угла в левый нижний. Единицы измерения Мпа (1 Мпа = 106 Па= 10 бар). Изохоры - пунктирные линии) начинаются там же, где изобары, идут так же из правого верхнего угла в левый нижний, но круче. Изотермы в области влажного пара совпадают с изобарами, но на кривой х=1 (отделяющей пар влажный от сухого перегретого) раздваиваются и идут вправо. Адиабаты (изоэнтропы, линии равной энтропии)- вертикальные прямые. Выполнение задания. Изучили диаграмму i - s, нашли расположение на ней изобар, изохор, изотерм, адиабат, кривых степени сухости. Задание 2. Пар, начальные параметры которого Р1 = 1 Мпа, Т1=250 0С, в результате адиабатного расширения переходит в другое равновесное состояние с параметрами равным Р2 = 0,1 Мпа, температурой Т2. Определить: удельные объёмы пара в начальном v 1 и конечном состояниях, v 2 , конечную температуру Т2, изменения энтальпии, энтропии, внутренней энергии, а так же теплоту и работу процесса. Выполнение задания. Находим на диаграмме кривые линии, изображающие изобару Р1 = 1 МПа и изотерму Т1 = 250° С. На их пересечении отмечаем точку 1. Она характеризует начало адиабатного процесса. Опускаем из неё перпендикуляр на ось энтропии (горизонтальная ось), округляем значения до цены деления клетки (0,1 кДж/ кг град), или половины клетки (0,05 кдж/кг град) и находим начальное значение энтропии: s 1 ( кДж/ кг град). Значение удельного объёма находим по ближайшей изохоре (слева или справа от точки, а возможно и к середине отрезка между двумя изохорами; в этом случае складываем значения изохор и делим на 2); v 1 (м3/ кг). Опускаем перпендикуляр на ось энтальпии (вертикальная ось) и находим значения i 1 ( кДж/кг). Результат округляем до цены деления клетки (40 кДж/кг или половины клетки 20 кдж/ кг). Начальное значение удельной внутренней энергии определяем по формуле (6-7) i = u + p · v; u = i – p · v; u 1 = i 1 – p 1 · v 1 . Следует обратить внимание на то, что энтальпия выражается в кДж/кг, а произведение p 1 · v 1 . даёт дж/кг, если давление перевести в Па=н/м2 из Мпа= 106 Па, а удельный объём брать в м3/кг. Полученные значения p 1 · v 1 . следует поделить на 103, для перевода дж в кДж. Вторая точка на диаграмме, характеризующая окончание адиабатного процесса, находится на пересечении адиабаты (изоэнтропы) s 1 = s 2 и изобары P 2. Находим конечное значение температуры, удельного объёма, внутренней энергии (как и для первой точки): i 2; v 2; Т2; u 2 = i 2 – p 2 · v 2. Внимание: для нахождения температуры точек влажного пара необходимо по изобаре, проходящей через эту точку(или ближайшей изобаре) подняться до кривой х=1 и найти ближайшую изотерм у, отходящую от точки пересечения данной изобары и кривой х=1. Дело в том, что во влажном паре изотермы и изобары совпадают, а на диаграмме показывают изобару и не показывают изотерму.
В адиабатном процессе теплота не отводится и не подводится к рабочему телу (пару), т. е. q = 0 и удельная механическая работа (изменения объём а), согласно первому началу термодинамики в форме): q = Δ u + l; l = q – Δ u = 0 – Δ u = - Δ u = - (u 2 – u 1) = u 1 – u 2. У дельная техническая работа (работа изменения давления) определяется по первому началу в виде: q = (i 1 – i 2) + l *; отсюда для . q= 0 . l * = i 1 – i 2. u1 = i1 = s 1 = n 1 =
u2= i2 = s 2 = n 2 =
l = - Δ u = - (u2 – u1) = u1 – u2 =
l * = i 1 – i 2 = Задание 3. Провести расчёт термических к.п.д и мощности паровой турбины, используя i – s диаграмму. Условия задания: паровая турбина расходует M = 50 кг/с пара. Значения давления пара и его температуры на входе в турбину и выходе из неё в конденсатор примем равными Р1 = 10 МПа, Т1= 5500С, Р2= 0,005 МПа. Процесс расширения пара в турбине считать адиабатным. Это означает, что s 1 = s 2. Расчёты проводятся по формулам (6-10) и (6-11). Выполнение задания. Как и в предыдущем случае, находим точку на диаграмме, характеризующую начальное состояние пара. Она находится на пересечении изобары Р1 = 10 МПа и изотермы Т1= 5500С. Опуская из неё перпендикуляры на оси энтальпии и энтропии, находим значения i 1 и s 1 = s 2. Вторая точка, характеризующая конечное состояние пара, лежит на пересечении изобары Р2= 0,005 МПа и изоэнтропы (адиабаты) s 2 = s 1. Опуская из неё перпендикуляр на ось энтальпии, находим значение i 2.
Рассчитываем мощност ь турбины по формуле (12) и термический к.п.д. по формуле (13). Значение удельной энтальпии воды i 3, полученной при конденсации пара, находим из таблиц.
i1 = s 1 = i2 = i3 = i2’ =
N т = (i1 – i2)· М = ηt = (i 1 – i 2)/(i 1 – i 2 ’) =
При отчёте необходимо представить расчёты одного из термодинамических процессов, выполненные самостоятельно. Номер задания получить у преподавателя. Контрольные вопросы. 1. Из каких термодинамических процессов состоит цикл Ренкина для идеальной паровой турбины? 2. Какие параметры и функции состояния можно определить с помощью диаграммы i – s, если известно положение на диаграмме точки, характеризующей состояние пара? 3. Какие параметры и функции состояния пара надо знать, чтобы определить к.п.д. идеальной паровой турбины? 4. Какие параметры и функции состояния пара надо знать, чтобы определить мощность. идеальной паровой турбины? 5. Каким образом с помощью диаграммы i – s можно определить работу, совершаемую паром (или над ним), если заданы параметры двух точек на диаграмме? Контрольные задания по работе. Задание l Пар из состояния 1 (Р1 =0,05 МПа, Т1 = 650 0С) переходит в состояние 2 (Р2 =0,05 МПа, Т2 = 300 0С), совершая термодинамический процесс (определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 2 Пар из состояния 1 (v1 = 5,0 м3 / кг, Т1 = 700 0С) переходит в состояние 2 (v2 = 5,0 м3 /кг, Т2= 2000С), совершая термодинамический (определить, какой?) процесс. Используя диаграммму i-s, найти неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание З Пар из состояния 1 (v1 = 5,0 м3 / кг, Т1 = 400 0С) переходит в состояние 2 (v2 =0,5 м3 / кг, Т2 = 400 0С), совершая термодинамический (определить, какой?) процесс. Используя диаграмму i-s, найти неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 4. Пар из состояния 1 (Р1 =0,5 МПа, S1 = 8,5 кдж/кг град) переходит в состояние 2 (Р2 =0,05 МПа, S2 = 8,5 кдж/кг град), совершая термодинамический (определить, какой?) процесс. Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, температуру, энтальпию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 5 Пар из состояния 1 (Р1 = 1,0 МПа, Т1 = 600 0С) переходит в состояние 2 (Р2 =1,0 МПа, Т2 = 300 0С), совершая термодинамическцй (определить, какой?) процесс. Используя диаграмму i-s, найти неизвестные параметры и функции состояния. (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 6 Пар из состояния 1 (v1 = 1,0 м3 / кг, Т1 = 600 0С) переходит в состояние 2 (v2 = 1,0 м3 / кг, Т2= 3000С), совершая термодинамический (определить, какой?)процесс. Используя диаграмму i-s, найти. неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 7 Пар из состояния 1 (Р1 =2,0 МПа, Т1 = 700 0С) переходит в состояние 2 (Р2 =0,1 МПа, Т2 = 700 0С), совершая термодинамический (определить, какой?) процесс. Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 8. Пар из состояния 1 (Р1 =1,0 МПа, S1 = 8,0 кдж/кг град) переходит в состояние 2 (Р2 =0,1 МПа, S2 = 8,0 кдж/кг град), совершая термодинамический (определить, какой?) процесс. Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, температуру, энтальпию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 9 Пар из состояния 1 (Р1 =2,0 МПа, Т1 = 500 0С) переходит в состояние 2 (Р2 =2,0 МПа, Т2 = 400 0С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 10 Пар из состояния 1 (v1 = 2,0 м3 / кг, Т1 = 500 0С) переходит в состояние 2 (v2 = 2,0 м3 / кг, Т2= 2000С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти. неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 11 Пар из состояния 1 (v1 = 10,0 м3 /кг, Т1 = 400 0С) переходит в состояние 2 (v2 = 1,0 м3 / кг, Т2= 4000С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти. неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 12. Пар из состояния 1 (Р1 =10,0 МПа, S1 = 7,0 кдж/кг град) переходит в состояние 2 (Р2 =1,0 МПа, S2 = 7,0 кдж/кг град), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, температуру, энтальпию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса Задание 13 Пар из состояния 1 (Р1 =1,0 МПа, Т1 = 600 0С) переходит в состояние 2 (Р2 =1,0 МПа, Т2 = 300 0С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 14 Пар из состояния 1 (v1 = 1,0 м3 / кг, Т1 = 600 0С) переходит в состояние 2 (v2 = 1,0 м3 / кг, Т2= 3000С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти. неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 15 Пар из состояния 1 (Р1 = 2,0 МПа, Т1 = 700 0С) переходит в состояние 2 (Р2 =0,1 МПа, Т2 = 700 0С), совершая термодинамический процесс (определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 16. Пар из состояния 1 (Р1 =1,0 МПа, S1 = 8,0 кдж/кг град) переходит в состояние 2 (Р2 =0,1 МПа, S2 = 8,0 кдж/кг град), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти неизвестные параметры и функции состояния (объём, температуру, энтальпию, нутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса. Задание 17 Пар из состояния 1 (v1 = 0,5 м3 / кг, Т1 = 600 0С) переходит в состояние 2 (v2 = 0,5 м3 / кг, Т2= 4000С), совершая термодинамический процесс(определить, какой?). Используя диаграмму i-s, найти. неизвестные параметры и функции состояния (давление, энтальпию, энтропию, внутреннюю энергию) для первого и второго состояний, а также теплоту и работу процесса.
|
|||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 89; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.39.32 (0.036 с.) |
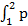 · dV. (2) Удельная работа l = L / m =
· dV. (2) Удельная работа l = L / m = 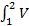 dP. l * = -
dP. l * = - 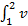 dP (6-5) По определению энтальпии I = U + P · V. (6-6) Удельная энтальпии i = u + p · v (6-7). Первое начало термодинамики с учётом ф-л (6-5) - (6-7) можно записать в виде: Q = ∆ I + L *; (6-8) q = ∆ i + l * (6-9).
dP (6-5) По определению энтальпии I = U + P · V. (6-6) Удельная энтальпии i = u + p · v (6-7). Первое начало термодинамики с учётом ф-л (6-5) - (6-7) можно записать в виде: Q = ∆ I + L *; (6-8) q = ∆ i + l * (6-9).


