Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Переаминирование(трансаминирование)Содержание книги
Поиск на нашем сайте
Это обратимый перенос аминогруппы из мол-лы одного орг. соед. в мол-лу другого. Наиб.роль переаминирование играет в биохимии в процессах метаболизмаазотистых оснований в тканях животных и растений.
В жив орг-мах на р-циях такого типа основ-тся синтез и диссимиляцияАМК. Аминотрансферазы содержат в качестве кофсрмента производные вит-а В6-пири-доксаль-5'-фосфат (ф-ла I) и пиридоксамин-5'-фосфат (II). В основе каталитич. активности пиридоксаль-5'-фосфата лежит способность его формильной группы образовывать с АМКамишиффовы основания, легко гидролизующиеся до пиридоксамин-5'-фосфата и -кеток-ты. Нарушение нормального течения переаминирования в орг-ме наблюдается при патологич. состояниях, напр. при инфаркте миокарда, заболеваниях печени. Переаминирование в орг-ме подавляется противотуберкулезными лек.ср-вами (изониазидом, циклосерином и др.), а также при В6-авит-озе.Общая схема переаминирования:
Переаминирование АМК может происходить и вне клетки в присут. пиридоксаль-5'-фосфата, однако скорость р-ции в 106 раз меньше. К переаминированию относят также превращ. -кеток-ты в -амино-к-ту при нагр. с др. АМКой в водном р-ре (р-ция Хербста - Энгеля):
40) Биоти́н (витамин Н, витамин B7, кофермент R) — водорастворимый витамин группы В. Молекула биотина состоит из тетрагидроимидазольного и тетрагидротиофенового кольца, в тетрагидротиофеновом кольце один из атомов водорода замещен на валериановую кислоту. Биотин является кофактором в метаболизме жирных кислот, лейцина и в процессе глюконеогенеза. Входит в состав ферментов, регулирующих белковый и жировой обмен, обладает высокой активностью. Участвует в синтезе глюкокиназы — фермента, регулирующего обмен сахаров. Является коферментом различных ферментов, в том числе и транскарбоксилаз. Участвует в синтезе пуриновых нуклеотидов. Является источником серы, которая принимает участие в синтезе коллагена. С участием биотина протекают реакции активирования и переноса СО2. Авитаминозы Причины
Проявления
При недостатке биотина наблюдаются:
Биотин в живом организме концентрируется в печени, почках.
41) Аскорби́новая кислота́ — органическое соединение, родственное глюкозе, является одним из основных веществ в человеческом рационе, которое необходимо для нормального функционирования соединительной и костной ткани. Выполняет биологические функции восстановителя и кофермента некоторых метаболических процессов, является антиоксидантом. Биологически активен только один из изомеров — L- аскорбиновая кислота, который называют витамином C. В природе аскорбиновая кислота содержится во многих фруктах и овощах. По физическим свойствам аскорбиновая кислота представляет собой белый кристаллический порошок кислого вкуса. Легко растворим в воде, растворим в спирте. Из-за наличия двух асимметрических атомов существуют четыре диастереомера аскорбиновой кислоты. Две условно именуемые L- и D- формы хиральны относительно атома углерода в фурановом кольце, а изо- форма является D- изомером по атому углерода в боковой этиловой цепи. L- изоаскорбиновая, или эриторбовая, кислота используется в качестве пищевой добавки E315. Синтетически получают из глюкозы. Синтезируется растениями из различных гексоз (глюкозы, галактозы)] и большинством животных (из галактозы), за исключением приматов и некоторых других животных (например, морских свинок), которые получают её с пищей.
Биологическая роль Образование коллагена, серотонина из триптофана, образование катехоламинов, синтез кортикостероидов. Аскорбиновая кислота также участвует в превращении холестерина в желчные кислоты. Витамин С необходим для детоксикации в гепатоцитах при участии цитохрома P450. Витамин С сам нейтрализует супероксид-анион радикал до перекиси водорода. Восстанавливает убихинон и витамин Е. Стимулирует синтез интерферона, следовательно, участвует в иммуномодулировании. Переводит трёхвалентное железо в двухвалентное, тем самым способствует его всасыванию. Тормозит гликозилирование гемоглобина, тормозит превращение глюкозы в сорбит.
42) Коферменты ФМН и ФАД Флавиновые коферменты ФМН и ФАД найдены в дегидрогеназах, оксидазах и монооксигеназах. Обычно оба соединения ковалентно связаны с ферментами. Активной группой обоих коферментов является флавин, имеющий сопряженную систему из трех колец, которая может при восстановлении принимать два электрона и два протона. В ФМН к флавину присоединен фосфорилированный полиол рибит. ФАД состоит из ФМН, связанного с АМФ. Восстановление флавиновых коф-тов осуществляется через ряд промежут. стадий, включающих обр-ние радикалов.
43) Важнейшие коферменты НАД и НАДФ. Никотинамидные коферменты - коферментная форма витамина ниацина. К этой группе коферментов, универсальных по распространению и биол. роли, относятся НАД и НАДФ, а также восстановленные (по пиридиновому кольцу) формы этих соед. (соотв. НАДН и НАДФН); наиб.важная биохим. функция этих коферментов - их участие в переносе электронов и водорода от окисляющихся субстратов к кислороду в клеточном дыхании. При участии НАД или НАДФ, связанных прочно или легко диссоциирующих, ферменты дегидрогеназы катализируют обратимое превращ. спиртов, гидроксикислот и нек-рых аминокислот в соответствующие альдегиды, кетоны или кетокислоты.
44) коА КоА, кофермент ацетилирования (или ацилирования), важнейший из коферментов, принимающий участие в реакциях переноса ацильных групп. С КоА связан обширный круг биохимических реакций, лежащих в основе окисления и синтеза жирных кислот, биосинтеза липидов, окислительных превращений продуктов распада углеводов и т. д. Во всех случаях КоА действует как промежуточное соединение, связывающее (акцептирующее) и переносящее кислотные остатки на др. вещества. При этом кислотные остатки либо подвергаются в составе соединения с КоА тем или иным превращениям, либо передаются без изменений на определённые метаболиты. «Активную» форму органических кислот представляют ацильные остатки, присоединённые к сульфгидрильной (SH) группе КоА макроэргической ацилтиоэфирной связью. Пантотеноваяк-та в виде КоА участвует в УГном и жировом обмене, в синтезе ацетилхолина, в коре надпочечников стимулирует обр-ние кортикостероидов.
Карбоксилазныереакции: CH3–CO–S-KoA + CO2 + АТФ<=> HOOC–CH2–CO–KoA + АДФ метилмалонил-оксалоацетат-транскарбоксилазная реакция, катализ.обратимое превраще-ние пировиноградной и щавелевоуксусной кислот:
Метилмалонил-КоА Пируват Пропионил-КоА Оксалоацетат В организме человека изуказанных процессов открыта только реакция изомеризации метилмалонил-КоА в сукцинил-КоА.
L-метилмалонил-КоА Сукцинил-КоА
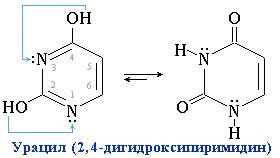
45) Азо́тистые основа́ния — гетероциклические органические соединения, производные пиримидина и пурина, входящие в состав нуклеиновых кислот. Для сокращенного обозначения пользуются большими латинскими буквами. К азотистым основаниям относят аденин (A), гуанин (G), цитозин (C), которые входят в состав как ДНК, так и РНК. Тимин (T) входит в состав только ДНК, а урацил (U) встречается только в РНК. Пиримидиновые основания – производные пиримидина, входящие в состав нуклеиновых кислот: урацил, тимин, цитозин. Для оснований, содержащих группу –ОН, характерно подвижное равновесие структурных изомеров, обусловленное переносом протона от кислорода к азоту и наоборот:
Подобное динамическое равновесие структурных изомеров называют "таутомерией". Пиримидиновые основания входят в состав нуклеозидов — структурных компонентов нуклеиновых кислот. Нуклеозиды образуются за счет отщепления водорода от N–H-связи в молекуле азотистого основания и гидроксила при С1 в молекуле углевода рибозы (или 2-дезоксирибозы).Здесь проявляются нуклеофильные свойства амина (группа:N–H в азотистом гетероцикле) и способность к нуклеофильному замещению полуацетальногогидрокисила (при С1) в молекуле углевода.
46,47) Мажорные-минорные осн, пуриновые-пиримидиновые НК (ДНК и РНК) относятся к сложным высокомол соед, сост из небольшого числа индивид хим компонентов более простого строения. Так, при полном гидролизе НК (нагревание в присутствии хлорной кислоты) в гидролизате обнаруживают пуриновые и пиримидиновые основания, углеводы (рибоза и дезоксирибоза) и фосфорную кислоту. В мол-леДНКуглевод представлен дезоксирибозой, а в молекулеРНК – рибозой, отсюда их названия: дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) кислоты. Кроме того, они содержат фосфорную кислоту, по два пуриновых и по два пиримидиновых основания; различия только в пиримидиновых основаниях: в ДНК содержится тимин, а в РНК – урацил. В составе ДНК и РНК открыты так называемые минорные (экзотические) азотистые основания.Углеводы (рибоза и дезоксирибоза) в молекулахДНК и РНК находятся в β-D-рибофуранозной форме:
Основу стр-ры пуриновых и пиримидиновых оснований составляют два ароматических гетероциклических соединения – пиримидин и пурин:
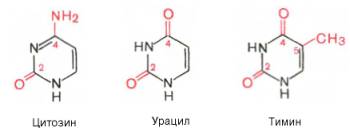
Мол-лапуринасост из 2 конденсированных колец: пиримидина и имидазола. В составе нуклеиновых кислот встречаются три главных пиримидиновых основания: цитозин, урацил и тимин.
Помимо главных пиримидиновых оснований, в составе нуклеиновых кислот открыты минорные пиримидиновые основания, 5-метил- и 5-окси-метилцитозин, дигидроурацил, псевдоурацил, 1-метилурацил, оротовая кислота, 5-карбоксиурацил, 4-тиоурацил и др. только для тРНК список минорных оснований приближается к 50. На долю минорных оснований приходится до 10% всех нуклеотидовтРНК, что имеет, очевидно, важный физиологический смысл (защита молекулыРНК от действия гидролитических ферментов). Стр-рные формулы ряда минорных пиримидиновых оснований представлены в форме нуклеозидов – соединений с углеводным компонентом:
Два пуриновых основания, постоянно встречающихся в гидролизатах нуклеиновых кислот, имеют следующее строение:
К минорным нуклеозидам пуринового ряда, обнаруживаемым в составе ДНК и РНК, относятся инозин, N6-метиладенозин, N2-метилгуанозин, ксантин, гипоксантин, 7-метилгуанозин и др.
48) Таутомерные превращения азотистых оснований Одним из важных св-в свободных АО (содержащих оксигруппы) явл возм-сть их сущ-ния в 2 таутомерных формах, явление таутомерии заключается в том, что вещество определенного состава и молекулярного веса существует в виде равновесной смеси двух или нескольких изомеров, легко переходящих друг в друга, в частности лактим- и лактамной формах, в завис от знач рН среды: при рН 7,0 они представл в лактамной форме, при снижении велич рН – в лактимной форме. Таутомерные превращения можно представить на примере урацила.
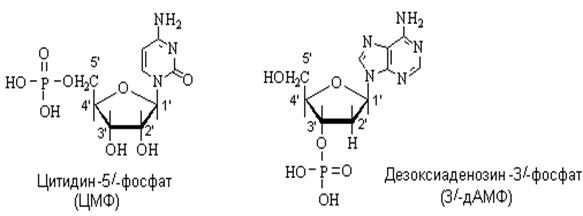
49, 50) Нуклеоти́ды —фосфорные эфиры нуклеозидов, нуклеозидфосфаты. Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ, служат в клетках переносчиками энергии, а также являются составляющими частями нуклеиновых кислот и многих коферментов (органические соединения небелковой природы – компонент некоторых ферментов) и других биологически активных веществ.Молекула каждого нуклеотида (мононуклеотида) состоит из трёх химически различных частей. Во-первых, это пятиуглеродный сахар (пентоза) – рибоза (в этом случае нуклеотиды называются рибонуклеотидами и входят в состав рибонуклеиновых кислот, или РНК) или дезоксирибоза (нуклеотиды называются дезоксирибонуклеотидами и входят в состав дезоксирибонуклеиновых кислот, или ДНК). Во-вторых, это пуриновое или пиримидиновое азотистое основание. Связанное с углеродным атомом сахара, оно образует соединение, называемое нуклеозидом. И наконец, один, два или три остатка фосфорной кислоты, присоединённые эфирными связями к углероду сахара, образуют молекулу нуклеотида. Азотистые основания нуклеотидов ДНК – это пурины аденин и гуанин и пиримидины цитозин и тимин. Нуклеотиды РНК содержат те же основания, что и ДНК, но тимин в них заменён близким по химическому строению урацилом. Азотистые основания и, соответственно, включающие их нуклеотиды в биологической литературе принято обозначать начальными буквами (латинскими или русскими) их названий: аденин – А(А), гуанин – G(Г), цитозин – С(Ц), тимин – Т(Т), урацил – U(У). Соединение двух нуклеотидов называется динуклеотидом, нескольких – олинонуклеотидом, множества – полинуклеотидом, или нуклеиновой кислотой. Кроме того что нуклеотиды образуют цепи ДНК и РНК, они являются коферментами, а нуклеотиды, несущие три остатка фосфорной кислоты (нуклеозидтрифосфаты), – источниками химической энергии, заключённой в фосфатных связях. Чрезвычайно велика во всех процессах жизнедеятельности роль такого универсального переносчика энергии, как аденозинтрифосат (АТФ). Особую группу составляют циклические нуклеотиды, опосредующие действие гормонов при регуляции обмена веществ в клетках.В водных растворах нуклеотиды подвергаются таутомерии. Основная таутомерная форма азотистых оснований – лакт а мная форма.
Нуклеозиды и нуклеотиды Нуклеозиды – это N-гликозиды, образованные нуклеиновыми основаниями и рибозой или дезоксирибозой. Между аномерным атомом углерода моносахарида и атомом азота в положении 1 пиримидинового цикла или атомом азота в положении 9 пуринового цикла образуется b -гликозидная связь.
В зависимости от природы моносахаридного остатка нуклеозиды делят на рибонуклеозиды (содержат остаток рибозы) и дезоксирибонуклеозиды (содержат остаток дезоксирибозы). Названия нуклеозидов строят на основе тривиальных названий нуклеиновых оснований, добавляя окончание –идин для производных пиримидина и -озин для производных пурина. К названиям дезоксирибонуклеозидов добавляют приставку дезокси-. Исключение составляет нуклеозид, образованный тимином и дезоксирибозой, к которому приставка дезокси- не добавляется, так как тимин образует нуклеозиды с рибозой лишь в очень редких случаях.
Для обозначения нуклеозидов используются однобуквенные обозначения, входящих в их состав нуклеиновых оснований. К обозначениям дезоксирибонуклеозидов (за исключением тимидина) добавляется буква ”д”. Наряду с представленными на схеме основными нуклеозидами в составе нуклеиновых кислот встречаются минорные нуклеозиды, содержащие модифицированные нуклеиновые основания.В природе нуклеозиды встречаются также в свободном состоянии, преимущественно в виде нуклеозидных антибиотиков, которые проявляют противоопухолевую активность. Нуклеозиды-антибиотики имеют некоторые отличия от обычных нуклеозидов в строении либо углеводной части, либо гетероциклического основания, что позволяет им выступать в качестве антиметаболитов, чем и объясняется их антибиотическая активность. нуклеозиды устойчивы к действию щелочей, но расщепляются под действием кислот с образованием свободного моносахарида и нуклеинового основания. Пуриновые нуклеозиды гидролизуются значительно легче пиримидиновых. Нуклеотиды. Нуклеотиды – это эфиры нуклеозидов и фосфорной кислоты (нуклеозидфосфаты). Сложноэфирную связь с фосфорной кислотой образует ОН группа в положении 5/ или 3/ моносахарида. В зависимости от природы моносахаридного остатка нуклеотиды делят на рибонуклеотиды (структурные элементы РНК) и дезоксирибонуклеотиды (структурные элементы ДНК). Названия нуклеотидов включают название нуклеозида с указанием положения в нем остатка фосфорной кислоты. Сокращенные обзначения нуклеозидов содержат обозначение нуклеозида, остатка моно-, ди- или трифосфорной кислоты, для 3/-производных указывается также положение фосфатной группы.
Нуклеотиды являются мономерными звеньями, из которых построены полимерные цепи нуклеиновых кислот. Некоторые нуклеотиды выполняют роль коферментов и участвуют в обмене веществ.
51) Циклические аденозинмонофосфаты,стр-ра функции Циклический аденозинмонофосфат (циклический AMФ, цAMФ, cAMP) — производное АТФ, выполняющее в организме роль вторичного посредника, использующегося для внутриклеточного распространения сигналов некоторых гормонов (например, глюкагона или адреналина), которые не могут проходить через клеточную мембрану; бусцветные крист.
Образуется из АТФ под действием фермента аденилциклазы: фосфатная группа соединена с атомами углерода в 3’- и 5’-положениях рибозы.цAMФ синтезируется аденилатциклазой в ответ на некоторые гормональные стимуляторы; действует как вторичный посредник при клеточном гормональном контроле путем стимуляции протеинкиназ; является аллостерическим эффектором протеинкиназ A и ионных каналов. Синтезируется мембранными аденилатциклазами. Расщепление цАМФ с образованием АМФ катализируется фосфодиэстеразами. Ингибируются цАМФ только при высоких концентрациях метилированных производных ксантина. цAMФ осуществляет функции вторичного внутриклеточного посредника в действии первичных посредников (веществ, имеющих короткий период биодеградации) — например, ряда гормонов и нейромедиаторов; опосредует биологическую функцию гормонов путем активации (инактивации) клеточных протеинкиназ (фосфатаз). Протеинкиназы, в свою очередь, фосфорилируют эффекторные белки и изменяют (увеличивают или уменьшают) их активность.
52). отличия и сходста ДНК и РНК ДНК – это полинуклеотиды, полианионы, неразветвленные и нерегулярные, исключит крупные биополимеры. Сущ-ют линейные и замкнутые (кольцевые), одно- и двухцепоч полинуклеотиды. По особенностям хим строения НК делят на ДНК и РНК. Есть несколько типов ДНК: хромосомная (ядерная, нуклеоидная) и внехромосомная (митохондриальная, хлоропластная ДНК, плазмидная ДНК и др.). Все НК роднит принцип сходство стр. В природных олиго- и полинуклеотидах мономеры (нуклеотиды) связаны 3’,5’-фосфодиэфирными связями. При глубоком гидролизе разрушаются не только фосфодиэфирные, но и гликозидные связи, и нуклеиновые кислоты распадаются до азотистых оснований, моносахаридов и фосфорной кислоты. Как известно, в число канонических (основных) азотистых осн в сост ДНК преимущ входят А, Г, Ц т Т, а в сост РНК - А, Г, Ц и У. Реже встречающиеся (минорные) пуриновые и пиримидиновые азотистые основания явлются продуктами О-, С- или N-алкилирования канонических азотистых оснований. В тРНК минорные основания могут составлять до 19 %, а в ДНК проростков злаковых, в молоках рыб – до 8-10 %. У эукариотов ДНК в основном локализована в ядре, а также в митох и хлоропл, где сост несколько процентов от общего кол-ва клет ДНК. У прокариотов ДНК представлена в виде нуклеоида (бактер хромосома), а также в виде внехром-ной плазмидной ДНК. Только хром-ная ДНК эукариот способна обр-вать нуклеопротеины, динамичные комплексы со специфич ДНК-связывающими белками, и формирует видоспецифическую структуру хромосом. У вирусов ДНК весьма плотно упакована в комплексе с белками. РНК гетерогенна и предст в виде: мРНК – 3-5 %; тРНК – около 10 %; рРНК – около 85 % от общего кол-ва РНК в кл. Молекулы РНК менее крупные, чем ДНК, и всегда одноцепочечные. Все виды РНК представляют собой продукты транскрипции ДНК. У эукариотов РНК локализована в ядре, митох, хлоропластах и цитоплазме. Абсолютное содержание ДНК и РНК, а также их соотношение сильно варьирует в клетках разных видов и в разных клетках одного вида. Следует заметить, что во внеклеточной среде обнаруживаются только следовые количества нуклеиновых кислот, по-видимому, в силу быстрого ферментативного гидролиза активными нуклеазами. Доля ДНК в метаболически активной клетке значительно меньше, чем в метаболически неактивной: например, в сперматозоидах ДНК составляет около 60 % сухого вещества, а в мышцах лишь 0,2%. С другой стороны величина отношения содержания РНК к содержанию ДНК в клетке тем выше, чем выше ее метаболическая активность. Сложность и размеры ДНК увеличиваются с усложнением организации живых организмов, параллельно с усложнением организации, увеличивается доля некодирующей ДНК (многократные повторы, интроны, регуляторные участки). 53) Первичная структура нуклеиновых кислот Под первичной структурой нуклеиновых кислот понимают порядок, последовательность расположения мононуклеотидов в полинуклеотидной цепи ДНК и РНК. Такая цепь стабилизируется 3',5'-фосфодиэфирными связями. Поскольку молекулярная массануклеиновых кислот колеблется в широких пределах (от 2•104 до 1010–1011), установить первичную структуру всех известных РНК и особенно ДНК весьма сложно. Тем не менее во всех нуклеиновых кислотах (точнее, в одноцепочечной нуклеиновой кислоте) имеется один и тот же тип связи – 3',5'-фосфодиэфирная связь между соседними нуклеотидами. Эту общую основу структуры можно представить следующим образом:
Установлено, что в образовании межнуклеотидной связи участвуют гидроксильные группы в 3'- и 5'-положениях остатков углевода. К настоящему времени удалось определить первичную структуру почти всех тРНК, ряда молекул 5S рРНК, 16S рРНК E.coli, вирусных РНК, в состав которых входят сотни и тысячи нуклеотидных остатков. Полинуклеотидная цепь молекулыРНК имеет на одном конце почти всегда свободный монофосфорный эфир, который принято обозначать как 5'-конец; на противоположном конце цепи такой фосфат отсутствует, а содержится нуклеотид со свободными 2'- и 3'-гидроксильными группами. Если подвергнуть щелочному гидролизумолекулуРНК, то в качестве концевого нуклеотида будут обнаружены ЦМФ со свободным фосфатом у 5'-конца и свободныйаденозин в виде свободного нуклеозида у 3'-конца полинуклеотидной цепи. В выяснении первичной структуры РНК решающую роль сыграли методы ступенчатого гидролиза, осуществленного в основном экзонуклеа-зами и заключающегося в последовательном отщеплении по одному мононуклеотиду с одного конца молекулынуклеиновой кислоты. Следует особо указать на две существенные особенности первичной структуры всех тРНК. Первая из них заключается в том, что 5'-концом всегда является гуаниловая (редко цитидиловая) кислота, несущая свободный остаток фосфата у С-5'. Вторая особенность – наличие на противоположном конце молекулы остатков трех мононуклеотидов с одинаковой последовательностью – ЦЦА, причем остаток адениловой кислоты содержит свободную 3'-ОН-группу. Между этими структурами в строго определенной последовательности располагаются все остальные нуклеотидные остатки, среди которых на долю минорных нуклеотидов приходится до 10%. Полинуклеотидная цепь разных типов тРНК содержит около 75 нуклеотидов. Матричные (информационные) РНК относятся к наиболее гетерогенному классу нуклеиновых кислот, отличающихся по массе, структуре, размерам, стабильности и функциям. Основной функцией мРНК является перенос информации от ДНК (точнее, от гена) на белоксинте-зирующую систему клетки. мРНК выполняет роль матрицы и, следовательно, определяет первичную структуру синтезируемого белка. мРНК наделены рядом особенностей первичной структуры; в частности, на 5'-конце все они содержат определенную последовательность рибонуклеотидов, получившую название шапочки (кэп). Роль «кэпирования» и «полиаденилирования» мРНК в белковом синтезе окончательно не выяснена. Предполагают, что кэп необходим для специфического узнавания в процессе трансляции, в то время как поли-А отводится роль фактора стабилизации всей молекулымРНК. В настоящее время проводятся исследования первичных структур различных молекулДНК. Около 15 лет назад была полностью расшифрована нуклеотидная последовательность митохондриальной ДНК человека (16569 пар нуклеотидов). Известны полные нуклеотидные последовательностиДНК ряда вирусов и плазмид. Исследователи активно работают над полной расшифровкой генома человека. Результаты секвенирования (определение нуклеотидной последовательности) разных молекулДНК накапливаются в виде компьютерных банков данных. Ниже представлены три варианта схемы нуклеотидной последовательностиДНК:
В последнее время о первичной структуре ДНК (точнее, отдельных ее фрагментов) судят по ряду косвенных данных, например, по степени сплоченности нуклеотидных звеньев в молекулеДНК (определение сводится в конечном счете к выяснению числа и структуры отдельных фракций нуклеотидов, так называемых изоплитов), также по кинетикереассоциации ДНК (метод позволяет выяснить наличие в молекуле повторяющихся последовательностей нуклеотидов). О первичной структуре ДНК судят, кроме того, по распределению минорных оснований (имеются данные о существовании подобной закономерности) и обнаружению в ДНК и определению последовательности палиндромов («обратно бегущие» последовательности, или перевертыши), которые обнаруживаются главным образом в местах рестрикции. Большие надежды в определении первичной структуры ДНК исследователи возлагают на физические, химические (синтез генов), генетические и другие методы, а также на методы выделения некоторых генов (или их фрагментов) из природных источников и синтеза генов на мРНК при участии ферментаобратной транскриптазы. Для установления первичной структуры ДНК недавно предложен экспресс-метод, включающий применение двух ДНК-полимераз.
54) Под вторичной структурой нуклеиновых кислот понимают пространственно упорядоченные формы полинуклеотидных цепей. Вторичная структура ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг общей оси в двойную спираль. Такая пространственная структура удерживается множеством водородных связей, образуемых азотистыми основаниями, направленными внутрь спирали. Водородные связи возникают между пуриновым основанием одной цепи и пиримидиновым основанием другой цепи. Эти основания составляют комплементарные пары. · ТИМИН (Т) комплементарен АДЕНИНУ (А), · ЦИТОЗИН (Ц) комплементарен ГУАНИНУ (Г). Комплементарность оснований определяет комплементарность цепей в молекулах ДНК. Она характер. Следующими свойствами: · хранения и передачи наследственных признаков. · молекулы ДНК способны к репликации (удвоению) · молекулы ДНК могут направлять совершенно точным и определенным образом синтез белков, специфичных для организмов данного вида.
55) Пра́вила Ча́ргаффа — система эмпирически выявленных правил, описывающих количественные соотношения между различными типами азотистых оснований в ДНК. Были сформулированы в результате работы группы биохимика Эрвина Чаргаффа в 1949—1951 гг. До работ группы Чаргаффа господствовала так называемая «тетрануклеотидная» теория, согласно которой ДНК состоит из повторяющихся белков по четыре разных азотистых основания (аденин, тимин, гуанин и цитозин). Чаргаффу и сотрудникам удалось разделить нуклеотиды ДНК при помощи бумажной хроматографии и определить точные количественные соотношения нуклеотидов разных типов. Они значительно отличались от эквимолярных, которых можно было бы ожидать, если бы все четыре основания были представлены в равных пропорциях. Соотношения, выявленные Чаргаффом для аденина (А), тимина (Т), гуанина (Г) и цитозина (Ц), оказались следующими: 1. Количество аденина равно количеству тимина, а гуанина — цитозину: А=Т, Г=Ц. 2. Количество пуринов равно количеству пиримидинов: А+Г=Т+Ц. 3. Количество оснований с аминогруппами в положении 6 равно количеству оснований с кетогруппами в положении 6: А+Ц=Г+Т. Вместе с тем, соотношение (A+Т):(Г+Ц) может быть различным у ДНК разных видов. У одних преобладают пары АТ, в других — ГЦ. Правила Чаргаффа, наряду с данными рентгеноструктурного анализа, сыграли решающую роль в расшифровке структуры ДНК Дж. Уотсоном и Фрэнсисом Криком. Комплемента́рность (в химии, молекулярной биологии и генетике) — взаимное соответствие молекул биополимеров или их фрагментов, обеспечивающее образование связей между пространственно взаимодополняющими (комплементарными) фрагментами молекул или их структурных фрагментов вследствие супрамолекулярных взаимодействий (образование водородных связей, гидрофобных взаимодействий, электростатических взаимодействий заряженных функциональных групп и т. п.). Взаимодействие комплементарных фрагментов или биополимеров не сопровождается образованием ковалентной химической связи между комплементарными фрагментами, однако из-за пространственного взаимного соответствия комплементарных фрагментов приводит к образованию множества относительно слабых связей (водородных и ван-дер-ваальса) с достаточно большой суммарной энергией, что приводит к образованию устойчивых молекулярных комплексов. Вместе с тем, следует отметить, что механизм каталитичекой активности ферментов определяется комплементарностью фермента и переходного состояния либо промежуточного продукта катализируемой реакции — и в этом случае может происходить обратимое образование химической связи.
56) Каждая молекула ДНК упакована в отдельную хромосому. В диплоидных клетках человека содержится 46 хромосом. Общая длина ДНК всех хромосом клетки составляет 1,74 м, но она упакована в ядре, диаметр которого в миллионы раз меньше. Чтобы расположить ДНК в ядре клетки, должна быть сформирована очень компактная структура. Компактизация и суперспирализация ДНК осуществляются с помощью разнообразных белков, взаимодействующих с определёнными последовательностями в структуре ДНК. Все связывающиеся с ДНК эукариотов белки можно разделить на 2 группы: гисгоновые и негистоновые белки. Комплекс белков с ядерной ДНК клеток называют хроматином. Гистоны - белки с молекулярной массой 11-21 кД, содержащие много остатков аргинина и лизина. Благодаря положительному заряду гистоны образуют ионные связи с отрицательно заряженными фосфатными группами, расположенными на внешней стороне двойной спирали ДНК. Существует 5 типов гистонов. Четыре гистона Н2А, Н2В, НЗ и Н4 образуют октамерный белковый комплекс (Н2А, Н2В, НЗ, Н4)2, который называют "нуклеосомный кор" (от англ. nucleosome core). Молекула ДНК "накручивается" на поверхность гистонового октамера, совершая 1,75 оборота (около 146 пар нуклеоти-дов). Такой комплекс гистоновых белков с ДНК служит основной структурной единицей хроматина, её называют "нуклеосома". ДНК, связывающую нуклеосомные частицы, называют линкерной ДНК. В среднем линкерная ДНК составляет 60 пар нуклеотидных остатков. Молекулы гистона H1 связываются с ДНК в межнуклеосомных участках (линкерных последовательностях) и защищают эти участки от действия нуклеаз (рис. 4-8). В ядре каждой клетки присутствует около 60 млн молекул каждого типа гистонов, а общая масса гистонов примерно равна содержанию ДНК. Аминокислотные остатки лизина, аргинина и концевые аминогруппы гистонов могут модифицироваться: ацетилироваться, фосфорилироваться, метилироваться или взаимодействовать с белком убиквитином (неги-стоновый белок). Модификации бывают обратимыми и необратимыми, они изменяют заряд и конформацию гистонов, а это влияет на взаимодействие гистонов между собой и с ДНК. Активность ферментов, ответственных за модификации, регулируется и зависит от стадии клеточного цикла. Модификации делают возможными конформационные перестройки хроматина.
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-21; просмотров: 397; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.72.245 (0.013 с.) |