
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опд. Ф. 09. 02 пищевые и биологически активныеСодержание книги
Поиск на нашем сайте
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
Кафедра химии
ОПД. Ф. 09.02 ПИЩЕВЫЕ И БИОЛОГИЧЕСКИ АКТИВНЫЕ ДОБАВКИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ к выполнению лабораторных работ
Направление подготовки дипломированного специалиста 260200 Производство продуктов питания из растительного сырья специальности: 260201 Технология хранения и переработки зерна 260202 Технология хлеба, кондитерских и макаронных изделий 260203 Технология бродильного производства и виноделия
260500 Технология продовольственных продуктов специального назначения и общественного питания специальности: 260501 Технология продуктов общественного питания Уфа 2013
УДК 54:6.63:6.64(07) ББК 24:36-1 Г 48
Рекомендовано к изданию методической комиссией факультета пищевых технологий
(протокол № от «____» __________ 2013 г.)
Составитель: Чернышенко Ю.Н.
Ответственный за выпуск: заведующий кафедрой химии Исламова Р.М.
Оглавление
ВВЕДЕНИЕ
Методические указания к лабораторным работам по дисциплине «Пищевые и биологически активные добавки» предназначены для студентов 3 курса факультета пищевых технологий. Каждая лабораторная работа выполняется студентами индивидуально и проводится в течение 4-х часов следующим образом: 1) студент дома самостоятельно знакомится с целью работы, изучает методическое указание и соответствующую учебную литературу, оформляет описательную часть отчета;
2) на занятии студент получает задание у преподавателя и приступает к выполнению работы; 3) после завершения работы студент приводит рабочее место в порядок, делает необходимые расчеты, заканчивает оформление отчета и сдает его преподавателю.
Работа считается выполненной студентом только тогда, когда отчет со всеми результатами и сделанными на основании их выводами принят преподавателем. Предлагаемые методические указания составлены на основе опыта проведения лабораторных занятий на кафедре химии Башкирского государственного аграрного университета. ОБЩИЕ ПРАВИЛА РАБОТЫ В ЛАБОРАТОРИИ И ТЕХНИКА БЕЗОПАСНОСТИ 1. Перед каждой лабораторной работой следует изучить относящийся к ней теоретический материал. Только тогда лабораторные занятия будут полезными и продуктивными. 2. Начинать опыты следует только после внимательного ознакомления с описанием работы и уяснив технику ее выполнения. 3. Не брать реактивы в большем количестве, чем требуется для проведения опыта. 4. Неизрасходованные или взятые в избытке реактивы не рекомендуется сливать обратно в бутыли или другую тару; их необходимо сдавать лаборанту. 5. Не загромождать рабочее место посторонними предметами или реагентами. 6. Не уносить приборы и аппараты, а также реактивы общего пользования на свое рабочее место. Принять за правило: каждый предмет или реактив возвращать на место сразу после его использования. 7. Все работы с вредными веществами проводить только под вытяжным шкафом. Нельзя переносить концентрированные кислоты и щелочи с одного места на другое. 8. Не путать пробки от склянок, а также пипетки для отбора жидких реактивов. 9. Горячие приборы и посуду ставить только на специальные подставки, а не на стол. 10. По окончании работы необходимо вымыть химическую посуду, тщательно убрать рабочее место, отключить воду и электричество. 11. Обязательно вести запись результатов, проведенных лабораторных работ. Пока в тетрадь не занесены результаты предыдущего опыта, не переходить к следующему. 12. При нагревании пробирок и колб с их содержимым во избежание выброса жидкости нельзя направлять их отверстием к себе или в сторону соседа.
13. Если на кожу попала концентрированная кислота, то пораженное место следует тотчас же промыть обильным количеством воды под краном, после чего обработать 5%-ным раствором соды. 14. В случае попадания концентрированной щелочи пораженное место следует промыть водой, затем разбавленным раствором уксусной кислоты. 15. При получении ожогов от прикосновения к горячим предметам надо обожженное место покрыть марлей, пропитанной 2%-ным раствором перманганата калия или 3%-ным раствором танина. 16. При порезах рук стеклом следует в первую очередь удалить из раны осколки стекла, затем смыть кровь 2%-ным раствором перманганата калия или спиртом и, смазав рану йодной настойкой, забинтовать. 17. Испытывать газы на запах нужно осторожно: пробирку следует держать в полувытянутой левой руке так, чтобы отверстие находилось ниже уровня носа, и правой рукой направлять к себе слабый ток воздуха. 18. Огнеопасные вещества, такие, как водород, бензин, эфир, надо держать подальше от источника открытого огня. Лабораторная работа №1 «Определение массовой доли крахмала в колбасных изделиях» Крахмал – полисахарид II порядка, содержится практически во всех пищевых добавках растительного происхождения. Обладая гидрофильностью, он усиливает влагосвязывающую способность мясных фаршей, повышая выход продукта. Ассортимент варёных колбас включает колбасы высшего, 1-ого и 2-ого сортов. Для производства колбас высшего сорта используется высококачественное мясное сырье: говядина жилованная высшего сорта, свинина жилованная нежирная, баранина жилованная односортная, языки свиные и говяжьи и т.д. Внесение в них каких-либо наполнителей типа крахмала или соевых белковых препаратовне предусмотрено. В варёные колбасы 1-го и 2-го сортов и в некоторые низкосортные полукопчёные и ливерные колбасы и сардельки добавляют крахмал или пшеничную муку. Крахмал снижает пищевую ценность колбас, и по этому его количество не должно превышать 2-3%. Мука, крахмал - наполнители. Они устраняют бульонные отеки, придают монолитность и увеличивают выход, могут стать причиной резиноподобной консистенции, "пустого" вкуса. Определение крахмала в колбасных изделиях основано на окислении альдегидных групп моносахаридов, образующихся при гидролизе крахмала в кислой среде, двухвалентной медью реактива Фелинга с образованием осадка закиси меди. При гидролизе крахмала образуются редуцирующие сахара, основную массу которых составляет глюкоза.
(С6Н10О5)n + n H2O ® n(C6H12O6)
Образовавшиеся при гидролизе крахмала редуцирующие сахара, благодаря наличию альдегидных групп, окисляются в щелочной среде реактивом Фелинга - растворимым комплексным соединением меди (II) с сегнетовой солью. При окислении глюкозы Сu (II) восстанавливается до закиси меди Сu2О.
Количество восстановленной меди соответствует разнице содержания окисной меди в холостом опыте и после кипячения с раствором инвертного сахара. Содержание общего и остаточного количества окисной меди определяется йодометрически с индикатором – крахмалом: I2 + 2 Na2S2O3 = 2 NaI + Na2S4O6
Цель работы: определить массовую долю крахмала в различных пищевых добавках и мясных продуктах. Реактивы и оборудование:
1) технические весы; 2) электрическая плитка; 3) водяной или воздушный холодильник; 4) бюретка на 25 мл; 5) мерные колбы на 50, 100, 250 мл; 6) конические колбы на 100 и 250 мл; 7) пипетки на 2, 10 и 25 мл. 8) 10%-ный раствор соляной кислоты; 9) 10%-ный раствор гидроксида натрия; 10) 15%-ный раствор гексацианоферрата (II) калия; 11) 30%-ный раствор сульфата цинка; 12) диэтиловый эфир; 13) раствор Фелинга; 14) 30%-ный раствор иодида калия; 15) 25%-ный раствор серной кислоты; 16) 0,1 М раствор тиосульфата натрия; 17) раствор крахмала; 18) индикатор фенолфталеин.
Порядок выполнения работы Навеску образца продукта массой ~20 г, взвешенную с точностью до 0,01 г, помещают в круглодонную колбу на 250 мл и приливают небольшими порциями 80 мл раствора соляной кислоты при постоянном помешивании стеклянной палочкой. Колбу с содержимым присоединяют к обратному водяному или воздушному холодильнику, ставят на электроплитку, подложив под колбу асбестовую сетку, нагревают до кипения и 15 мин кипятят. Затем колбу охлаждают до комнатной температуры холодной водой и содержимое количественно переносят в мерную колбу на 250 мл и доводят объем жидкости в колбе до метки дистиллированной водой таким образом, чтобы попавший в колбу жир находился над меткой. После перемешивания содержимое колбы фильтруют через бумажный фильтр. Вносят пипеткой 25 мл фильтрата в мерную колбу на 50 мл, добавляют 1 каплю раствора индикатора фенолфталеина и нейтрализуют раствором гидроксида натрия до появления от одной капли щелочи красноватой окраски. Сразу же добавляют в колбу по каплям раствор соляной кислоты до исчезновения красноватой окраски и еще 2-3 капли этой же кислоты для установления слабокислой реакции раствора. Для осветления гидролизата и осаждения белков к раствору в колбе на 50 мл пипеткой добавляют 1,5 мл раствора гексацианоферрата калия (реактив Карреза I) и 1,5 мл раствора сульфата цинка (реактив Карреза II). Содержимое колбы охлаждают до комнатной температуры, доводят объем дистиллированной водой до метки, перемешивают и фильтруют через бумажный фильтр. В две мерные колбы на 100 мл добавляют: в одну - 10 мл прозрачного бесцветного фильтрата, в другую - 10 мл дистиллированной воды (для приготовления контрольного раствора). Затем в каждую колбу добавляют по 20 мл раствора Фелинга, полученного смешиванием (1:1) растворов Фелинга-1 (10 мл) и Фелинга-2 (10 мл). Содержимое обеих колб взбалтывают и кипятят на электроплитке 3 мин, считая с момента закипания. После кипячения колбы охлаждают холодной водой, доводят объемы дистиллированной водой до метки, тщательно перемешивают и дают осесть выпавшему оксиду меди.
В коническую колбу вместимостью 100 мл пипеткой вносят 20 мл отстоявшейся жидкости (каждого раствора по очереди), последовательно добавляют мерным цилиндром сначала 10 мл 30%-ного раствора йодистого калия, затем 10 мл 25%-ного раствора серной кислоты и сразу же титруют выделившийся йод раствором тиосульфата натрия до слабо-желтой окраски. Затем добавляют 1 мл раствора крахмала и продолжают медленно титровать (с промежутком между каплями 5-6 с) до полного исчезновения синей окраски раствора. Затем производят титрование контрольного раствора.
Расчеты: 1) Объем 0,1 М раствора тиосульфата натрия Vx (в мл), пошедшего на титрование образующегося в ходе реакции йода, рассчитывают по формуле:
где К – коэффициент пересчета на точно 0,1 М раствор тиосульфата натрия; Vк, Vи – соответственно, объемы 0,1 М раствора тиосульфата натрия, израсходованного на титрование контрольного и испытуемого растворов, мл; 100 – разбавление гидролизата после кипячения, мл; 20 – объем титруемого раствора, мл. По таблице 1 находят массу крахмала (a, мг), соответствующую массе тиосульфата натрия (Na2S2O3), содержащегося в 1 мл 0,1 М раствора. 2) Рассчитывают массовую долю крахмала w (%) по формуле:
где a - масса крахмала, соответствующая массе тиосульфата натрия, содержащегося в 1 мл 0,1 М раствора (определяют по табл. 1), г; 250 – объем гидролизата, мл; 50 – разведение фильтрата после нейтрализации и осаждения белков, мл; m – масса навески образца, г; 25 – объем фильтрата, взятый для нейтрализации и осаждения белков, мл; 10 – объем гидролизата, взятый для кипячения, мл.
Таблица 1. Взаимосвязь массы крахмала, содержащегося в анализируемом продукте и объема раствора тиосульфата натрия, пошедшего на титрование
Расхождение между результатами параллельных определений не должно превышать 0,2%. За окончательный результат принимают среднее арифметическое результатов трех параллельных определений. Вычисление производят с точностью до 0,1%. После выполнения работы и расчетов студенты делают заключение о соответствии продукта требованиям государственного стандарта по массовой доле крахмала в анализируемом продукте. Примечание. При вычислении содержания крахмала в ливерной яичной колбасе найденный процент умножают на 0,7 (поправочный коэффициент на содержание редуцирующих веществ в продукте). При анализе растительных добавок делают расчет количества добавки в фарше для получения качественной продукции, соответствующей государственному стандарту.
Пример расчетов: на титрование 20 мл контрольного раствора израсходовано 3,21 мл 0,1 М раствора тиосульфата натрия (К = 0,9877), а на титрование 20 мл анализируемого раствора - 2,18 мл:
По таблице 1 находим массу крахмала, соответствующую 5,09 мл 0,1 М раствора тиосульфата натрия:
где 14,2 - масса крахмала, соответствующая 5 мл 0,1 М раствора Na2S2O3, мг; 2,9 - разность значений массы крахмала для 5 и 6 мл раствора Na2S2O3, мг; 0,261 - масса крахмала, соответствующая 0,09 мл 0,1 М раствора Na2S2O3, мг.
Таким образом, массовая доля крахмала в анализируемом продукте равна 3,62%. Контрольные вопросы
1. Какие добавки входят в группу веществ, изменяющих структуру и физико-химические свойства пищевых продуктов? 2. Какие пищевые гидроколлоиды, разрешенные в производстве пищевых продуктов, вам известны? 3. Какие основные виды модификаций крахмалов вы знаете? Как строение модифицированных крахмалов связано с особенностями их свойств? 4. К какому классу добавок относятся каррагинаны? Какие из них являются гелеобразующими? Как это связано с химическим строением. 5. Какой загуститель полисахаридной природы получают микробиологическим путем? Можно ли его использовать при получении пищевых гелей? 6. Из каких источников получают пектины? Каковы области их применения? 7. Что такое эмульгатор? Какова их химическая природа? 8. Каким методом определяют массовую долю крахмала в колбасных изделиях? 9. В каких колбасных изделиях разрешается добавление крахмала и какая массовая доля должна быть? 10. С какой целью добавляется крахмал в колбасные изделия? 11. Какую химическую реакцию проводят для получения из крахмала моносахаридов? Составьте уравнение реакции, назовите продукты реакции. 12. Напишите уравнение реакции окисления альдегидных групп моносахаридов. 13. Изложите методику осветления гидролизата и окисления белков. 14. Составьте уравнение реакции титрования раствором тиосульфата натрия. Лабораторная работа № 2 «Определение нитрита натрия в колбасных изделиях Фотометрическим методом» Нитрит натрия относится к цветокорректирующим материалам, то есть соединениям, изменяющим окраску продукта в результате взаимодействия с компонентами пищевого сырья и готовых продуктов. Для придания копченостям и колбасам характерной для них окраски (от розовой до красной) традиционно используют нитриты калия и натрия (KNO2 и NaNO2) и/или нитраты (селитры) – Е249…Е252. Нитраты под действием ферментов, выделяемых микроорганизмами, восстанавливаются до нитритов. Нитриты оказывают вредное влияние на организм человека. В связи с этим установлены максимально допустимые нормы содержания их в готовом продукте. Норма применения нитрита при посоле мяса в рассоле от 50 до 100 мг/кг, а в готовой продукции- 30…50 мг/кг. Исключить опасности, связанные с применением нитритов, можно заменив их природными и синтетическими пищевыми красителями. Однако нитриты придают мясным изделиям не только приятный цвет, но и способствуют образованию характерных для копченостей и колбас вкуса и аромата, а также тормозят развитие нежелательной микрофлоры при производстве и хранении.
Цель работы: определить содержание нитрита натрия (цветокорректирующей добавки) в колбасных изделиях различных сортов.
Реактивы и оборудование: 1) насыщенный раствор тетрабората натрия; 2) 15-% раствор гексацианоферрата (II) калия (реактив Карреза I); 3) 30-% раствор сульфата цинка (реактив Карреза II); 4) аммонийная буферная смесь; 5) раствор сульфаниламида (фотометрический реагент № 1); 6) раствор N-(1-нафтил)этилендиаминодигидрохлорида (фотометрический реагент № 2); 7) раствор III (разбавляют 445 мл концентрированной соляной кислоты (ρ20 1,19 г/мл) водой до 1000 мл); 8) Мерные колбы на 100 и 200 см3; 9) пипетки; 10) электрическая плитка; 11) фотоэлектроколориметр; 12) водяная баня; Порядок выполнения работы В мерную колбу на 200 мл помещают 10 г анализируемой пробы, взвешивают на аналитических весах, добавляют 5 мл насыщенного раствора Na2B4O7 и 100 мл дистиллированной воды температурой не ниже 75°С. Колбу с содержимым нагревают на кипящей водяной бане в течение 15 мин, периодически встряхивая, затем охлаждают до 20°С, тщательно перемешивают и последовательно добавляют по 2 мл реактива Карреза I и реактива Карреза II. Объем доводят водой до метки и выдерживают 30 мин при 20°С. Затем содержимое колбы фильтруют через складчатый фильтр. К 20 мл полученного безбелкового фильтрата в мерной колбе на 100 мл добавляют 10 мл фотометрического реагента № 1 и добавить 6 мл. раствора Ш. Содержимое колбы перемешивают и выдерживают 5 мин в темном месте. Затем добавляют 2 мл фотометрического реагента № 2, перемешивают и выдерживают в темном месте 3 мин при 20°С. Светопоглощение (А) анализируемого раствора измеряют на фотоэлектроколориметре в кювете с толщиной поглощающего свет слоя 1 см, относительно раствора сравнения при длине волны 538 нм. Раствор сравнения готовят также как и анализируемый, но вместо 20 мл безбелкового фильтрата в колбу добавляют 20 мл дистиллированной воды. По калибровочному графику (рис 1) определяют массу нитрита натрия, содержащегося в 1 мл фильтрата. Построение калибровочного графика. Для приготовления основного раствора нитрита натрия взвешивают навеску реактива, содержащую точно 1г нитрита натрия, растворяют в воде, количественно переносят в мерную колбу вместимостью 500 мл, доводят дистиллированной водой до метки и перемешивают. Для приготовления рабочего раствора 1 мл основного раствора переносят в мерную колбу вместимостью 200 мл, доводят дистиллированной водой до метки и перемешивают. Из полученного рабочего раствора готовят серию стандартных растворов: 5, 10 и 20 мл рабочего раствора пипеткой вносят в три мерные колбы вместимостью 100 мл, доводят дистиллированной водой до метки и перемешивают. Полученные стандартные растворы содержат в 1 мл соответственно 2,5; 5,0 и 10,0 мкг нитрита натрия. Рабочий и стандартные растворы нитрита натрия нестойки, поэтому их готовят непосредственно перед построением калибровочного графика. Для построения калибровочного графика в четыре мерные колбы вместимостью 100 мл пипеткой вносят: в первую колбу для приготовления контрольного раствора 10 мл дистиллированной воды, а в остальные- по 10 мл стандартных растворов, содержащих 2,5; 5,0 и 10,0 мкг нитрита натрия в 1 мл раствора. В каждую колбу добавляют по 50 мл дистиллированной воды, по 10 мл фотометрического реагента № 1 и по 6 мл раствора III для проведения цветной реакции. Растворы в колбах перемешивают и выдерживают в темном месте в течение 5 мин. Добавляют 2 мл фотометрического реагента № 2 для проведения цветной реакции, перемешивают и выдерживают 3-10 мин в темном месте при (20±2)°С. Растворы в колбах доводят дистиллированной водой до метки и перемешивают. Измеряют интенсивность красной окраски на фотоэлектроколориметре при λ = 538 нм в кювете с толщиной поглощающего свет слоя 1 см в отношении контрольного раствора. По полученным средним данным из трех стандартных растворов на миллиметровой бумаге строят калибровочный график. На оси абсцисс откладывают концентрацию нитрита натрия (мкг в 1 мл окрашенного раствора); на оси ординат- соответствующую оптическую плотность. Пример калибровочного графика приведен на рисунке 1.
Массовую долю нитрита нитрия (х 1) мг, определяют о формуле
где m – масса NaNO2 в 1 мл окрашенного раствора, найденного по калибровочному графику, мкг; m0 – масса навески продукта, г; V – объем фильтрата, взятый для фотометрического измерения, мл; 1000 – перевод в миллиграммы. За конечный результат принимают среднее арифметическое трех параллельных определений, допустимые расхождения между которыми не должны превышать 0,2 мкг. Вычисления проводят с точностью до 0,1 мг в 100 г продукта. После выполнения работы делают заключение о соответствии массовой доли нитрита натрия в колбасных изделиях требованиям государственного стандарта. Контрольные вопросы 1. Что такое пищевые добавки? 2. Какова роль пищевых добавок в создании продуктов питания? 3. Какова классификация пищевых красителей? Чем объясняется повышенное внимание потребителей и технологов к окраске продуктов питания? 4. Какие натуральные красители вам известны? Каковы источники их получения? 5. Какие красители относятся к синтетическим? Каковы их особенности по сравнению с натуральными красителями? 6. Какие пищевые красители запрещены к применению в РФ? 7. Что такое «цветокорректирующие материалы»? Какие представители этой группы соединений вам известны? 8. Роль нитрита натрия в производстве мясных продуктов питания. 9. Какими фотометрическими методами определяют нитриты и нитраты. На чем они основаны? 10. В чем опасность применения нитритов и нитратов в продуктах питания? 11. С какими веществами мяса образуют устойчивые соединения нитраты и нитраты. 12. Массовая доля нитрита натрия в колбасных изделиях согласно требованиям государственного стандарта. 13. Изложите методику подготовки пробы исследуемого продута для проведения анализа. 14. Принцип построения калибровочного графика.
Аромат пищевых продуктов
Лабораторная работа № 5 Порядок выполнения работы В стакан вместимостью 100 мл отвешивают 26 г продукта. Навеску растирают стеклянной палочкой с небольшим количеством дистиллированной воды температурой 60-700С и полностью переносят в мерную колбу на 200 мл, смывая стакан несколько раз водой. Колбу с навеской охлаждают до 20±20 и прибавляют 5 мл раствора ацетата цинка (реактив 1), а через 2-3 мин – 5 мл раствора гексацианоферрата калия (II) (реактив 2). Следует соблюдать последовательность добавления упомянутых растворов. После добавления каждого раствора содержимое колбы осторожно перемешивают круговыми движениями во избежание образования пузырьков, доводят водой до метки, снова перемешивают и спустя 10 мин фильтруют через сухой складчатый бумажный фильтр в сухую колбу. 50 мл фильтрата переносят пипеткой в мерную колбу на 100 мл, добавляют 0,8 г оксида кальция и выдерживают колбу на кипящей водяной бане в течение 4-5 мин, перемешивая содержимое. После этого колбу с раствором быстро охлаждают до температуры 20±20С и прибавляют 2 мл концентрированной уксусной кислоты. (Допускается неполное растворение оксида кальция.) Колбу доливают до метки дистиллированной водой, тщательно перемешивают и фильтруют через складчатый бумажный фильтр. Кювету сахариметра длиной 400 мм заполняют фильтратом дважды и каждый раз делают по 3-5 отсчетов шкалы сахариметра. Среднее арифметическое результатов показаний шкалы сахариметра находят из 6-10 отсчетов.
Расчеты: Массовую долю сахарозы в плавленых сырах вычисляют по формуле
S = 2 PK, где Р – среднее показание шкалы сахариметра; К – поправка на объем осадка (0,975). За окончательный результат определения принимают среднее арифметическое двух параллельных определений. Расхождение между двумя параллельными определениями не должно превышать 0,5%. Сахариметр имеет линейную международную сахарную шкалу, градуированную в градусах 0S. Отсчет 1000 по шкале получают, когда в кювете длиной 200 мм поляризуют раствор, содержащий 26 г чистой сахарозы при t = 200С. Таким образом, 10 международной сахарной шкалы соответствует раствору, содержащему в 100 мл 0,26 г сахарозы. Навеска сахарозы массой 26 г называется нормальной. 10 международной шкалы сахариметра соответствует 0,346150 круговой шкалы поляриметра, а 10 шкалы поляриметра соответствует 2,88890 международной шкалы сахариметра.
Приготовление реактивов Реактив 1 (ацетат цинка). 60 г ацетата цинка растворяют в дистиллированной воде в химическом стакане на 100 мл при слабом подогревании и переливают в мерную колбу на 200 мл. Стакан промывают водой. В колбу пипеткой приливают 9 мл концентрированной уксусной кислоты и доливают до метки дистиллированной водой. Реактив 2 (гексацианоферрат (II) калия K4[Fe(CN)6]). 30 г гексацианоферрата (II) калия растворяют в дистиллированной воде в химическом стакане на 100 мл при слабом подогревании и переливают в мерную колбу на 200 мл. Стакан промывают водой. Раствор в колбе доливают до метки дистиллированной водой.
Контрольные вопросы 1. Что такое подслащивающие вещества (подсластители)? Дайте их классификацию. 2. Охарактеризуйте представителей интенсивных подсластителей. 3. Почему интенсивные подсластители широко применяются в пищевой технологии? 4. Технологические функции сахарозы. 5. На чем основан поляриметрический метод анализа сахарозы?
Лабораторная работа № 4. Порядок выполнения работы Выбор светофильтра В пробирке смешивают 2 мл 1%-ного раствора сульфата меди, 1 мл 5%-ного водного раствора аммиака и 2 мл воды. Содержимое пробирки встряхивают и измеряют интенсивность образовавшейся окраски при разных светофильтрах (длинах волн) с целью уточнения максимума поглощения. Данные заносят в табл. 2 и строят график изменения оптической плотности от длины волны и выбирают для работы светофильтр, при котором оптическая плотность раствора максимальна. Таблица 2. Зависимость оптической плотности раствора от длины волны
Список использованной литературы 1. Руководство по методам анализа качества и безопасности пищевых продуктов/ под ред. Скурихина И.М., Тутельяна В.А. – М.: Брандесс Медицина, 1998. – 342 с. 2. Крусь Г.Н., Шалыгина А.М., Волокитина З.В. Методы исследования молока и молочных продуктов. – М.: Колос, 2000. – 368 с. 3. Антипова Л.В., Глотова Н.Н. Методы исследования мяса и мясных продуктов. – М.: Колос, 2001. – 371 с. 4. Журавская Н.К., Алехин Л.Т., Отряшенкова Л.М. Исследование и контроль качества мяса и мясопродуктов. – М.: Агропромиздат, 1985. – 296 с. 5. Химический состав российских пищевых продуктов: Справочные таблицы /под ред Скурихина И.М., Тутельяна В.А.– М.: ДеЛи принт, 2002. – 236 с. 6. Антипова Л.В., Данилов В.Н. Методические указания к выполнению лабораторных работ по дисциплине «Пищевая химия» (для студентов спец. «Технология мяса и мясопродуктов»)/ Воронеж. гос. технол. акад. – Воронеж, 1998. – 24 с. 7. Попов М.П., Витол И.С., Суслянок Г.М. Учебно-методическое пособие по курсу «Пищевая химия» (для студентов технологических специальностей заочной формы обучения). – М.: Издательский комплекс МГУПП, 2000. – 52 с. 8. Методические указания к выполнению лабораторных работ по курсу «Пищевая химия» (для студентов технологических специальностей) / под ред. А.П. Нечаева. – М.: Издательский комплекс МГАПП, 1994. – 38 с. 9. Нечаев А.П., Кочеткова А.А., Зайцев А.Н.. Пищевые и биологически активные добавки. - М: Колос, 2004. 10. Булдаков А. Пищевые добавки. Справочник. - М: Дели, 2001. 11. ПилатТ.Л., Иванов А.А. Биологически активные добавки к пище (теория, производство, применение).- М.: Авваллон, 2002.- 710 с.
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
Кафедра химии
ОПД. Ф. 09.02 ПИЩЕВЫЕ И БИОЛОГИЧЕСКИ АКТИВНЫЕ ДОБАВКИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ к выполнению лабораторных работ
Направление подготовки дипломированного специалиста 260200 Производство продуктов питания из растительного сырья специальности: 260201 Технология хранения и переработки зерна 260202 Технология хлеба, кондитерских и макаронных изделий 260203 Технология бродильного производства и виноделия
260500 Технология продовольственных продуктов специального назначения и общественного питания специальности: 260501 Технология продуктов общественного питания Уфа 2013
УДК 54:6.63:6.64(07) ББК 24:36-1 Г 48
Рекомендовано к изданию методической комиссией факультета пищевых технологий
(протокол № от «____» __________ 2013 г.)
Составитель: Чернышенко Ю.Н.
Ответственный за выпуск: заведующий кафедрой химии Исламова Р.М.
Оглавление
ВВЕДЕНИЕ
Методические указания к лабораторным работам по дисциплине «Пищевые и биологически активные добавки» предназначены для студентов 3 курса факультета пищевых технологий. Каждая лабораторная работа выполняется студентами индивидуально и проводится в течение 4-х часов следующим образом: 1) студент дома самостоятельно знакомится с целью работы, изучает методическое указание и соответствующую учебную литературу, оформляет описательную часть отчета; 2) на занятии студент получает задание у преподавателя и приступает к выполнению работы; 3) после завершения работы студент приводит рабочее место в порядок, делает необходимые расчеты, заканчивает оформление отчета и сдает его преподавателю.
Работа считается выполненной студентом только тогда, когда отчет со всеми результатами и сделанными на основании их выводами принят преподавателем. Предлагаемые методические указания составлены на основе опыта проведения лабораторных занятий на кафедре химии Башкирского государственного аграрного университета.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-27; просмотров: 188; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.131.64 (0.019 с.) |


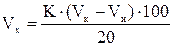 ,
,
 ,
, = 0,9877×(3,21-2,18)×5 = 5,09 мл
= 0,9877×(3,21-2,18)×5 = 5,09 мл ,
, = 0,014461×250 = 3,62%
= 0,014461×250 = 3,62%




