Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Биохимические изменения при ИБССодержание книги
Поиск на нашем сайте
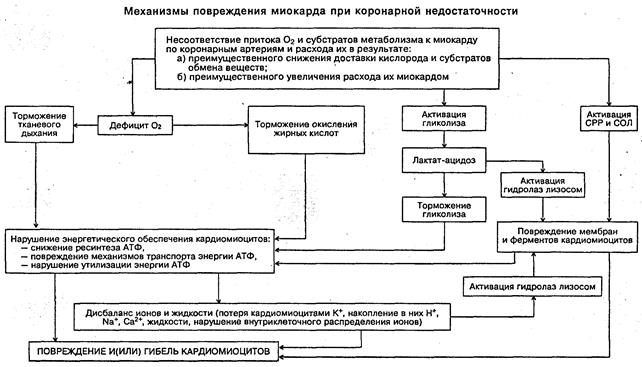
· гипоксия · снижение количества гликогена и глюкозы · накопление лактата, неокисленных жирных кислот · ацидоз · активация СРО и накопление токсичных продуктов ПОЛ · снижение активности ферментов аэробного дыхания, синтеза клеточных структур, транспорта субстратов обмена веществ и катионов. · перестройка изоферментного спектра · изменение ионного равновесия · воспалительная реакция · уменьшение электрической активности · нарушение «энергоснабжения» · повреждение клеток, субклеточных частиц, мембран · снижением сократительной функции сердца · нарушением кровообращения в органах и тканях
В условиях гипоксии миокард поглощает ТГ из липопротеинов, при этом они не используются, а накапливаются, приводя к ожирению миокарда. В условиях ИБС назначают безжировую диету, повышают уровень ЛПВП в крови.
Дефицит энергии в клетках миокарда обусловливает также развитие аритмий, что является одной из наиболее частых причин внезапной смерти пациентов с КН. Повреждение мембранного аппарата и ферментных систем кардиомиоцитов Основные свойства миокарда (автоматизм, возбудимость, проводимость, сократимость), а также их регуляция в значительной мере зависят от состояния мембран и ферментов клеток миокарда. В условиях КН их повреждение является следствием действия ряда общих механизмов. К числу наиболее значимых среди них относятся избыточная интенсификация свободнорадикальных реакций и перекисного окисления липидов; чрезмерная активация лизосомальных, свободных и мембранно-связанных гидролаз (протеаз, липаз, фосфолипаз и др.); внедрение продуктов указанных процессов (жирных кислот, гидроперекисей липидов, других амфифильных соединений) в мембраны кардиомиоцитов; торможение «субстрат- и энергозависимых» процессов ресинтеза поврежденных липидных и белковых компонентов мембран и синтеза их заново; нарушение конформации молекул белков (структурных, ферментов) и липопротеидов; растяжение и микроразрывы мембран в результате набухания клеток миокарда и их органелл. Важно заметить, что все указанные механизмы прямо или опосредованно обусловливают повреждение, изменение конформации и(или) кинетических свойств ферментов, многие из которых связаны с мембранами кардиомиоцитов (подробнее анализ реализации названных выше механизмов см. в разделе «Повреждение клетки»). Дисбаланс ионов и жидкости КН характеризуется существенными нарушениями общего содержания ионов и жидкости в ткани миокарда, их внутри- и внеклеточного соотношения, а также интрацеллюлярного распределения. Как правило, дисиония развивается «вслед» или одновременно с расстройствами реакций энергообеспечения кардиоцитов, а также — повреждением их мембран и ферментов. Дисбаланс ионов в свою очередь лежит в основе нарушения таких фундаментальных процессов, протекающих в клетках миокарда, как возбуждение, электромеханическое сопряжение, сокращение и расслабление, ритмогенез, расстройство которых характерно для КН. В основе указанных изменений лежит выход ионов калия из ишемизированных кардиомиоцитов, накопление в них натрия, кальция, а также жидкости. В отдаленных от зоны ишемии участках сердца концентрация указанных и других ионов, а также жидкости тоже меняется, однако степень этих изменений значительно меньшая. В качестве ведущих причин К+ — Na+ дисбаланса при КН называют дефицит АТФ, повышение проницаемости сарколеммы и торможение активности К+Ма2+-зависимой АТФазы, что создает возможность пассивного выхода К+из клетки и входа в нее Na+ по градиенту концентрации. КН сопровождается также высвобождением больших количеств К+ и Са2+ из митохондрий. Непосредственными факторами, обусловливающими этот процесс, могут быть снижение мембранного потенциала деэнергизированных митохондрий и увеличение проницаемости их мембраны под влиянием ацидоза, продуктов СПОЛ и фосфолипаз, активируемых Са2+. Значительное количество К+ высвобождается и при гликолитиЧеском распаде молекул гликогена (синтез которого идет с захватом ионов калия). Потеря К+ клетками миокарда при КН сопровождается повышением содержания его в крови. Гиперкалиемия является характерным признаком КН, особенно завершающейся развитием инфаркта миокарда. В эксперименте на собаках уже в первые пять минут ишемии содержание калия в крови, оттекающей как от ишемизированной, так и отдаленной зон, существенно увеличивается. Нарушение энергообеспечения кардиомиоцитов, повреждение их мембран и ферментов, дисбаланс ионов и жидкости в совокупности обусловливают расстройство механизма регуляции объема клеток миокарда при КН. Последнее является результатом повышения проницаемости клеточных мембран для ионов и органических гидрофильных молекул (белка, углеводов); гиперосмии кардиомиоцитов в результате накопления в них ионов (натрия, кальция) и мелкодисперсных соединений (альбуминов, пирувата, лактата); гипергидратации и набухания клеток; снижение механической прочности биологических мембран.
|
||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 435; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.007 с.) |