
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Разделение катионов методом бумажной хроматографии.
Приборы и реактивы: исследуемый раствор, содержащий смесь ионов Fе3+ и Сu2+, Н2О (дистиллированная), раствор К4[Fe(CN)6], хроматографическая бумага, стаканы, Цель работы: Разделение катионов методом бумажной хроматографии. Алгоритм выполнения.
Практический навык №14 Адсорбционная хроматография на колонках. Приборы и реактивы исследуемый раствор, содержащий смесь ионов Fе3+ и Сu2+, хроматографическая колонка (стеклянная трубка), заполненная на 2/3 адсорбентом. Цель работы: Разделение катионов методом колоночной хроматографии. Алгоритм выполнения.
Практический навык №15. Определение плотности исследуемых растворов. Приборы и реактивы: исследуемые растворы, цилиндры, набор ареометров, справочные данные. Цель работы: Определение концентрации раствора по его плотности.
Алгоритм выполнения.
Рубежный контроль №2
Практический навык №1.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 374; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.130.13 (0.005 с.) |

 моль/л
В этих формулах:
Мх – молярная масса вещества, г/моль,
w - массовая доля растворенного вещества,
d – плотность исследуемого раствора, г/мл.
моль/л
В этих формулах:
Мх – молярная масса вещества, г/моль,
w - массовая доля растворенного вещества,
d – плотность исследуемого раствора, г/мл.
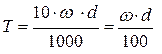 г/мл
г/мл



