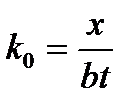Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Математична обробка результатівСодержание книги Поиск на нашем сайте
Спостережувані константи швидкості реакції ацидолізу епіхлоргідрину були розраховані за рівняннями:
де k0 – константа швидкості реакції, розрахована за рівнянням (1.3.1), с-1; k1 – константа швидкості реакції, розрахована за рівнянням(1.3.2), л/моль·с; x – концентрація вільного кислотного гідроксилу, моль/л; a – вихідна концентрація ацетилсаліцилової кислоти, моль/л; (а – x) – поточна концентрація ацетилсаліцилової кислоти, моль/л; b – вихідна концентрація ЕХГ, моль/л; t – час перебігу реакції, с. Таблиця 2.1 Кінетика реакції ацетилсаліцилової кислоти (a=0,333 моль/л) с ЕХГ (b=12 моль/л) в присутності ТЕАБ (m=0,005 моль/л) при 60 °С.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
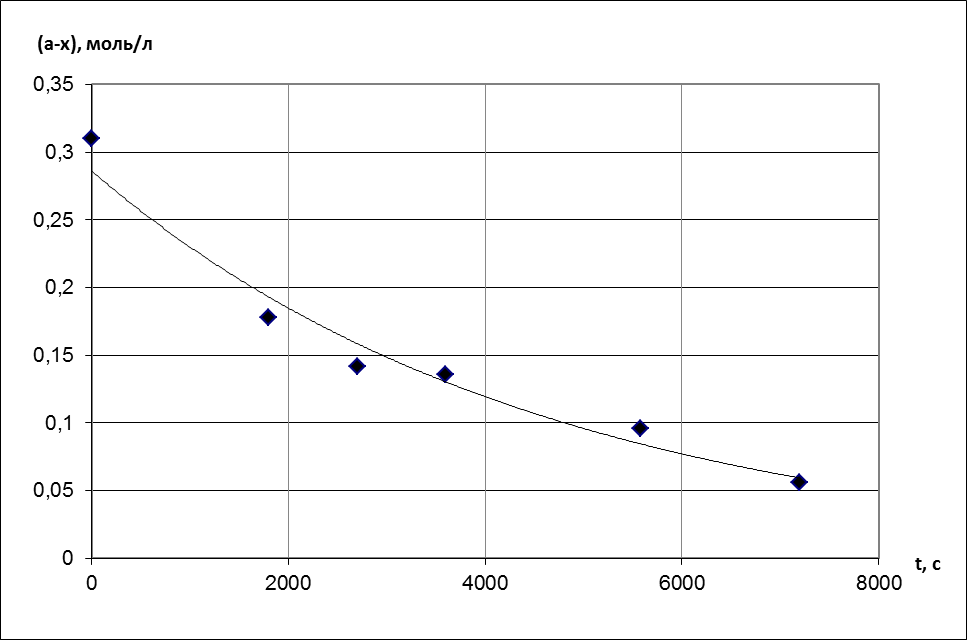
Першочерговим завданням для отримання кінетичних параметрів реакції ацидолізу ЕХГ ацетилсаліциловою кислотою в присутності тетраетиламоній броміду є встановлення порядків реакції за вихідними реагентами та кінетичного закону, що описує даний процес. Для оцінки порядку реакції за кислотою проведені дослідження реакції ацидолізу ЕХГ в присутності тетраетиламоній броміду при температурі 60 °С. За отриманими даними побудовано графічну залежність конверсії епоксидних груп від часу (рис. 2.1). Рис. 2.1. Залежність виходу хлоргідринового ефіру (%) в реакції ацетилсаліцилової кислоти (а, моль/л) з ЕХГ (b, моль/л) в присутності тетраетиламоній броміду (m=0,005 моль/л) від часу (t, c) при 60ºС.
Залежність в координатах зміни концентрації ацетилсаліцилової кислоти від часу має криволінійний характер, тому для визначення порядку реакції побудовано графічну залежність ln (a – x) від t. Рис. 2.2. Залежність натурального логарифму виходу хлоргідринового ефіру (%) в реакції ацетилсаліцилової кислоти (а, моль/л) з ЕХГ (b, моль/л) в присутності тетраетиламоній броміду (m=0,005 моль/л) від часу (t, c) при 60ºС.
Отримано прямолінійну залежність із задовільним коефіцієнтом кореляції, що свідчить на користь першого порядку реакції за ацетилсаліциловою кислотою. За експериментальними даними розраховані спостережувані константи швидкості за рівнянням псевдопершого порядку (див. табл. 1.3.1). Аналіз даних показує, що константи швидкості є сталими у межах похибки експерименту, що також підтверджує перший порядок реакції за кислотним реагентом. З літературних даних відомо, що порядок реакції за епіхлоргідрином – перший, за каталізатором – перший. Таким чином, з урахуванням визначеного порядку за кислотним реагентом кінетичне рівняння реакції ЕХГ з ацетилсаліциловою кислотою має вигляд:
ВИСНОВКИ 1. З’ясована ефективність реакції детоксикації епоксидних сполук ацетилсаліциловою кислотою на прикладі модельної реакції ацидолізу ЕХГ. 2. Досліджено кінетику реакції ЕХГ з ацетилсаліциловою кислотою в присутності тетраетиламоній броміду. 3. Встановлено перший порядок реакції за ацетилсаліциловою кислотою.На основі отриманих та літературних даних встановлено перший порядок реакції ЕХГ з ацетилсаліциловою кислотою в присутності тетраетиламоній броміду.
СПИСОК ЛІТЕРАТУРИ
1. Пакен А.М. Эпоксидные соединения и эпоксидные смолы /Л.: Госхимиздат, 1962. - С.568-614. 2. Химические методы получения глицидиловых эфиров карбоновых кислот / М.Ф Сорокин., М.Г.Шодє, А.И. Кузьмин и др. // Труды МХТИ им. Д.И., 1982, - №4. – С.4. 3. Кинетика реакции ЭХГ с фенолом при катализе солями четвертичного аммония / Д.Р. Меджитов, Е.А. Коновалова, Л.Г. Шодэ и др.// Деп. ВИНИТИ 13.11.91. ― №4266 В.91 – М. – 1991 – 9с. 4. Кинетика и механизм реакции замещенных α-окисей с карбоновыми кислотами / И.М. Шологон, М.С. Клебанов, В.А. Алдошин и др. // Кинетика и катализ, 1985. – Т.23, №5. – С.841 – 846. 5. Региоселективное раскрытие пропиленоксида / Н.Н. Лебедев, Е.В. Соколова, О.А. Тюкова и др. // Журн. орг. химии, 1965. - №5. – С. 608-612. 6. Исследование реакции образования хлоргидриновых эфиров карбоновых кислот / И.М. Шологон, М.С. Клебанов, В.А. Алдошин и др. // Кинетика и катализ, 1985. --№ 5. – С.1059 – 1061. 7. Белов П.С. Н.С. Барай, К.П. Коренев. Изучение реакции карбоновых кислот с эпихлоргидрином в присутствии анионообменной смолы АВ – 17 как катализатора / Известия ВУЗ-ов. Химия и хим. технол., 1983. – Т. 26, № 6. – С. 668-672. 8. Механизм реакций глицидиловых эфиров с карбоновыми кислотами / М.С. Клебанов, Ф.Ю. Кирьязев, А.Ю. Червинский и др. // Журн. орг. химии, 1984. - №11. – С. 2407-2411. 9. Швец В.Ф. Н.Н. Лебедев, О.А. Тюкова Кинетика и стериохимия некаталитической реакции α – оксидов со спиртами и карбоновыми кислотами. / Журн. орг. химии, 1971. - №9. – С. 1851-1856. 10. Bukowska A.,Bukowski W. A higly regioselective catalyst of epichlorohydrin acidolysis / J.Chem. Technol. Biotechnol., 1998. - № 73 – P. 341-344. 11. Розентулер Е.М., Николаев А.Ф. Образование хлоргидриновых эфиров и дегидрохлоридов при синтезе эпоксидных смол / Журн. прикл. химии, 1969.-Т.12,№8.-С.1881-1887. 12. О механизме реакции глицидиламинов с карбоновыми кислотами / М.С. Клебанов, Ф.Ю. Кирьязев, И.М. Шологон и др. // Кинетика и катализ., 1984. – Т.25, Вып.4. – С. 1004-1007. 13. Сорокин М.Ф., Гершанова Э.Л. О механизме реакций моноэпоксидных соединений с карбоновыми кислотами / Кинетика и катализ, 1967. ― Т.8, № 3. ― С.512-519. 14. Справочник химика / Под редакцией Б.П. Никольского и др. – М. – Л.: Химия, 1971. – Т.2, -- 1168 с. 15. Вейганд К., Хильгетаг Г. Методы эксперимента в органической химии. М.: Химия, 1969. – с. 430, 449-450. 16. Эммануэль Н.М., Кнорре Д.Г. Курс химической кинетики / М.: Высшая школа, 1969. – 431 с.: ил.
|
||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-16; просмотров: 290; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.209.20 (0.009 с.) |