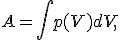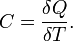Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутренняя энергия. Работа в термодинамике. Количество теплоты. Теплоемкость.Содержание книги
Поиск на нашем сайте Вну́тренняя эне́ргия тела (обозначается как E или U) — это сумма энергий молекулярных взаимодействий и тепловых движений молекулы. Внутренняя энергия является однозначной функцией состояния системы. Это означает, что всякий раз, когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе из одного состояния в другое будет всегда равно разности между ее значениями в конечном и начальном состояниях, независимо от пути, по которому совершался переход. Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:
где
U = A/q Эта формула является математическим выражением первого начала термодинамики Для квазистатических процессов выполняется следующее соотношение:
где
Работа в термодинамике При рассмотрении термодинамических процессов механическое перемещение макротел в целом не рассматривается. Понятие работы здесь связывается с изменением объема тела, т.е. перемещением частей макротела друг относительно друга. Процесс этот приводит к изменению расстояния между частицами, а также часто к изменению скоростей их движения, следовательно, к изменению внутренней энергии тела.
Рис. 1 Пусть в цилиндре с подвижным поршнем находится газ при температуре T 1 (рис. 1). Будем медленно нагревать газ до температуры T 2. Газ будет изобарически расширяться, и поршень переместится из положения 1 в положение 2 на расстояние Δ l. Сила давления газа при этом совершит работу над внешними телами. Так как p = const, то и сила давления F = pS тоже постоянная. Поэтому работу этой силы можно рассчитать по формуле
где Δ V — изменение объема газа. Если объем газа не изменяется (изохорный процесс), то работа газа равна нулю. Сила давления газа выполняет работу только в процессе изменения объема газа. При расширении (Δ V > 0) газа совершается положительная работа (А > 0); при сжатии (Δ V < 0) газа совершается отрицательная работа (А < 0), положительную работу совершают внешние силы А’ = - А > 0. Запишем уравнение Клапейрона—Менделеева для двух состояний газа:
Следовательно, при изобарном процессе
Если m = М (1 моль идеального газа), то при Δ Τ = 1 К получим R = A. Отсюда вытекает физический смысл универсальной газовой постоянной: она численно равна работе, совершаемой 1 моль идеального газа при его изобарном нагревании на 1 К. На графике p = f (V) при изобарном процессе работа равна площади заштрихованного на рисунке 2, а прямоугольника.
Рис. 2 Если процесс не изобарный (рис. 2, б), то кривую p = f (V) можно представить как ломаную, состоящую из большого количества изохор и изобар. Работа на изохорных участках равна нулю, а суммарная работа на всех изобарных участках будет
т.е. будет равна площади заштрихованной фигуры. При изотермическом процессе (Т = const) работа равна площади заштрихованной фигуры, изображенной на рисунке 2, в. Определить работу, используя последнюю формулу, можно только в том случае, если известно, как изменяется давление газа при изменении его объема, т.е. известен вид функции p (V). Таким образом, газ при расширении совершает работу. Приборы и агрегаты, действия которых основаны на свойстве газа в процессе расширения совершать работу, называются пневматическими. На этом принципе действуют пневматические молотки, механизмы для закрывания и открывания дверей на транспорте и др. Коли́чество теплоты́ — энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин. Количество теплоты является функцией процесса, а не функцией состояния, то есть количество теплоты, полученное системой, зависит от способа, которым она была приведена в текущее состояние. Единица измерения: Джоуль Дж Теплоёмкость тела (обычно обозначается латинской буквой C) — физическая величина, определяющая отношение бесконечно малого количества теплоты δ Q, полученного телом, к соответствующему приращению его температуры δ T:
Единица измерения теплоёмкости в системе СИ — Дж/К.
|
|||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 394; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.007 с.) |

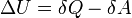
 — подведённая к телу теплота, измеренная в джоулях
— подведённая к телу теплота, измеренная в джоулях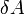 [1] — работа, совершаемая телом против внешних сил, измеренная в джоулях
[1] — работа, совершаемая телом против внешних сил, измеренная в джоулях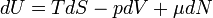
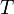 — температура, измеренная в кельвинах
— температура, измеренная в кельвинах — энтропия, измеренная в джоулях/кельвин
— энтропия, измеренная в джоулях/кельвин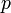 — давление, измеренное в паскалях
— давление, измеренное в паскалях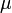 — химический потенциал
— химический потенциал — количество частиц в системе
— количество частиц в системе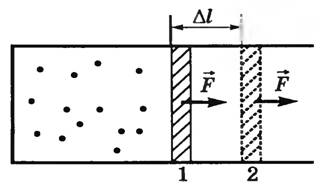


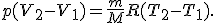


 , или
, или