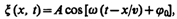Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Механические волны (продольные и поперечные). Графическое представление. Длина волны. Уравнения плоской бегущей волны. Стояние воды.Содержание книги
Поиск на нашем сайте Волна - это колебания, распространяющиеся в пространстве в течениие времени. Для возникновения волны нужна деформация (наличие Fупр) среды. Механические волны делятся на: а) продольные
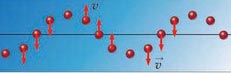
- колебания среды происходят вдоль направления распространения волн,
- возникают в любой среде (жидкости, в газах, в тв. телах). б) поперечные
-колебания среды происходят перпендикулярно направлению их распространения,
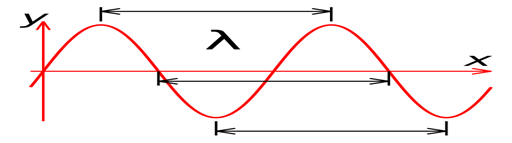
Длина́ волны́ — расстояние между двумя ближайшими друг к другу точками, колеблющимися в одинаковых фазах
Волнам де Бройля также соответствует определенная длина волны. Частице с энергией Е и импульсом p, соответствуют: частота: где h — постоянная Планка.
В общем случае уравнение плоской волны, распространяющейся вдоль положительного направления оси х в среде, не поглощающей энергию, имеет вид
где А = const — амплитуда волны, w — циклическая частота, j 0 — начальная фаза волны, определяемая в общем случае выбором начал отсчета х и t, [ w (t—x/v)+ j 0] — фаза плоской волны Стоя́чая волна́ — колебания в распределённых колебательных системах с характерным расположением чередующихся максимумов (пучностей) и минимумов (узлов) амплитуды. Практически такая волна возникает при отражениях от преград и неоднородностей в результате наложения отражённой волны на падающую. При этом крайне важное значение имеет частота, фаза и коэффициент затухания волны в месте отражения. Примерами стоячей волны могут служить колебания струны, колебания воздуха в органной трубе 18. Атомно-молекулярная теория строения вещества. Принципы молекулярной теории (МКТ) газа. Уравнение состояния и его параметры(давление, объем, температура). Физический смысл температуры(по Кельвину). Молекулы состоят из атомов. Атом – мельчайшая, далее химически неделимая составная часть молекулы Получается, молекулярная теория объясняет физические явления, которые происходят с веществами. Учение об атомах приходит на помощь молекулярной теории при объяснении химических явлений. Обе эти теории – молекулярная и атомная – объединяются в атомно-молекулярное учение. Сущность этого учения можно сформулировать в виде нескольких законов и положений: 1. вещества состоят из атомов; 2. при взаимодействии атомов образуются простые и сложные молекулы; 3. при физических явлениях молекулы сохраняются, их состав не изменяется; при химических – разрушаются, их состав изменяется; 4. молекулы веществ состоят из атомов; при химических реакциях атомы в отличие от молекул сохраняются; 5. атомы одного элемента сходны друг с другом, но отличаются от атомов любого другого элемента; 6. химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества. В середине ХVIII века великий русский учёный М.В. Ломоносов обосновал атомно-молекулярные представления в химии. Основные положения его учения изложены в работе «Элементы математической химии» (1741 г.) и ряде других. Ломоносов назвал теорию корпускулярно-кинетической теорией.
В основе молекулярно-кинетической теории лежат три основных положения: 1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»). Молекулы химического вещества могут быть простыми и сложными, т.е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы. 2. Атомы и молекулы находятся в непрерывном хаотическом движении. 3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало Любая термодинамическая система при неизменных внешних условиях самопроизвольно переходит в состояние термодинамического равновесия (это такое состояние, при котором все макроскопические параметры сколь угодно долго остаются неизменными). Температура тела – это физический параметр, одинаковый во всех частях системы тел, которая находится в состоянии термодинамического равновесия. При тепловом равновесии микроскопические процессы внутри тела (движение частиц и взаимодействие частиц) не прекращаются. Термодинамическая система может находиться в различных состояниях теплового равновесия, каждому из которых соответствует определённое значение температуры. При теплообмене между телами происходит обмен энергией: тела с большей энергией передают свою энергию телам с меньшей энергией. Направление теплообмена между ними указывает разность температур тел. То есть энергия передаётся от более горячего тела к менее горячему Ке́львин (обозначение: K) — единица измерения температуры в Международной системе единиц (СИ), одна из семи основных единиц СИ. Предложена в 1848 году. Один кельвин равен 1/273,16 части термодинамической температуры тройной точки воды[1]. Начало шкалы (0 К) совпадает с абсолютным нулём. Пересчёт в градусы Цельсия: °С = K−273,15 (температура тройной точки воды — 0,008 °C)
|
||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 435; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.216 (0.01 с.) |




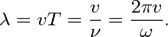 фазовая скоростью (
фазовая скоростью (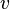 ) и частотой (
) и частотой ( )
)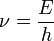 длина волны:
длина волны: