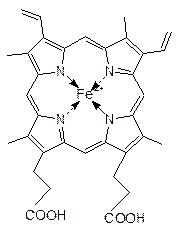Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Структурная организация белковых молекулСодержание книги Поиск на нашем сайте Белки - очень крупные молекулы, молярная масса белков колеблется от 6ооо до 1 млн. грамм/моль (см. таблицу).
Некоторые белки в своем составе могут иметь химические группы небелковой природы. Такие белки называют сложными или холопротеинами. Неаминокислотную часть белков называют простетической группой, белковую часть - апоферментом. Сложные белки классифицируются по простетической группе. Например, липопротеины это белки, содержащие в своем составе группу - липид; металлопротеины содержат в своем составе ионы металла; в состав хромопротеинов входит хромофор, окрашенная группа небелковой природы. Частный случай, когда хромофором является гем. К таким белкам относятся гемоглобин и цитохромы. Простетические группы играют важную роль при функционировании сложного белка.
Простые белки можно классифицировать по форме молекул и по способности растворяться в воде на глобулярные и фибриллярные. Глобулярные белки имеют форму глобулы и, как правило, растворимы в воде. Фибриллярные белки имеют форму вытянутого волокна - фибриллы и нерастворимы в воде. Фибриллярные белки выполняют главным образом опорные функции, обеспечивая прочность тканей; глобулярные белки более разнообразны по функциям. Первичная структура белков
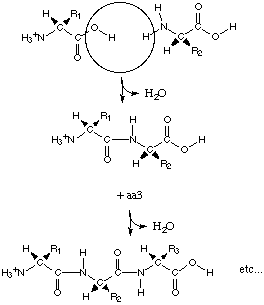
Первичной структурой белка называют состав и последовательность аминокислотных остатков в белковой молекуле. Аминокислоты в белке связаны пептидными связями. Все молекулы данного индивидуального белка идентичны по аминокислотному составу, последовательности аминокислотных остатков и длине полипептидной цепи. Установление последовательности аминокислотной последовательности белков - трудоемкая задача. Более подробно на эту тему мы поговорим на семинаре. Инсулин был первым белком, для которого установили аминокислотную последовательность. Бычий инсулин имеет молярную массу около 5700. Его молекула состоит из двух полипептидных цепей: А-цепи, содержащей 21 а.к., и В-цепи, содержащей 30 а.к., эти две цепи соединены двумя дисульфидными (-S-S-) связями. Даже небольшие изменения первичной структуры могут значительно изменять свойства белка. Болезнь серповидноклеточная анемия является результатом изменения всего 1 аминокислоты в b-цепи гемоглобина (Glu ® Val). Видовая специфичность первичной структуры При изучении аминокислотных последовательностей гомологичных белков, выделенных из разных видов, было сделано несколько важных выводов. К гомологичным белкам относятся те белки, которые у разных видов выполняют одинаковые функции. Примером может служить гемоглобин: у всех позвоночных он осуществляет одну и ту же функцию, связанную с транспортом кислорода. Гомологичные белки разных видов обычно имеют полипептидные цепи одинаковой или почти одинаковой длины. В аминокислотных последовательностях гомологичных белков во многих положениях всегда находятся одни и те же аминокислоты - их называют инвариантными остатками. Вместе с тем в других положениях белков наблюдаются значительные различия: в этих положениях аминокислоты варьируются от вида к виду; такие аминокислотные остатки называются вариабельными. Всю совокупность сходных черт в аминокислотных последовательностях гомологичных белков объединяют в понятие гомология последовательностей. Наличие такой гомологии предполагает, что животные, из которых были выделены гомологичные белки, имеют общее эволюционное происхождение. Интересным примером является сложный белок - цитохром с - митохондриальный белок, учавствующий в качестве переносчика электронов в процессах биологического окисления. М» 12500, содержит»100 а.к. Были установлены а.к. последовательности для 60 видов. 27 а.к. - одинаковы, это указывает на то, что все эти остатки играют важную роль в определении биологической активности цитохрома с. Второй важный вывод, сделанный на основе анализа аминокислотных последовательностей, состоит в том, что число остатков, по которым различаются цитохромы с любых двух видов, пропорционально филогенетическому различию между данными видами. Например, молекулы цитохрома с лошади и дрожжей различаются по 48 а.к., у утки и курицы - по 2 а.к., у курицы и индейки не различаются. Сведения с числе различий в аминокислотных последовательностях гомологичных белков из разных видов используют для построения эволюционных карт, отражающих последовательные этапы возникновения и развития различных видов животных и растений в процессе эволюции.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 475; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.102 (0.009 с.) |