
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение съема металла и количества выделившихся газовСодержание книги
Поиск на нашем сайте
Если на электроде происходит одна электрохимическая реакция то массу снятого металла или выделившегося газа m определяют по первому закону Фарадея: m=к·I·t, (1.2) где к - электрохимический эквивалент металла, газа; I - сила тока; t - время электролиза.
При ЭХО на каждом электроде может протекать две и более реакций. На одну реакцию расходуется только часть общего тока. Поэтому для одной реакции массу снятого металла или выделевшегося газа определяют: m=η·к·I·t, (1.3) где η - коэффициент выхода по току металла или газа. Коэффициент выхода по току в настоящее время определяют экспериментальным путем. При ЭХО конструкционных, инструментальных сталей и сплавов в растворах NaCl η = 0,8...О,95, в растворах NaNO3 η =0,3...0,9. Для реакции выделения водорода при ЭХО в растворах NaCl η = 1, в растворах NaNO3, NH4NO3 η уменьшается до 0...0,2. Коэффициент выхода по току кислорода η ≤0,1. Объем выделившегося водорода V при ЭХО в растворе NaCl согласно законам Фарадея и Авогадро можно определить по упрощенной формуле V=К·m, где V - объем водорода, л; m - масса снятого металла, г; К - коэффициент, равный 0,43 - 0,45 л/г при температуре электролита 20 - 40°С. Порядок выполнения работы Экспериментальное определение линейного съема металла
с поверхности электрода-заготовки при ЭХО неподвижным электродом-инструментом за время t (рис.1.4). Подготовка к эксперименту I. Изучить установку (с.11-18) дан исследования процесса электрохимической размерной обработки. 2. Изучить правила техники безопасности (приложение 1). 3. Зачистить и протереть контактные поверхности образца и штока, 4. Установить обрабатываемый образец в контейнер и закрепить его на штоке винтом. 5. Закрыть крышку контейнера изакрепить её гайками. 6. Записать в отчет: материал ЭЗ и ЭИ, площадь обрабатываемой поверхности, химический состав электролита. 7. Ареометром измерять плотность электролита, установить соответствующую концентрацию раствора. 8. Термометром измерить температуру электролита. 9. Индикаторной бумагой определить кислотность pH электролита. 10. По суточному отстою электролита оценить степень его загрязнения в % (отношение объема, осадка к объему электролита). Результаты всех измерений записать в отчет.
Проведение эксперимента 1. Заполнить табл.1.1 отчета. 2. Установить начальный межэлектродный зазор а0=0,5 мм.Отсчет вести по индикатору часового типа. 3. Включить питание пульта управления и станка. 4. Включить подачу электролита и провести прокачку его в течение 1 минуты для установления стационарного режима. Если давления Рвх и Рвых отличаются от требуемых значений, подрегулировать их.
5. Включить вентиляцию. 6. Включить рабочее напряжение. В начальный момент времени зарегистрировать и записать в отчет (табл.1.2) значения силы тока I0 и напряжения U0. 7. В течение 1 минуты провести ЭХО образца. В конце обработки 8. Выключить ток, подачу электролита, вентиляцию. 9. Измерить конечный межэлектродный зазор ак (табл.1.2). 10. Повторить опыт еще 2 раза.
Оформление отчёта. 1. Вычислить средние арифметическое значения 2. Вычислить систематическую θ, случайную ε погрешности прямых измерений а0 и а к и доверительные интервалы Δа0 и ΔaК при доверительной вероятности 0,95. 3. Записать окончательный результат прямых измерений* 4. Рассчитать относительные ошибки δа0 и δак, 5. Вычислить линейный съём материала 6. Рассчитать доверительный интервал для значения х по формуле 7. Записать результат эксперимента в окончательном виде. 8. Сделать выводы о средней скорости съёма металла, об изменении силы тока и напряжения при ЭХО. ОТЧЕТ По лабораторной работе № I (ЭХО-1) студентов (Ф.И.О., № группы) ________________________________________ __________________________________________________________________
Исходные данные материал образца: сталь_________________________________________ площадь обрабатываемой поверхности образца S = 5 см2; р =_________г/см3, концентрация _________ %, Т =_________°С; давление электролита: Рвх = 0,15...0,2 МПа (1,5...2 кгс/см2), Рвых= 0,02...0,05 МПа (0,2...0,5 кгс/см2);
Т а б л и ц a 1.1
Т а б л и ц a 1.2
n=3; p=0,95; t=4,3;
εa = t·Sa =
Выводы:_________________________________________________________ ________________________________________________________________ ________________________________________________________________ ________________________________________________________________ ________________________________________________________________ ________________________________________________________________
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-07-11; просмотров: 394; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.009 с.) |

 В данной работе необходимо определить линейный съем металла
В данной работе необходимо определить линейный съем металла

 зарегистрировать силу тока Iк и напряжение UK (табл.1.2).
зарегистрировать силу тока Iк и напряжение UK (табл.1.2). и
и  .
.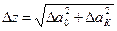


 =
= =
= =
= =
= =
=



