
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тесты к модулю №1 (для итогового рубежного контроля)Содержание книги
Поиск на нашем сайте
ТЕСТЫ к МОДУЛЮ №1 (для итогового рубежного контроля)
ТЕРМОДИНАМИКА. ХИМИЧЕСКОЕ РАВНОВЕСИЕ. 1) Известно, что для реакции 2CH4(г) + 2NH3(г)=2HCN(г) + 3H2O (ж) ΔH0=-345,2кДж и ΔG0=-325,9кДж. Следовательно, это реакция… 1) эндотермическая и при стандартных условиях протекает в прямом направлении 2) эндотермическая и при стандартных условиях протекает в обратном направлении 3) экзотермическая и при стандартных условиях протекает в обратном направлении 4) экзотермическая и при стандартных условиях протекает в прямом направлении 2) Для получения 1132 кДж тепла по реакции 2NO(г)+O2(г)↔2NO2(г), ∆Но= -566кДж необходимо затратить____ литр(ов) кислорода 1) 56 2) 11,2 3) 44,8 4) 22,4 3) Теплота, необходимая для испарения 18 г воды, если DfH0 образования жидкой воды (-285,3 кДж/моль), DfH0 образования газообразной воды (-241,8 кДж/моль) равна… 1) 43,5 кДж 2) 527,1 кДж 3) -43,5 кДж 4) 174 кДж 4) Для нахождения 1) 2) 3) 4) 5) Для нахождения 1) 2) 3) 4) 6) Если энтальпия образования SO2 равна -297 кДж/моль, то количество теплоты, выделяемое при сгорании 16г серы, равно... кДж 1) 148,5 2) 297 3) 594 4) 74,25 В реакции, протекающей в соответствии с термохимическим уравнением 3H2 + N2 = 2 NH3 + 92 кДж Выделилось 23 кДж теплоты. Объём полученного (при н.у.) аммиака составляет 1) 5,6 л 2) 11,2л 3) 22,4л 4) 44,8л 8) По термохимическому уравнению реакции С2Н4 + Н2О ↔ С2Н5ОН +46 кДж вычислите объём взятого этилена (н,у.), если известно, что выделившаяся в этом процессе теплота составила 138 кДж. 1) 44,8 л 2) 22,4л 3) 67,2л 4) 89,6л 9) В реакцию, протекающую в соответствии с термохимическим уравнением2Al + 3S = Al2S3 +509 кДж вступило 108 г алюминия. Количество выделившейся теплоты равно 1) 242,5 кДж 2) 509 кДж 3) 1018 кДж 4) 2036 кДж 10. В результате реакции, термохимическое уравнение которой 2Al +Fe2O3 = Al2O3 + 2 Fe +848 кДж, выделилось 169,6 кДж теплоты. Масса образовавшегося железа равна: 1) 11,2 г 2) 22,4 г 3) 56 г 4) 28 г 11) По термохимическому уравнению реакции горения ацетилена 2С2Н4 + 5О2 = 4СО2 + 2Н2О +2610 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило 67, 2 л ацетилена (н.у.) 1) 870 кДж 2) 3915 кДж 3) 5220 кДж 4) 7830 кДж В результате реакции, описываемой термохимическим уравнением 2С2Н4+ 5О2 = 4СО2 + 2Н2О +2610 кДж выделилось 652, 5 кДж теплоты. Оцените объём сгоревшего ацетилена
1) 11,2 л 2) 22,4 л 3) 44,8 л 4) 67,2 л 13. Согласно термохимическому уравнению реакции СН4 + 2О2 = СО2 + 2Н2О + 802 кДж количество теплоты, выделившейся при сжигании 24 г метана, равно 1) 1604 кДж 2) 1203 кДж 3) 601,5 кДж 4) 401 кДж 14. В результате реакции, термохимическое уравнение которой 4NH3 + 5O2 = 4NO + 6H2O + 902 кДж, выделилось 1127,5 кДж теплоты. Объём (н.у.) образовавшегося при этом оксида азота (II) равен 1) 112л 2) 11,2 л 3) 89,6 л 4) 896 л В результате реакции, термохимическое уравнение которой 2KClO3 = 2KCl + 3O2 +91 кДж выделилось 182 кДж теплоты. Масса образовавшегося при этом кислотрода равна 1) 96 г 2) 192 г 3) 288 г 4) 576 г 16. В соответствии с термохимическим уравнением C6H12O6 + 6O2 ↔ 6CO2 + 6 H2O + 2800кДж при образовании 12 моль углекислого газа 1) выделяется 2800 кДж теплоты 2) поглощается 2800 кДж теплоты 3) выделяется 5600 кДж теплоты 4) поглощается 5600 кДж теплоты 17. В соответствии с термохимическим уравнением 2 Na + Cl2 = 2NaCl + 411,3 кДж при окислении 4 моль натрия в избытке хлора 1) выделяется 411,3 кДж 2) поглощается 411,3 кДж 3) выделяется 822,6 кДж 4) поглощается 822,6 кДж 18. Согласно термохимическому уравнению ZnS + 2HCl ↔ ZnCl2 + H2S +139,3 кДж при образовании 0,5 моль ZnS в реакции 1) выделяется 69,65 кДж теплоты 2) поглощается 69,65 кДж теплоты 3) выделяется 139,3 кДж теплоты 4) поглощается 139,3 кДж теплоты 19. В соответствии с термохимическим уравнением реакции 2СH3OH +3O2 = 2CO2 +4H2O +1452 кДж при сгорании 8г метанола выделится ….. кДж теплоты 1) 181,5 2) 363 3) 726 4) 1452 20. В соответствии с термохимическим уравнением реакции С2H5OH +3O2 = 2CO2 +3H2O + 1370 кДж для получения 685 кДж теплоты требуется сжечь... г этанола 1) 23 2) 46 3) 92 4) 184 21. В результате реакции, термохимическое уравнение которой 2Мg + O2 = 2MgO +600 кДж выделилось 150 кДж теплоты. Масса сгоревшего магния составляет 1) 6 г 2) 12 г 3) 24 г 4) 48 г 22. При образовании аммиака согласно уравнению реакции N2 +3H2 = 2NH3 +92 кДж выделилось 230 кДж теплоты. При этом объём (н.у.) вступившего в реакцию водорода составил 1) 44,8 л 2) 56 л 3) 112 л 4) 168 л В реакции, протекающей в соответствии с термохимическим уравнением 3H2 + N2 = 2 NH3 + 92 кДж Выделилось 23 кДж теплоты. Объём полученного (при н.у.) аммиака 1) 5,6 л 2) 11,2л 3) 22,4л 4) 44,8л 24) По термохимическому уравнению С2Н4+Н2О↔С2Н5ОН+46 кДж Будет ли влиять давление на смещение равновесия данной реакции
H2 + Cl2 = 2 HCl 1) будет 2) нет 3) сместит равновесие вправо 4) сместит равновесие влево Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в прямом направлении 1) DG < 0 2) DG > 0, 3) DG = 0 3) 52,3 4) 104,6 52) Повышение давления смещает равновесие в сторону продуктов для реакции… 1) H2(г)+I2(к)↔2HI(г) 2) PCl5 (ж)↔ PCl3 (ж)+ Cl2(г) 3) 2HI(г) ↔ H2(г)+I2(г) 4) ВаО(к.) + СО2(г) ↔ ВаСО3(к.) 53) Для увеличения выхода продуктов реакции FeO(т) + H2(г)↔Fe(т) + H2O(г), ∆Н>0 необходимо… 1) понизить давление 2) понизить температуру 3) повысить давление Повысить температуру 54) Согласно первому началу термодинамики, справедливо выражение … 1) ∆U=A-Q 2) ∆U=Q+A 3) ∆U=∆Q+∆A 4) ∆U=Q-A 55) Для нахождения ∆Н0298 реакции 4HCN(г) + 5О2(г) = 2Н2О(ж) + 4СО2(г) + 2N2(г), следует воспользоваться формулой… 1) ∆Н0298 = 2∆Н0298, Н2О (ж) + 4∆Н0298, СО2 (г) - 4∆Н0298, НСN (г) 2) ∆Н0298 = ∆Н0298, Н2О (ж) + ∆Н0298, СО2 (г) - ∆Н0298, НСN (г) 3) ∆Н0298 = 4∆Н0298, НСN (г) + 2∆Н0298, Н2О (ж) - 4∆Н0298, СО2 (г) 4) ∆Н0298 = ∆Н0298, НСN (г) + ∆Н0298, Н2О (ж) - ∆Н0298, СО2 (г) 56) Неверно, что согласно 2 началу термодинамики… 1) теплота самопроизвольно переходит от более нагретого тела к менее нагретому 2) тепловой эффект обратной реакции больше теплового эффекта прямой реакции 3) КПД тепловой машины всегда меньше единицы (100%) 4) в изолированной системе самопроизвольно идут процессы, сопровождающиеся увеличением энтропии 57) Если прямая экзотермическая реакция протекает с уменьшением количества газообразных веществ, то согласно принципу Ле-Шателье, чтобы сместить равновесие в сторону продуктов, следует… 1 ) повысить давление 2) понизить давление 3) повысить температуру 4) добавить катализатор 58) Наибольшему значению энтропии соответствует состояние воды… 1) Н2О(ТВ) 273К 2) Н2О(ТВ) 200К 3) Н2О(ж) 273К 4) Н2О(г) 398К 59) Количественное соотношение между изменением внутренней энергии, теплотой и работой устанавливает______ закон термодинамики 1) третий 2 ) первый 3) второй 4) нулевой 60) Реакция CaCO3= CaO + CO2, для которой ∆Н=178кДж, ∆S=160Дж/моль×К, при стандартных условиях: 1) протекает в прямом направлении 2 ) протекает в обратном направлении 3) находится в равновесии 4) находится в колебательном режиме 61) Для экзотермического процесса синтеза аммиака одновременное понижение температуры и увеличение давления_________выход аммиака 1) не влияет на 2) сначала увеличивает, а затем уменьшает Увеличивает 4) уменьшает 62) Уравнение реакции, проходящей с увеличением энтропии, имеет вид… 1) NH4NO3(Т) = N2(Г) + 2 H2O(Г) 2) CaO(Т) + CO2(Г) =CaCO3(Т) 3) N2(Г) + O2(Г) = 2 NO(Г) 4) 2 H2S(Г) + 3 O2(Г) = 2 SO2(Г) + 2 H2O(Г) 63) Выберите соединения с макроэргическими связями: 1) Na3PO4 2) АТФ 3) глицин 4) фосфолипиды 2) Окислительно-восстановительные реакции. Электролиз. 1) Перманганат ион MnO4- в кислой среде восстанавливается до … 1) Mn 2) MnO42- 3)MnO2 4) Mn2+ 2) Оксид марганца (IV) MnO2 может проявлять в окислительно-восстановительных реакциях свойства и окислителя, и восстановителя 1) только окислителя 2) ни окислителя, ни восстановителя 3) только восстановителя 3) При электролизе водного раствора KCl на катоде выделяется … 1) H2 2) Cl2 3) O2 4) K 4) В качестве восстановителей в промышленных условиях используют… 1) СО и Н2 2) Н2О и H2SO4 (конц.) 3) Br2 и N2 4) MnO2 и CO2 5) Согласно уравнению Нернста потенциал электрода… 1) Зависит от его массы 2) Зависит от его природы 3) Не зависит от температуры
4) Не зависит от концентрации электролита 6) Окислителем в реакции KMnO4+KNO2+H2SO4®K2SO4+MnSO4+H2O является… 1) KNO2 2) H2SO4 3) MnSO4 4) KMnO4 В реакции K2Cr2O7 +6KI +7H2SO4=Cr2(SO4)3 + 4K2SO4 +3I2 +7H2O восстанавливается ион… 1) Н+ 2) Сr2O72- 3) I- 4) SO42- 36) При электролизе водного раствора СuCl2 с графитовым анодом на … 1) катоде выделяется водород 2) аноде выделяется кислород 3) аноде выделяется хлор 4) катоде выделяется хлор 37) Oкислительно-восстановительная реакция в стандартных условиях возможна, если… 1) электроотрицательность окислителя выше электроотрицательсности восстановителя 2) стандартный потенциал Е0 восстановителя имеет отрицательное значение 3) значение разности потенциалов полуреакций окисления и восстановления положительно 4) стандартный потенциал Е0 окислителя имеет положительное значение 38) Согласно схеме гальванического элемента Fe|Fe2+||Ni2+|Ni,… 1) электроны движутся от железного электрода к никелевому 2) никель окисляется 3) никелевый электрод является анодом 4) в процессе работы элемента на электроде осаждается железо 39) В системе, состоящей из луженого (покрытого оловом) железа при нарушении целостности покрытия в морской воде самопроизвольно протекает… 1) восстановление олова 2) окисление олова 3) восстановление железа 4) окисление железа 40) При электролизе водного раствора хлорида натрия на катоде протекает реакция… 1) 2H2O –4e → O2+4H+ 2) 2H2O +2e → H2+2OH- 3) Na+ +e→Na 4) 2H++2e→H2 41) При электролизе воды на аноде выделилось 11,2 л (н.у.) кислорода. Объем водорода, выделившегося на катоде равен ____ л (н.у.) 1) 22.4 2) 5.6 3) 44.8 4) 11.2 В реакции 2 KMnO4 + 3 Na2SO3 + H2O = 2MnO2 + 3 Na2SO4+ 2 KOH восстанавливается ион… 1) SO42- 2) K+ 3) MnO4- 4) SO32- 54) Максимальное значение ЭДС (при одинаковых концентрациях солей) будет у гальванического элемента Ме|Me(NO3)2||Cu(NO3)2|Cu, если стандартный потенциал второго металла равен ___В. 1) – 0,76 2) – 2,36 3) + 1,19 4) +1,50 55) Раствор, образующийся в результате электролиза водного раствора Cu(NO3)2 c инертными электродами, имеет ___ среду 1) Щелочную 2) Кислую 3) Нейтральную 4) Зависящую от времени электролиза! 56) Увеличение концентрации растворенного вещества в водном растворе происходит при электролизе раствора… 1) NiBr2 2) CuCl2 3) Na2SO4 4) MgI2 57) Краткое ионное уравнение реакции окисления меди хлоридом железа () имеет вид: 1) Cu0 + 2Fe3+ = Cu2+ + 2Fe2+ 2) 3Cu0 + 2Fe3+ = 3Cu2+ = 2Fe0 3)Cu0 + Fe3+ = Cu+ + Fe2+ 4) Cu0 + Fe3+ = 3Cu+ + Fe0 58) Согласно схеме гальванического элемента Zn| Zn2+|| Fe2+|Fe 1) цинк восстанавливается 2)цинковый электрод является анодом 3) железный электрод в процессе работы элемента растворяется
4) электроны движутся от железного электрода к цинковому 59) Коэффициент перед окислителем в реакции H2S + HNO3 = S + NO + H2O 1) 1 2)2 3) 3 4) 4 60) В реакции 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O ионы натрия 1) окисляются 2 ) не изменяют степени окисления 3) окисляются и восстанавливаются одновременно 4) восстанавливаются 61) Гидроксид хрома () Сr(OH)3 может проявлять в окислительно – восстановительных реакциях свойства: 1) только окислителя 2)и окислителя и восстановителя 3) только восстановителя 4) ни окислителя ни восстановителя 3) Способы выражения состава растворов. Коллигативные свойства растворов 1. Молярная масса неэлектролита, раствор 11,6 г которого в 200 г воды замерзает при -1,86°С ( 1) 232 2) 58 3) 77 4) 29 2. Массовая доля метанола в растворе, содержащем 60 г спирта и 40 г воды равна… 1) 1,5 2) 2 3) 0,6 4) 0,5 3. Метод определения молярной массы растворенного вещества по понижению температуры замерзания его раствора называется… 1) эбуллиоскопией 2) экстракцией 3) криоскопией 4) перегонкой 4. Если водные растворы различных неэлектролитов имеют одинаковую температуру кипения, то это растворы с одинаковой … 1) моляльной концентрацией 2) молярной концентрацией 3) мольной долей растворенного вещества 4) массовой долей растворенного вещества 5. Для приготовления 2 л 0,1 М раствора NaOH требуется ___ г растворенного вещества 1) 40 2) 16 3) 4 4) 8 6. Моляльная концентрация раствора, содержащего 18 г глюкозы (М (С6Н12О6)=180 г/моль) в 1 кг воды, равна… 1) 0,1 моль 2) 1 моль 3) 2 моль 4) 0,5 моль 7. Вычислите молярность 20% раствора хлороводородной кислоты. Плотность раствора принять равную 1,10 г/мл 1) 2,8 М 2) 25 % 3) 6,03 моль/л 4) 0,47 % 8. Массовая доля растворенного вещества в растворе рассчитывается по формуле: 1) 3) 9. Раствор, содержащий 9,2 г этилового спирта в 200 г воды 1) –0,186 2) 0,186 3) –1,86 4) 1,86 10. Массовая доля метанола в растворе, содержащем 60 г спирта и 40 г воды равна… 1) 1,5 2) 2 3) 0,6 4) 0,5 11. Молярная концентрация раствора, в 2 л которого содержится 4,25 г хлорида лития, равна ______ моль/л. 1) 0,5 2) 0,1 3) 0,05 4) 1 12. Укажите верное определение понятия «раствор» 1) это система, состоящая из растворенного вещества и воды 2) это гомогенные системы, состоящие из двух и более компонентов и продуктов их взаимодействия 3) это гетерогенные системы, состоящие из двух и более компонентов и продуктов их взаимодействия 4) все предложенные утверждения верны 13. Формула для расчета молярной концентрации имеет вид: 1) 2) 3) 4) При смешивании воды объемом 50 мл (плотностью 1 г/мл) и метилового спирта объемом 70 мл (плотностью 0,8 г/мл) получили раствор с плотностью 0,9 г/мл. Определите объемную долю метилового спирта в растворе 1) 47 моль/л 2) 68 моль/л 3) 59,4 % 4) 5,94 % 24. Какую массу медного купороса CuSO4×5H2O и воды надо взять для приготовления раствора сульфата меди (II) массой 40 кг с массовой долей CuSO4 2%? 1) 1,25 кг CuSO4×5H2O и 38,75 кг H2O 2) 100 кг CuSO4×5H2O и 56 кг H2O 3) 12 кг CuSO4×5H2O и 800 г H2O 4) 60 г CuSO4×5H2O и 1 кг H2O 3) 46 4) 23 70. Мольная доля растворенного вещества может быть выражена в … 1) моль/л Процентах
3) г/моль 4) моль/кг 71. Молярная масса вещества, при растворении 2,3 г которого в 100г воды, температура кипения раствора относительно температуры кипения воды повышается на 0,26 градуса(k=0,52 град×кг/моль), составляет 1) 60 2) 180 3) 46 4)98 72. 500 см3 водного раствора, содержащего 106 г Na2CO3, разбавили дистилированной водой в 2 раза. Молярная концентрация карбоната натрия в полученном растворе составляет____ моль/л 1) 10 2) 2 3) 1 4) 2,5 73. Водный раствор неэлектролита замерзает при -1,860С. Концентрация вещества в растворе составляет _____ моль/кг. (КН2О=1,86 град×кг/моль) 1) 10 2) 20 3 ) 1 4) 2 74. В 500 см3 растворили 105 г фторида натрия. Моляльность раствора составляет_____ моль/кг 1) 50 2) 5 3) 10 4) 15 75. После растворения нелетучего вещества в растворителе при температуре 200С давление насыщенного пара растворителя над раствором… 1) повышается 2) повышается до критического значения, затем понижается 3) понижается 4) не изменяется 76. К 250 г раствора, содержащего 25 г сульфата калия, добавили 250 см3 дистиллированной воды. Массовая доля растворённого вещества в растворе… 1) увеличилась в 2 раза 2) уменьшилась в 2 раза 3) уменьшилась в 2,1 раза 4) осталась неизменной Алкалоз - это 1) смещение рН крови в кислую область 2) смещение рН желудочного сока в щелочную область 3) смещение рН крови в щелочную область 4) смещение рН желчи в кислую область Ацидоз - это 1) 2) смещение рН желудочного сока в кислую область 3) смещение рН крови в щелочную область 4) смещение рН желчи в кислую область Уменьшается в 4 раза 4) увеличивается в 4 раза 21. В состоянии химического равновесия скорость прямой реакции ________ скорости обратной реакции. 1) равна 2) меньше 3) не зависит от 4) больше 22. Для увеличения скорости прямой реакции 2NO(г) + О2(г)↔2NO2(г) в 1000 раз, необходимо увеличить давление в ____раз 1) 500 2) 50 3) 330 4) 10 23. Правило Вант-Гоффа выражает зависимость скорости химической реакции от… Температуры 2) времени 3) концентрации 4) природы реагентов 24. Введение катализатора в систему приводит к ______ реакции. 1) изменению энтальпии 2) изменению энтропии ТЕСТЫ к МОДУЛЮ №1 (для итогового рубежного контроля)
|
|||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 1100; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.119.34 (0.014 с.) |

 реакции
реакции  , следует воспользоваться формулой…
, следует воспользоваться формулой…



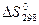 реакции
реакции  , следует воспользоваться формулой …
, следует воспользоваться формулой …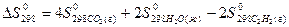
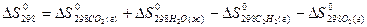

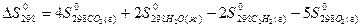
 ), равна _____ г/моль.
), равна _____ г/моль. 2)
2) 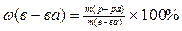
 4)
4) 
 , замерзает при температуре_____ °С
, замерзает при температуре_____ °С



 смещение рН крови в кислую область
смещение рН крови в кислую область


