
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физическое состояние нефти и газа при различных условиях в залежиСодержание книги
Поиск на нашем сайте
Свойства и состояние УВ зависят от их состава, давления и температуры. В залежах они могут находиться в жидком и газообразном состоянии или в виде газожидкостных смесей. В процессе разработки залежей в пластах и при подъеме на поверхность давление и температура непрерывно меняются, что сопровождается соответствующими изменениями состава газовой и жидкой фаз и переходом УВ из одной фазы в другую. Необходимо знать закономерности фазовых переходов, состояние и свойства УВ при различных условиях и учитывать их при подсчете запасов, проектировании и регулировании разработки проектировании и эксплуатации систем сбора и транспорта нефти и газа. Нефть и газ представляют собой смесь УВ преимущественно метанового (парафинового) (СnН2n+2), нафтенового (CnH2n) и в меньшем количестве ароматического (CnH2n-6) рядов. По физическому состоянию в поверхностных условиях УВ от СН4 до С4Н10 —газы; от С5Н12 до С16Н34 —жидкости и от С17Н34 до С35Н72 и выше — твердые вещества, называемые парафинами и церезинами. При большом количестве газа в пласте он может располагаться над нефтью в виде газовой шапки в повышенной части структуры. При этом часть жидких УВ нефти будет находиться в виде паров также и в газовой шапке. При высоком давлении в пласте плотность газа становится весьма значительной (приближающейся по величине к плотности легких углеводородных жидкостей). В этих условиях в сжатом газе растворяются значительные количества легкой нефти (С5Н12+С6Н14) подобно тому, как в бензине или других жидких УВ растворяются нефть и тяжелые битумы. В результате нефть иногда оказывается полностью растворенной в сжатом газе. При извлечении такого газа из залежи на поверхность в результате снижения давления и температуры растворенные в нем УВ конденсируются и выпадают в виде конденсата. Если же количество газа в залежи по сравнению с количеством нефти мало, а давление достаточно высокое, газ полностью растворяется в нефти и тогда газонефтяная смесь находится в пласте в жидком состоянии. С учетом сказанного в зависимости от условий залегания и количественного соотношения нефти и газа залежи УВ подразделяются на: 1) чисто газовые; 2) газоконденсатные; 3) газонефтяные или нефтегазовые (в зависимости от относительных размеров газовой шапки и нефтяной части залежи);
4) нефтяные (с различным содержанием растворенного газа). Газогидратные залежи содержат газ в твердом (гидратном) состоянии. Наличие такого газа обусловлено его способностью при определенных давлениях и температурах соединяться с водой и образовывать гидраты. Газогидратные залежи по физическим параметрам резко отличаются от обычных, поэтому подсчет запасов газа и разработка их во многом отличаются от применяемых для обычных месторождений природного газа. Районы распространения газогидратных залежей в основном приурочены к зоне распространения многолетнемерзлых пород. Состав и свойства газа. В нефтяном месторождении совместно с нефтью содержится газ; он может быть в растворенном состоянии или в виде свободного газа. Эти газы называются попутными (нефтяными). Углеводородные газы, залегающие в пластах, не содержащих нефть, называют природными (свободными), а месторождения – чисто газовыми.
Известны залежи с растворенным газом в пластовых водах; они пока практически не разрабатываются (кроме Японии и Китая).
Природные углеводородные газы представляют собой смесь предельных УВ вида СnН2n+2. Основным компонентом является метан СН4. Наряду с метаном в состав природных газов входят более тяжелые УВ, а также неуглеводородные компоненты: азот N, углекислый газ СО2, сероводород H2S, гелий Не, аргон Аr. Природные газы подразделяют на следующие группы. 1. Газ чисто газовых месторождений, представляющий собой сухой газ, почти свободный от тяжелых УВ. 2. Газы, добываемые из газоконденсатных месторождений, — смесь сухого газа и жидкого углеводородного конденсата. Углеводородный конденсат состоит из С5+высш. 3. Газы, добываемые вместе с нефтью (растворенные газы). Это физические смеси сухого газа, пропанбутановой фракции (жирного газа) и газового бензина. Газ, в составе которого УВ (С3, С4,) составляют не более 75 г/м3 называют сухим. При содержании более тяжелых УВ (свыше 150г/м3 газ называют жирным). Газовые смеси характеризуются массовыми или молярными концентрациями компонентов. Для характеристики газовой смеси необходимо знать ее среднюю молекулярную массу, среднюю плотность или относительную плотность по воздуху. Молекулярная масса природного газа
где Мi — молекулярная масса i-го компонента; Xi — объемное содержание i-го компонента, доли ед. Для реальных газов обычно М = 16—20. Плотность газа ρг рассчитывается по формуле
где Vм — объем 1 моля газа при стандартных условиях. Обычно значение ρг находится в пределах 0,73— 1,0 кг/м3. Чаще пользуются относительной плотностью газа по воздуху ρг.в равной отношению плотности газа ρг к плотности воздуха ρв взятой при тех же давлении и температуре:
Если ρг и ρв определяются при стандартных условиях, то ρг= 1,293 кг/м3 и ρв = ρг /1,293 кг/м3. Уравнения состояния газов используются для определения многих физических свойств природных газов. Уравнением состояния называется аналитическая зависимость между давлением, объемом и температурой. Состояние газов в условиях высоких давления и температуры определяется уравнением Клайперона — Менделеева: pV = NRT, (1.12) где р — давление; V — объем идеального газа; N — число киломолей газа; R — универсальная газовая постоянная; Т — температура. Эти уравнения применимы для идеальных газов. Идеальным называется газ, силами взаимодействия между молекулами которого пренебрегают. Реальные углеводородные газы не подчиняются законам идеальных газов. Поэтому уравнение Клайперона — Менделеева для реальных газов записывается в виде pV = ZNRT, (1.13) где Z — коэффициент сверхсжимаемости реальных газов, зависящий от давления, температуры и состава газа и характеризующий степень отклонения реального газа от закона для идеальных газов. Коэффициент сверхсжимаемости Z реальных газов — это отношение объемов равного числа молей реального V и идеального Vи газов при одинаковых термобарических условиях (т.е. при одинаковых давлении и температуре): Z = V/Vи Значения коэффициентов сверхсжимаемости наиболее надежно могут быть определены на основе лабораторных исследований пластовых проб газов. При отсутствии таких исследований прибегают к расчетному методу оценки Z по графику Г. Брауна. Для пользования графиком необходимо знать так называемые приведенные псевдокритическое давление и псевдокритическую температуру. Суть этих понятий состоит в следующем. Объем углеводородных газов меняется в зависимости от температуры и давления примерно в соответствии с рис. 4. Каждая из кривых соответствует фазовым изменениям однокомпонентного газа при постоянной температуре и имеет три участка. Отрезок справа от пунктирной линии соответствует газовой фазе, участок под пунктирной линией — двухфазной газожидкостной области и отрезок слева от пунктирной линии — жидкой фазе. Отрезок пунктирной кривой вправо от максимума в точке С называется кривой точек конденсации (точек росы), а влево от максимума — кривой точек парообразования. Точка С называется критической. Значения давления и температуры, соответствующие критической точке С, также называются критическими. Другими словами, критическойназывается такаятемпература, выше которой газ не может быть превращен в жидкость ни при каком давлении. Критическим давлением называется давление, соответствующее критической точке перехода газа в жидкое состояние. С приближением значений давления и температуры к критическим свойства газовой и жидкой фаз становятся одинаковыми, поверхность раздела между ними исчезает и плотности их уравниваются. С появлением в системе двух и более компонентов в закономерностях фазовых изменений возникают особенности, отличающие их поведение от поведения однокомпонентного газа. Не останавливаясь на подробностях, следует отметить, что критическая температура смеси находится между критическими температурами компонентов, а критическое давление смеси всегда выше, чем критическое давление любого компонента. Для определения коэффициента сверхсжимаемости Z реальных газов, представляющих собой многокомпонентную смесь, находят средние из значений критических давлений и температур каждого компонента. Эти средние называются псевдокритическим давлением Рпкр и псевдокритической температурой Тпкр.
Приведенные псевдокритические давление и температура, необходимые для пользования графиком Брауна, представляют собой псевдокритические значения, приведенные к конкретным давлению и температуре (к пластовым, стандартным или каким-либо другим условиям): Pпр=Р/Рпкр, (1.14) Тпр=Т/Тпкр, (1.15) где Р и Т— конкретные давление и температура, для которых определяется Z. Коэффициент сверхсжимаемости Z обязательно используется при подсчете запасов газа, прогнозировании изменения давления в газовой залежи и решении других задач. Влагосодержание природных газов связано с тем, что природные газы и газоконденсатные смеси контактируют с пластовыми водами различных форм и вследствие чего содержат определенное количество паров воды. Концентрация водяных паров в газе зависит от его состава, давления, температуры. Отношение количества водяных паров (в долях единицы или процентах), находящихся в газе, к максимально возможному содержанию водяных паров в том же газе при тех же условиях называют относительной влажностью газа. Она характеризует степень насыщения газа водяным паром. Количество водяных паров, находящихся в единице объема или массы газа (г/м3 или г/кг), называют абсолютной влажностью. Пары воды, присутствующие в газах и газоконденсатных смесях, влияют на фазовые превращения углеводородных систем. При определенных термодинамических условиях вода может выделяться из газа (конденсироваться), т.е. переходить в капельно-жидкое состояние. В газоконденсатных системах могут одновременно выделяться вода и конденсат. В присутствии воды давление начала конденсации УВ увеличивается. Объемный коэффициент пластового газа bг представляющий собой отношение объема газа в пластовых условиях Vпл.г к объему того же количества газа Vст, который он занимает в стандартных условиях, можно найти с помощью уравнения Клайперона — Менделеева:
bг = Vпл.г/Vст = Z(Pcт×Тпл/(Рпл×Тст), (1.16) где Рпл, Тпл, Pcт,××Тст — давление и температура соответственно в пластовых и стандартных условиях. Значение величины bг имеет большое значение, так как объем газа в пластовых условиях на два порядка (примерно в 100 раз) меньше, чем в стандартных условиях.
Среди природных углеводородов выделяют три основные группы (Р.И. Вяхирев, Ю.П. Коротаев, Н.И. Кабанов).
1. Метановые парафиновые углеводороды (алканы) с общей формулой СлН2л+2. Это предельные насыщенные соединения. Эти газы, как правило, состоят на 90-98 % из метана (СН4). Среди тяжелых газообразных углеводородов в составе природного газа преобладают этан и пропан; в меньших количествах содержатся бутан, пентан, гептан и более тяжелые углеводороды. Они образуют с метаном единый гомологический ряд, и их называют гомологами метана. Бутан и более тяжелые углеводороды имеют изомеры. Некоторые физико-химические свойства алканов приведены в табл. 2.1.
2. Нафтеновые углеводороды - алкены (цикланы) с общей формулой СлН2л. Это непредельные соединения. Но благодаря замыканию углеводородной цепи в кольцо они имеют насыщенный характер. Среди тяжелых газообразных углеводородов непредельные углеводороды (алкены) обнаруживаются в виде следов или в небольших количествах. Среди них часто встречается этилен С2Н2. В эту же группу входят пропилен С3Н6 и бутилен С4Н8. При атмосферном давлении все они газы.
3. Ароматические углеводороды, или арены, с простейшей формулой СЛН2л–6 содержат в своем составе ароматическое ядро бензола. Они часто входят в состав конденсата газоконденсатных месторождений.
Природные газы состоят из углеводородов метанового ряда, а также азота (N2), углекислого газа (СО2), сероводорода (Н2S), инертных газов: гелия (Не), аргона (Ar), криптона (Kr), ксенона (Хе); ртути. Содержание метана часто превышает 85–98 %. Содержание азота в природном газе не превышает 10 % (обычно 2–3 %); содержание углекислого газа меняется от долей процента до 10-25 %. Количество сероводорода колеблется от 0 до 20 % (иногда больше).
Природные газы подразделяют на:
1)сухой газ с небольшим содержанием тяжелых углеводородов, добываемый из чисто газовых месторождений;
2)смесь сухого газа, пропан-бутановой фракции (сжиженного газа) и газового бензина, добываемую вместе с нефтью;
3)сухой газ и жидкий углеводородный конденсат, добываемые из газоконденсатных месторождений. Углеводородный конденсат состоит из большого числа тяжелых углеводородов, являющихся ценнейшим сырьем нефтехимической и химической промышленности.
Метан очень устойчив. Он может сохраняться без изменений сотни миллионов лет. При утечке метана и достижении его концентрации (по объему) в воздухе 5,35 % любая искра вызывает взрыв. Метан и его гомологи растворяются в воде и нефти. Его растворимость растет с повышением давления. Вязкость газов в зависимости от изменения параметров, характеризующих их состояние, изменяется сложным образом. Динамическая вязкость ц газа связана с его плотностью рг, средней длиной свободного пути X и средней скоростью молекул v:
ц. = pvX/3.
Эта формула определяет зависимость динамической вязкости газа от давления и температуры, так как при повышении давления плотность газа возрастает, но при этом уменьшается средняя длина свободного пробега молекул, а скорость их остается постоянной. С увеличением температуры вязкость газа возрастает.
|
|||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 781; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.210.224 (0.012 с.) |

 (1.9)
(1.9)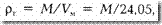 (1.10)
(1.10)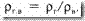 (1.11)
(1.11)


